16/04/2006
I den moderne medicinske verden er kampen mod sygdomme i stigende grad en kamp på molekylært niveau. For at udvikle effektive lægemidler er vi nødt til at forstå præcis, hvordan kroppens mindste byggeklodser fungerer, og hvordan de interagerer. Her træder et utroligt spændende og kraftfuldt felt ind på scenen: strukturel bioinformatik. Det lyder måske komplekst, men i sin kerne handler det om at bruge computerkraft til at visualisere og analysere den tredimensionelle arkitektur af biologiske molekyler, især proteiner. Ved at forstå deres form kan vi forstå deres funktion – og hvordan vi kan påvirke den til vores fordel.
Forestil dig, at en sygdom er forårsaget af et defekt tandhjul i en kompleks maskine. Traditionel medicin har måske forsøgt at smøre hele maskinen eller bremse den ned. Strukturel bioinformatik giver os derimod et detaljeret blik på selve tandhjulet. Vi kan se dets form, dets hakker og dets bevægelser. Med den viden kan vi designe et specialværktøj – et lægemiddel – der passer perfekt ind og enten reparerer eller blokerer det defekte tandhjul, uden at påvirke resten af maskinen unødigt. Dette er præcisionen og potentialet, som dette felt tilbyder.
Hvorfor er Proteinstruktur Altafgørende?
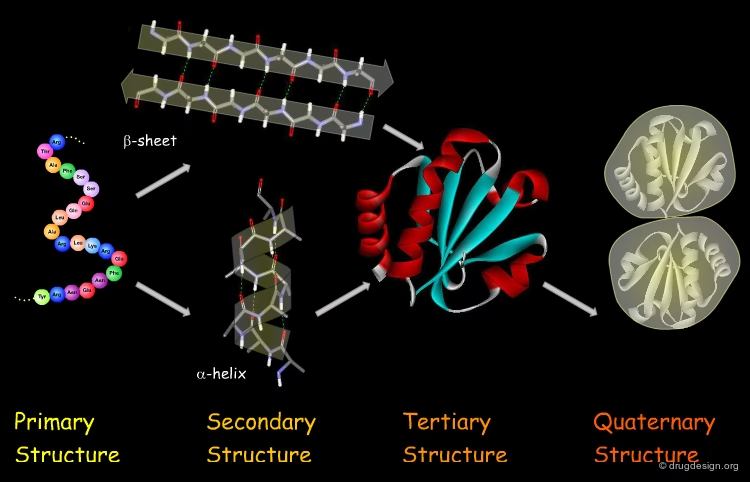
For at værdsætte betydningen af strukturel bioinformatik, må vi først forstå proteiner. De er cellens arbejdsheste og udfører næsten alle opgaver i en levende organisme. De fungerer som enzymer, der katalyserer kemiske reaktioner, som signalmolekyler, der sender beskeder, som strukturelle komponenter, der giver cellerne form, og som transportører, der flytter stoffer rundt. Hvert protein har en unik tredimensionel form, der er afgørende for dets specifikke funktion. Denne form opstår gennem en proces kaldet proteinfoldning, hvor en lang kæde af aminosyrer krøller sig sammen til en kompleks og stabil struktur.
En lille fejl i denne struktur, ofte forårsaget af en genetisk mutation, kan have katastrofale konsekvenser. Et protein kan miste sin funktion, eller det kan begynde at udføre en ny, skadelig funktion. Mange sygdomme, fra cystisk fibrose til visse former for kræft og Alzheimers, er direkte forbundet med fejlfoldede eller dysfunktionelle proteiner. Derfor er det at kunne se og analysere disse strukturer ikke bare en akademisk øvelse; det er en fundamental nøgle til at forstå og bekæmpe sygdomme.
Kerneværktøjerne i Strukturel Bioinformatik
Feltet bygger på en række computerbaserede metoder og ressourcer, der arbejder sammen for at afkode molekylernes hemmeligheder.
Proteindatabanken (PDB) - Et Digitalt Bibliotek af Strukturer
Fundamentet for næsten alt arbejde inden for strukturel bioinformatik er Proteindatabanken (PDB). Dette er et gigantisk, frit tilgængeligt online arkiv, der indeholder tusindvis af eksperimentelt bestemte 3D-strukturer af proteiner, nukleinsyrer (DNA og RNA) og andre komplekse molekyler. Forskere fra hele verden indsender deres data til denne bank, hvilket skaber en uvurderlig ressource for hele det videnskabelige samfund. Når en forsker ønsker at studere et bestemt protein, er det første skridt ofte at søge i PDB for at se, om dets struktur allerede er kendt.
Strukturel Sammenligning - At Finde Familiære Former
Naturen genbruger ofte succesfulde designs. To proteiner kan have meget forskellige aminosyresekvenser, men alligevel folde sig til næsten identiske 3D-strukturer og udføre lignende funktioner. Strukturel alignment er en beregningsmetode, der sammenligner to eller flere molekylære strukturer ved at overlejre dem i et 3D-rum for at finde den bedst mulige pasform. Kvaliteten af denne pasform måles ofte ved hjælp af en metrik kaldet RMSD (Root-Mean-Square Deviation), som er den gennemsnitlige afstand mellem de tilsvarende atomer i de overlejrede strukturer. En lav RMSD-værdi indikerer en høj grad af strukturel lighed. Dette kan afsløre evolutionære slægtskaber, som man aldrig ville have fundet ved kun at kigge på den genetiske kode.
Molekylær Docking - Det Digitale Håndtryk
Et af de mest kraftfulde værktøjer er molekylær docking. Dette er en simuleringsproces, der forudsiger, hvordan to molekyler vil binde til hinanden. Typisk bruges det til at forudsige, hvordan et lille molekyle (en potentiel lægemiddelkandidat, kaldet en ligand) vil passe ind i en specifik lomme eller et aktivt site på et større protein (målet eller receptoren). Computeren tester millioner af mulige orienteringer og konformationer af liganden i forhold til proteinet og beregner en score for hver position. Scoren afspejler, hvor stærk og stabil bindingen forventes at være. Høj-scorende positioner, eller 'poses', giver forskerne et detaljeret billede af de afgørende interaktioner – hvilke atomer i lægemidlet der interagerer med hvilke atomer i proteinet. Dette er essentielt for rationelt lægemiddeldesign, hvor man kan forbedre et lægemiddels effektivitet ved at modificere dets kemiske struktur for at optimere disse interaktioner.

Virtuel Screening - Jagten på Guldkornene
Mens molekylær docking analyserer interaktionen mellem ét lægemiddel og ét protein, tager virtuel screening processen til et helt nyt niveau. Her bruger man docking-algoritmer til systematisk at teste enorme digitale biblioteker, der kan indeholde millioner af forskellige kemiske forbindelser, mod et enkelt proteinmål. Målet er hurtigt at identificere de få forbindelser, der har den højeste sandsynlighed for at binde sig stærkt og specifikt til målet. Dette sparer utrolige mængder tid og penge sammenlignet med traditionel high-throughput screening i laboratoriet, hvor hver enkelt forbindelse skal testes fysiskt. Virtuel screening fungerer som en effektiv si, der frasorterer de uegnede kandidater og efterlader en lille, håndterbar gruppe af lovende 'hits', som derefter kan syntetiseres og testes i rigtige biologiske forsøg.
Molekylær Dynamik - At Se Molekyler i Bevægelse
Proteiner er ikke statiske, frosne strukturer. De er dynamiske maskiner, der konstant vibrerer, vrider sig og ændrer form for at udføre deres funktion. Molekylær dynamik (MD) er en simuleringsmetode, der skaber en 'film' af et molekyles bevægelser over tid. Ved at anvende fysikkens love på hvert enkelt atom i systemet kan forskere observere, hvordan et protein opfører sig, hvordan det interagerer med vandmolekyler, og hvordan bindingen af et lægemiddel kan ændre dets dynamik. Disse simulationer kan afsløre vigtige detaljer om et proteins funktion, som er umulige at se i en statisk struktur.
Sammenligning af Metoder: Laboratorie vs. Computer
For at illustrere fordelene ved en computerbaseret tilgang, er her en sammenligning mellem traditionelle laboratoriemetoder og strukturel bioinformatik i den tidlige fase af lægemiddelopdagelse.
| Parameter | Traditionel Laboratoriemetode | Strukturel Bioinformatik (In Silico) |
|---|---|---|
| Hastighed | Langsom (uger til måneder for screening) | Hurtig (dage til uger for screening af millioner) |
| Omkostning | Meget høj (kemikalier, udstyr, personale) | Lavere (primært beregningsressourcer) |
| Skala | Begrænset af fysiske biblioteker | Næsten ubegrænset (virtuelle biblioteker) |
| Indsigt | Giver et ja/nej svar (binder/binder ikke) | Giver detaljeret indsigt i bindingsmåde |
Ofte Stillede Spørgsmål
Er strukturel bioinformatik kun for specialiserede forskere?
Ja, udførelsen af analyserne kræver specialiseret viden inden for biologi, kemi og datalogi. Resultaterne har dog en bred indvirkning på os alle. De lægemidler, der udvikles ved hjælp af disse metoder, ender på apotekernes hylder og bruges til at behandle patienter verden over. Så selvom det er et ekspertfelt, er dets formål at forbedre den generelle folkesundhed.
Hvor præcise er disse computerforudsigelser?
Præcisionen er blevet markant forbedret over de seneste år, især med fremkomsten af kunstig intelligens som f.eks. AlphaFold til strukturforudsigelse. Dog er computerforudsigelser stadig netop det – forudsigelser. De fungerer som stærke hypoteser, der kan guide og prioritere det eksperimentelle arbejde. Laboratoriebekræftelse er stadig et absolut nødvendigt og afgørende skridt i processen med at udvikle et nyt lægemiddel.
Hvad er forskellen på almindelig bioinformatik og strukturel bioinformatik?
Bioinformatik er et meget bredt felt, der omfatter enhver brug af computere til at analysere biologiske data. Dette kan inkludere analyse af DNA-sekvenser (genomik), genekspression (transkriptomik) eller proteinsæt (proteomik). Strukturel bioinformatik er en specialiseret underdisciplin af bioinformatik, der udelukkende fokuserer på den tredimensionelle struktur af makromolekyler og de fysiske principper, der styrer deres interaktioner.
Konklusion: Arkitekter af Fremtidens Behandlinger
Strukturel bioinformatik har revolutioneret vores tilgang til at forstå biologi og udvikle medicin. Ved at omdanne biologiske problemer til beregningsmæssige udfordringer giver det os mulighed for at se, analysere og manipulere livets molekyler med en hidtil uset præcision. Fra at designe målrettede kræftlægemidler til at udvikle nye antibiotika mod resistente bakterier, er værktøjerne fra dette felt i frontlinjen af medicinsk innovation. Det er en bro mellem den digitale verden og den biologiske verden, og det er på denne bro, at mange af fremtidens sundhedsmæssige gennembrud vil blive bygget.
Hvis du vil læse andre artikler, der ligner Strukturel Bioinformatik: Design af Fremtidens Medicin, kan du besøge kategorien Sundhed.
