14/05/2005
Batterier er en uundværlig del af vores moderne liv. De driver alt fra vores smartphones og bærbare computere til elbiler og livsvigtigt medicinsk udstyr. Men hvordan fungerer disse små kraftværker egentlig? Kernen i et batteris funktion er en elegant omdannelse af kemisk energi til elektrisk energi. Denne artikel dykker ned i videnskaben bag batterier, forklarer de komplekse processer, der finder sted indeni, og afdækker de nøglefaktorer, der påvirker deres ydeevne og levetid. Uanset om du er nysgerrig af natur eller en teknologi-entusiast, vil denne omfattende guide give dig en klar forståelse af batteriets indre liv.
Sådan fungerer et batteri: Fra kemi til strøm
Grundlæggende fungerer et batteri ved at omdanne lagret kemisk energi til brugbar elektrisk energi gennem en proces, der kaldes en redoxreaktion. Dette sker ved hjælp af tre hovedkomponenter: en negativ elektrode (anoden), en positiv elektrode (katoden) og en kemisk separator (elektrolytten). Når du tilslutter et batteri til en enhed, skabes der et lukket kredsløb, som tillader elektroner at flyde fra anoden til katoden. Denne strøm af elektroner er det, vi kender som elektricitet, og den driver din enhed.
Afladningsprocessen: Når batteriet leverer strøm
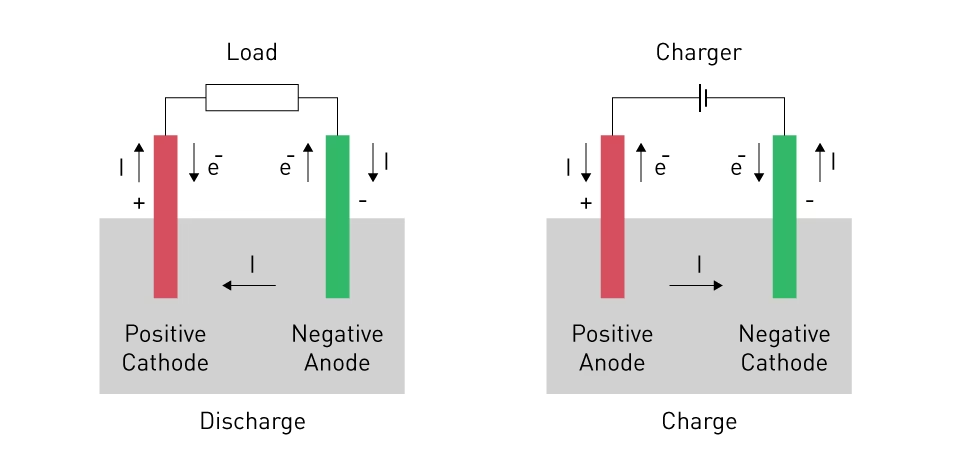
Afladningsprocessen er det øjeblik, hvor batteriet arbejder for dig. Det er her, den lagrede kemiske energi frigives som elektrisk energi. Processen starter ved anoden, som ofte er lavet af materialer som zink, lithium eller grafit. Her sker en oxidationsreaktion, hvor anodematerialet afgiver elektroner. Disse frigjorte elektroner kan ikke passere direkte gennem elektrolytten til katoden. I stedet tvinges de ud i det eksterne kredsløb – altså gennem din telefon, lommelygte eller bil – og udfører arbejde på deres vej.
Samtidig med at elektronerne rejser gennem det eksterne kredsløb, bevæger positive ioner sig fra anoden gennem elektrolytten til katoden. Elektrolytten er en afgørende komponent, der fungerer som en portvagt: den tillader kun ioner at passere, ikke elektroner. Dette forhindrer en intern kortslutning og sikrer, at elektronerne tager den lange vej gennem din enhed. Når elektronerne ankommer til katoden (ofte lavet af materialer som mangandioxid eller lithium-cobalt-oxid), forenes de med de ankomne ioner i en reduktionsreaktion. Denne komplette cyklus af elektron- og ionvandring skaber den elektriske strøm, der driver vores verden.
Opladningsprocessen: Genopfyldning af energilageret
For genopladelige batterier (sekundære batterier) er opladningsprocessen lige så vigtig som afladningen. Opladning er i bund og grund en omvendt afladning. Ved at tilslutte batteriet til en ekstern strømkilde, som en oplader i en stikkontakt, tvinger man den kemiske proces til at køre baglæns.
Under opladning påfører den eksterne strømkilde en spænding, der er højere end batteriets egen spænding. Dette tvinger elektronerne til at bevæge sig fra katoden tilbage til anoden gennem det eksterne kredsløb. Samtidig tvinges ionerne til at bevæge sig fra katoden tilbage gennem elektrolytten for at genindlejre sig i anodematerialet. Denne proces genopretter de oprindelige kemiske tilstande i anoden og katoden, og batteriet er igen klar til at levere strøm. Det er denne reversible natur, der adskiller genopladelige batterier fra engangsbatterier.
De kemiske reaktioner i batteriets hjerte
For at forstå batterier fuldt ud, er det nødvendigt at se nærmere på de forskellige typer og de specifikke roller, som anoden, katoden og elektrolytten spiller.
Primære vs. Sekundære Batterier
Der findes to overordnede kategorier af batterier, som adskiller sig markant i deres kemiske design og anvendelse.
- Primære batterier (Engangsbatterier): Disse er designet til at blive brugt én gang og derefter kasseret. De kemiske reaktioner i disse batterier er irreversible. Når reaktanterne er opbrugt, kan batteriet ikke længere producere strøm. Eksempler inkluderer alkaliske batterier (AA, AAA) i fjernbetjeninger og zink-kul-batterier.
- Sekundære batterier (Genopladelige batterier): Disse er designet til at blive opladet og afladet hundredvis eller endda tusindvis af gange. Deres kemiske reaktioner er reversible, hvilket gør det muligt at genoprette deres energilager. Eksempler er lithium-ion-batterier i smartphones og elbiler samt bly-syre-batterier i traditionelle biler.
Her er en sammenligningstabel for at illustrere forskellene:
| Egenskab | Primære Batterier (Engangsbatterier) | Sekundære Batterier (Genopladelige) |
|---|---|---|
| Genopladelighed | Nej, reaktionerne er irreversible. | Ja, reaktionerne er reversible. |
| Typiske Anvendelser | Fjernbetjeninger, legetøj, lommelygter, røgdetektorer. | Smartphones, laptops, elbiler, elværktøj. |
| Langtidsomkostning | Højere, da de konstant skal udskiftes. | Lavere, på trods af en højere startpris. |
| Miljøpåvirkning | Større affaldsmængde. | Mindre affald, men produktion og genanvendelse er ressourcekrævende. |
Anoden, Katoden og Elektrolyttens Roller
Disse tre komponenter udgør batteriets fundamentale treenighed. Valget af materialer til hver del bestemmer batteriets spænding, kapacitet, levetid og sikkerhed.
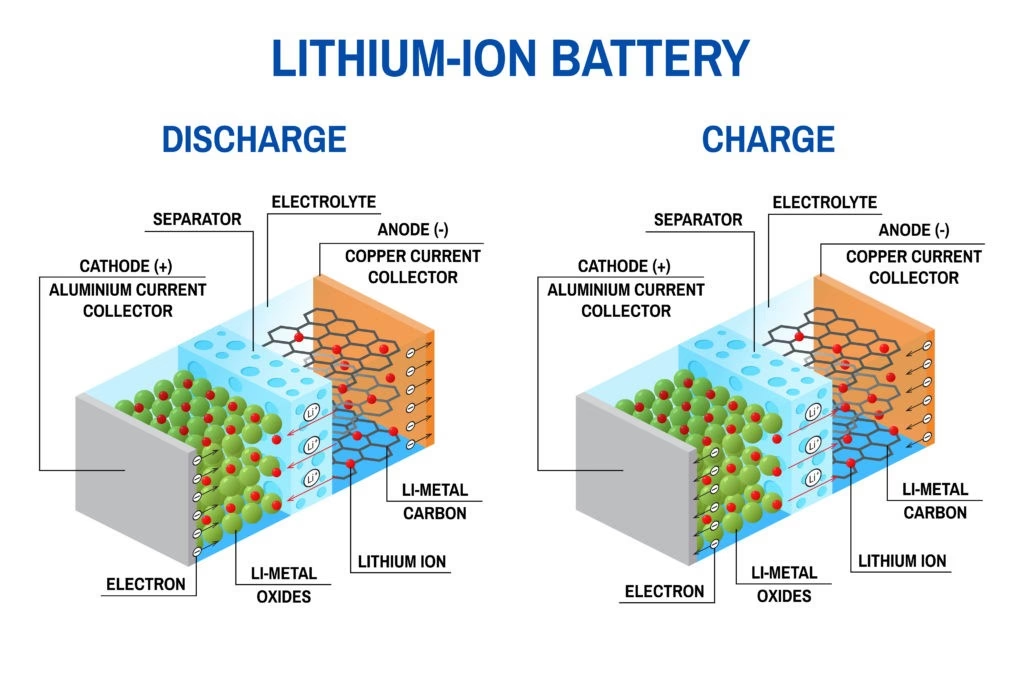
- Anoden (-): Er den negative terminal. Det er herfra elektronerne frigives under afladning. Materialet skal være godt til at afgive elektroner (oxidation). I lithium-ion-batterier er anoden typisk lavet af grafit, som kan huse lithium-ioner.
- Katoden (+): Er den positive terminal. Det er her elektronerne modtages under afladning. Materialet skal være godt til at modtage elektroner (reduktion). I lithium-ion-batterier bruges ofte metaloxider som lithium-cobalt-oxid.
- Elektrolytten: Er mediet, der adskiller anoden og katoden og transporterer ioner mellem dem. Det kan være en væske, en gel eller et fast stof. Elektrolyttens sammensætning er afgørende for batteriets ydeevne ved forskellige temperaturer og for dets generelle sikkerhed.
Faktorer, der påvirker batteriets ydeevne
Selv det bedste batteri vil ikke yde optimalt under alle forhold. Flere faktorer kan have en dramatisk indvirkning på et batteris kapacitet og levetid.

1. Temperatur: Ekstreme temperaturer er en af batteriets største fjender. Høje temperaturer (f.eks. en telefon efterladt i en varm bil) accelererer de kemiske reaktioner inde i batteriet. Dette fører til hurtigere selvudladning og permanent nedbrydning af de interne komponenter, hvilket forkorter batteriets levetid. Omvendt nedsætter meget lave temperaturer de kemiske reaktioners hastighed, hvilket midlertidigt reducerer batteriets kapacitet og evne til at levere strøm.
2. Afladningshastighed (C-rate): Den hastighed, hvormed et batteri aflades, påvirker dets effektivitet. At trække en stor mængde strøm på kort tid (høj afladningshastighed) er mindre effektivt og genererer mere varme, hvilket kan føre til et større samlet kapacitetstab over tid sammenlignet med en langsom, jævn afladning.
3. Cykling (Opladningscyklusser): En opladningscyklus defineres som en fuld afladning efterfulgt af en fuld opladning. Hver gang et genopladeligt batteri gennemgår en cyklus, sker der en lille, permanent nedbrydning af elektrodematerialerne. Over tid akkumuleres denne slitage og reducerer batteriets evne til at holde på en opladning. Derfor har alle genopladelige batterier en begrænset levetid, typisk angivet i antal cyklusser.
4. Opbevaringsforhold: Hvordan du opbevarer batterier, når de ikke er i brug, har stor betydning for deres holdbarhed. For langtidsopbevaring anbefales det generelt at opbevare lithium-ion-batterier ved en opladning på omkring 40-50% på et køligt, tørt sted. At opbevare et batteri fuldt opladet eller helt afladet i længere perioder kan fremskynde den kemiske nedbrydning.
Konklusion
At forstå, hvordan et batteri fungerer, er mere end blot teknisk nysgerrighed; det er nøglen til at få mest muligt ud af de enheder, der definerer vores dagligdag. Fra de grundlæggende principper om redoxreaktioner til de praktiske implikationer af temperatur og opladningsvaner, er batteriets funktion en kompleks, men fascinerende dans af kemi og fysik. Ved at respektere disse processer og anvende god praksis for brug og opbevaring, kan vi ikke kun forlænge levetiden af vores enheder, men også bidrage til en mere bæredygtig teknologisk fremtid.
Ofte Stillede Spørgsmål (FAQ)
Hvad er 'memory effect' i batterier?
Memory effect er et fænomen, der primært påvirkede ældre genopladelige batterityper som Nikkel-Cadmium (NiCd). Hvis batteriet gentagne gange blev opladet, før det var helt afladet, kunne det 'huske' det lavere energiniveau og nægte at levere sin fulde kapacitet. Moderne lithium-ion-batterier lider praktisk talt ikke af denne effekt, så du kan trygt oplade dem, når det passer dig.
Hvorfor mister mit batteri kapacitet over tid?
Alle genopladelige batterier mister kapacitet over tid på grund af kemisk nedbrydning. Hver opladnings- og afladningscyklus forårsager mikroskopisk slitage på anoden og katoden. Derudover sker der en langsom, men konstant, nedbrydning af elektrolytten. Faktorer som høj varme, dybe afladninger og opbevaring ved 100% opladning kan fremskynde denne proces betydeligt.
Hvordan opbevarer jeg bedst batterier, jeg ikke bruger?
For de fleste moderne batterier (lithium-ion) er den ideelle opbevaring at lade dem være omkring 40-50% opladede og placere dem et køligt og tørt sted. Undgå ekstreme temperaturer. For engangsbatterier (alkaliske) er det bedst at opbevare dem på et tørt sted ved stuetemperatur og undgå at lade dem sidde i enheder, der ikke bruges i lang tid, for at undgå lækage.
Er det farligt at overlade et batteri?
Moderne enheder med lithium-ion-batterier har indbyggede beskyttelseskredsløb, der automatisk stopper opladningen, når batteriet er fuldt. Derfor er det generelt sikkert at lade din telefon eller laptop være tilsluttet natten over. Dog kan konstant at holde batteriet på 100% opladning stresse det kemisk og potentielt forkorte dets samlede levetid en smule.
Hvis du vil læse andre artikler, der ligner Hvordan virker et batteri? En dybdegående guide, kan du besøge kategorien Teknologi.