18/11/2021
Fremstilling af medicinsk udstyr er en af de mest regulerede industrier i verden, og med god grund. Hver eneste komponent, hver samling og hver proces kan have en direkte indvirkning på en patients helbred og sikkerhed. Derfor er det ikke nok blot at producere et stykke udstyr; producenten skal kunne bevise, at udstyret konsekvent lever op til de højeste standarder for kvalitet og sikkerhed. Her kommer procesvalidering ind i billedet som en fundamental og uomgængelig disciplin. Det er ikke blot en teknisk øvelse, men en hjørnesten i moderne kvalitetssikring, der sikrer, at det endelige produkt er sikkert og effektivt, hver eneste gang.
Hvad er Procesvalidering helt præcist?
Procesvalidering er den dokumenterede proces, hvor man med en høj grad af sikkerhed fastslår, at en specifik fremstillingsproces konsekvent vil producere et produkt, der opfylder sine forudbestemte specifikationer og kvalitetsattributter. I mere simple termer handler det om at bevise, at din 'opskrift' virker hver gang, og ikke kun ved et tilfælde.
Dette er især vigtigt for processer, hvor resultatet ikke fuldt ud kan verificeres gennem efterfølgende inspektion og test af det færdige produkt. Hvis man for eksempel skulle skære hvert eneste produkt op for at kontrollere en intern svejsning, ville man ikke have nogen produkter tilbage at sælge. I stedet validerer man selve svejseprocessen for at sikre, at hver svejsning, der udføres under de kontrollerede forhold, er perfekt.
Når Loven Kræver Validering: Den Amerikanske QSR
For producenter, der ønsker at sælge medicinsk udstyr på det amerikanske marked, er kravene til procesvalidering klart defineret i lovgivningen. Specifikt i 21 CFR Part 820, også kendt som Quality System Regulation (QSR), fastslår sektion 820.75, hvornår validering er påkrævet.
Hovedprincippet er krystalklart: Procesvalidering skal udføres, når resultaterne af en proces ikke kan verificeres fuldt ud ved efterfølgende inspektion og test.
Eksempler på sådanne processer inkluderer, men er ikke begrænset til:
- Steriliseringsprocesser: Man kan ikke teste hvert enkelt produkt for sterilitet uden at bryde emballagen. Derfor valideres hele steriliseringscyklussen (f.eks. med ethylenoxid, damp eller stråling).
- Aseptisk påfyldning: Processen med at fylde sterile beholdere med et sterilt produkt i et sterilt miljø.
- Svejseprocesser: Både for metaller og plast, hvor styrken og integriteten af svejsningen er kritisk, men ikke kan ses udefra.
- Støbeprocesser: For komplekse plast- eller metalkomponenter, hvor interne dimensioner og materialetæthed er afgørende.
- Varmeforsegling: Forsegling af sterile barrieresystemer (emballage), hvor en utæt forsegling kan kompromittere produktets sterilitet.
Ud over selve kravet om validering stiller QSR også krav om, at producenter etablerer og vedligeholder procedurer for overvågning og kontrol af procesparametre for de validerede processer. Dette sikrer, at processen forbliver i en valideret tilstand. Desuden skal personalet, der udfører disse processer, være behørigt kvalificeret og trænet. Enhver ændring eller afvigelse fra den validerede proces skal evalueres nøje, og om nødvendigt skal der udføres en revalidering. Og altafgørende er kravet om dokumentation – hvis det ikke er skrevet ned, er det ikke sket.
Valideringens Tre Musketerer: IQ, OQ og PQ
En robust procesvalidering følger typisk en struktureret tilgang opdelt i tre faser. Disse faser sikrer, at alt fra udstyrets installation til den løbende produktion er under fuld kontrol.
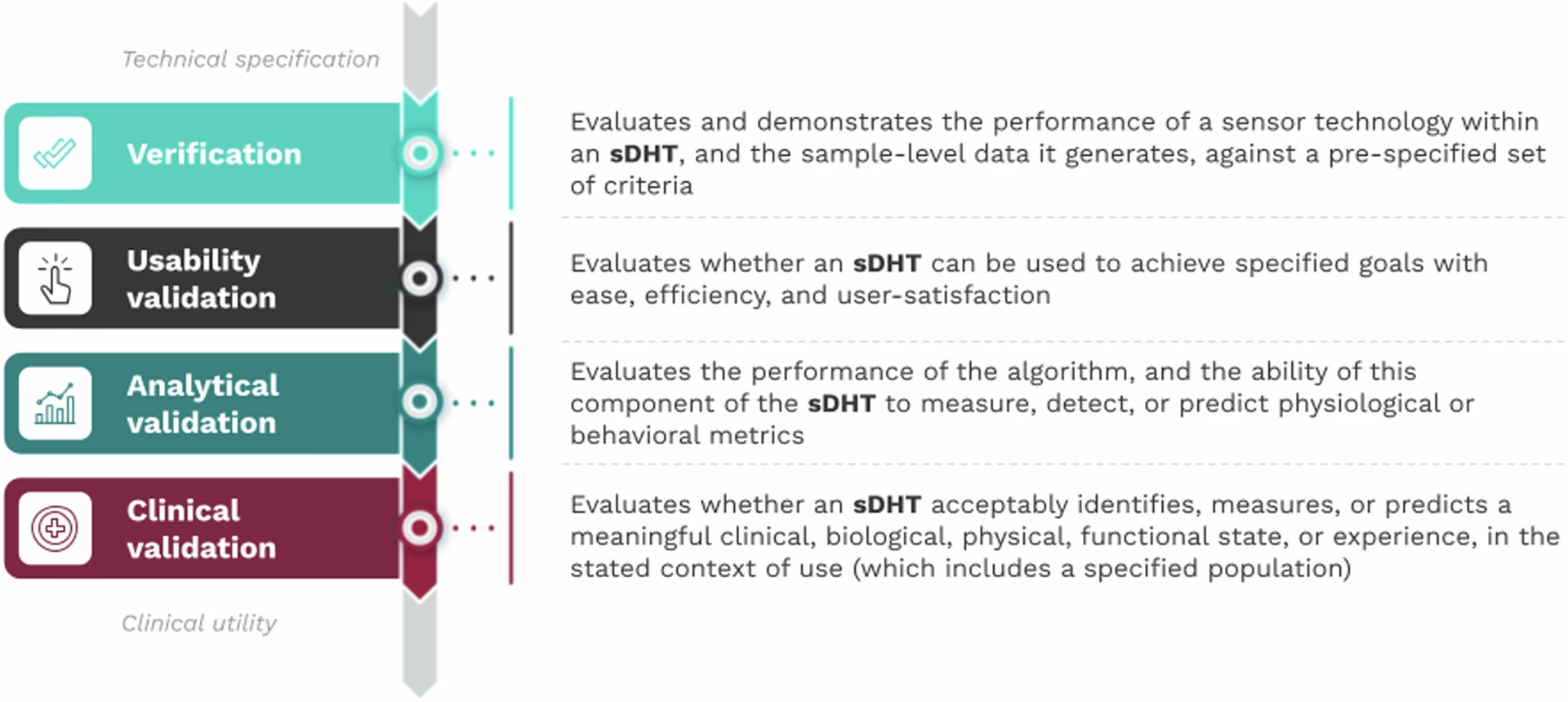
1. Installationskvalificering (IQ)
Den første fase, IQ, fokuserer på udstyret. Her dokumenteres det, at udstyret er modtaget som bestilt og er installeret korrekt i henhold til producentens anvisninger og designspecifikationer. Man verificerer ting som korrekte rørforbindelser, elektriske tilslutninger, softwareversioner og at alle nødvendige dokumenter og manualer er til stede.
2. Operationel Kvalificering (OQ)
I OQ-fasen testes det, om udstyret fungerer korrekt inden for de specificerede operationelle grænser. Dette indebærer ofte at køre udstyret uden produkt og teste 'worst-case' scenarier. Man tester alarmer, kontrolknapper, hastighedsindstillinger og andre kritiske driftsparametre for at bevise, at udstyret opfører sig som forventet under alle tænkelige driftsforhold.
3. Performance Kvalificering (PQ)
Den sidste og mest afgørende fase er PQ. Her køres processen under normale produktionsbetingelser med det faktiske produktmateriale for at demonstrere, at den konsekvent kan producere et produkt, der opfylder alle specifikationer. Typisk udføres tre succesfulde produktionskørsler for at bevise repeterbarhed og robusthed. Det er her, man samler de endelige data, der beviser, at processen er valideret og klar til kommerciel produktion.
Sammenligning af Valideringsfaser
| Fase | Formål | Typiske Spørgsmål |
|---|---|---|
| IQ (Installation) | Beviser, at udstyret er installeret korrekt. | Er alle dele leveret? Er det tilsluttet korrekt? Er softwaren den rigtige version? |
| OQ (Operationel) | Beviser, at udstyret fungerer som specificeret. | Virker alle knapper og alarmer? Kan udstyret køre ved min/max hastighed? |
| PQ (Performance) | Beviser, at processen konsekvent producerer et acceptabelt produkt. | Lever produktet op til specifikationerne over flere produktionskørsler? |
Holder sig Ajour med Industrien: "State of Validation"
Valideringsverdenen er ikke statisk. Nye teknologier, opdaterede regulatoriske krav og skiftende markedspåvirkninger betyder, at fagfolk konstant skal holde sig ajour. En interessant ressource i denne sammenhæng er rapporten 'State of Validation'. Denne årlige rapport, som er uafhængigt forfattet, analyserer praksis, fremskridt og faldgruber inden for valideringsindustrien globalt. Gennem kvantitative og kvalitative undersøgelser blandt valideringsprofessionelle giver den et øjebliksbillede af de kræfter, der former branchen. At følge med i sådanne analyser er afgørende for at forstå nye tendenser, såsom digitalisering af valideringsprocesser, og for at sikre, at ens egen organisations kvalitetssikring er på forkant med udviklingen.
Ofte Stillede Spørgsmål om Procesvalidering
- Hvad er forskellen på verifikation og validering?
- Verifikation bekræfter, at du har opfyldt specifikke krav (f.eks. måling af en komponents dimensioner). Validering bekræfter, at en proces konsekvent vil producere et produkt, der opfylder disse krav. Man verificerer et produkt; man validerer en proces.
- Gælder disse krav kun i USA?
- Nej. Mens 21 CFR Part 820 er specifik for USA, er principperne universelle. Den internationale standard for kvalitetsstyring for medicinsk udstyr, ISO 13485, som er afgørende for markedsadgang i Europa (under MDR) og mange andre regioner, har meget lignende krav til procesvalidering.
- Hvad sker der, hvis en proces ikke er valideret korrekt?
- Konsekvenserne kan være alvorlige og spænder fra advarselsbreve fra myndighederne og store bøder til tvungne tilbagekaldelser af produkter. I værste fald kan det føre til skade på patienter, hvilket kan have katastrofale menneskelige og økonomiske omkostninger for virksomheden.
- Skal software også valideres?
- Ja, absolut. Software, der anvendes som en del af produktionsprocessen eller som en del af selve kvalitetssystemet, skal valideres for sin tilsigtede anvendelse. Dette er et område med stigende fokus fra myndighedernes side.
Afslutningsvis er procesvalidering ikke en valgfri aktivitet eller en byrdefuld opgave, der skal overstås. Det er en integreret og vital del af fremstillingen af medicinsk udstyr, der direkte understøtter det endelige mål: at levere sikre og effektive produkter, der forbedrer og redder liv. En veludført validering er et bevis på en organisations engagement i kvalitet og patientsikkerhed.
Hvis du vil læse andre artikler, der ligner Procesvalidering for Medicinsk Udstyr: Hvorfor og Hvornår?, kan du besøge kategorien Sundhed.
