21/09/2013
Tuberkulose, en sygdom der for mange lyder som noget fra fortiden, er desværre stadig en af verdens mest dødelige infektionssygdomme. Bag denne sygdom står en formidabel modstander: en gruppe af nært beslægtede bakterier kendt som Mycobacterium tuberculosis-komplekset (MTBC). Dette er ikke blot én enkelt bakterie, men en hel familie af mikroorganismer, der har specialiseret sig i at inficere mennesker og dyr. At forstå dette kompleks er nøglen til at forstå sygdommen, den forårsager, og er afgørende for at udvikle nye, mere effektive metoder til diagnose og behandling. I denne artikel vil vi dykke ned i MTBC's biologi, udforske den komplicerede kamp mellem bakterien og vores immunforsvar, og se på fremtidens lovende teknologier, der kan ændre vores måde at bekæmpe tuberkulose på.
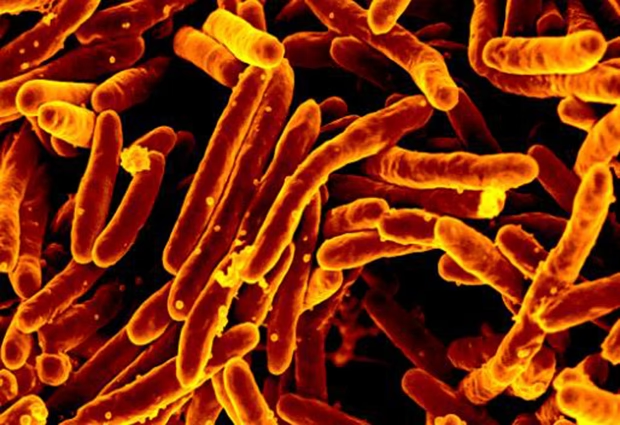
Hvad er Mycobacterium tuberculosis-komplekset?
Når vi taler om tuberkulose hos mennesker, er hovedårsagen næsten altid bakterien Mycobacterium tuberculosis. Men den er en del af en større familie, MTBC, som omfatter mindst ni forskellige, men genetisk meget ens, arter. Disse arter har udviklet sig fra en fælles forfader gennem tusinder af år, hvor små genetiske ændringer – som tilføjelser eller sletninger af DNA – har ført til, at de har specialiseret sig til at inficere forskellige værter. Andre kendte medlemmer af komplekset inkluderer:
- Mycobacterium bovis: Forårsager primært tuberkulose hos kvæg, men kan smitte til mennesker, typisk gennem indtagelse af upasteuriserede mælkeprodukter.
- Mycobacterium africanum: En væsentlig årsag til tuberkulose i visse dele af Vestafrika.
- Mycobacterium microti: Inficerer typisk gnavere, men kan i sjældne tilfælde inficere mennesker.
Selvom disse bakterier er genetisk meget ens, udviser de markante forskelle i, hvor aggressive de er (deres patogenicitet), og hvilke værter de foretrækker. Denne diversitet, trods den tætte genetiske lighed, gør studiet af MTBC både fascinerende og komplekst. Det er som at studere en familie, hvor alle medlemmer ligner hinanden, men har vidt forskellige personligheder og evner.
Sygdommens Udvikling: En Kompleks Dans Mellem Vært og Bakterie
Patogenesen – altså hvordan sygdommen udvikler sig – ved tuberkulose er utroligt kompleks og endnu ikke fuldt forstået. Det er en dynamisk proces, der involverer et konstant samspil mellem bakteriens overlevelsesstrategier og værtens immunforsvar. Processen starter typisk, når en person indånder små dråber i luften, der indeholder MTBC-bakterier fra en smittet persons hoste eller nys.
Immunforsvarets Første Reaktion og Dannelsen af Granulomer
Når bakterierne når lungerne, bliver de hurtigt mødt af kroppens første forsvarslinje: immunceller kaldet makrofager. Disse cellers opgave er at "spise" og ødelægge fremmede indtrængere. MTBC-bakterier har dog udviklet en uhyggelig evne til ikke blot at overleve inde i makrofagerne, men også at formere sig der. Dette gør makrofagen til et perfekt skjulested.
Som reaktion på denne vedvarende infektion samler immunforsvaret flere celler omkring de inficerede makrofager og danner en struktureret klump af immunceller. Denne struktur kaldes et granulom. I årtier har forskere debatteret granulomets rolle. Er det en succesfuld strategi fra immunforsvarets side for at indkapsle og kontrollere bakterierne, som en slags biologisk fængsel? Eller er det i virkeligheden en fordel for bakterien, der skaber et beskyttet miljø, hvor den kan ligge i dvale og overleve i årevis?
Svaret er sandsynligvis begge dele. I mange tilfælde lykkes det for granulomet at holde infektionen i skak, hvilket fører til en tilstand kendt som latent tuberkulose. Personen er smittet, men er ikke syg og kan ikke smitte andre. Bakterierne er dog ikke elimineret; de er blot i dvale. Hos omkring 5-10% af de smittede vil dette forsvar på et senere tidspunkt i livet bryde sammen – ofte på grund af et svækket immunforsvar – og bakterierne vil reaktivere og forårsage aktiv tuberkulose.
Udfordringer med Nuværende Diagnostik
En af de største udfordringer i den globale bekæmpelse af tuberkulose er utilstrækkelige diagnostiske værktøjer. De metoder, vi har i dag, har flere betydelige mangler, som forsinker behandlingen og bidrager til spredningen af sygdommen.
- Mikroskopi af opspyt: Den mest udbredte metode i ressourcefattige områder. Den er hurtig og billig, men den er ikke særlig følsom. En patient skal have et stort antal bakterier i sit opspyt, før de kan ses i et mikroskop, hvilket betyder, at mange smitsomme tilfælde overses.
- Dyrkning: Anses for at være guldstandarden. Her forsøger man at få bakterierne fra en prøve til at vokse i et laboratorium. Metoden er meget følsom, men den er ekstremt langsom. Det kan tage op til 6-8 uger at få et resultat, hvilket er kritisk lang tid for en alvorligt syg patient.
- Molekylære tests (f.eks. PCR): Disse tests leder efter bakteriens DNA og er meget hurtigere end dyrkning (timer i stedet for uger). De er dog dyre og kræver avanceret udstyr og uddannet personale, hvilket gør dem mindre tilgængelige i mange dele af verden.
Et centralt problem for alle metoder er at skelne mellem aktiv sygdom og latent infektion samt at overvåge, om en given behandling virker effektivt.
Fremtidens Værktøjer: "Omics" og Jagten på Biomarkører
For at overvinde de nuværende diagnostiske udfordringer har forskningen rettet blikket mod en ny og spændende tilgang: opdagelsen af biomarkører ved hjælp af "multi-omics"-teknologier. En biomarkør er et målbart tegn i kroppen – f.eks. et specifikt protein eller et genetisk molekyle i blodet – der kan fortælle os om en persons helbredstilstand. Målet er at finde en unik "signatur" i en patients blod, spyt eller urin, der med sikkerhed kan sige: "Denne person har aktiv tuberkulose."
"Multi-omics" er en holistisk tilgang, der kombinerer flere forskellige analysemetoder for at få et komplet billede af, hvad der sker i kroppen under en infektion. Dette inkluderer:
- Genomics: Analyse af både patientens og bakteriens samlede DNA.
- Transcriptomics: Analyse af RNA-molekyler, som viser, hvilke gener der er aktive.
- Proteomics: Analyse af alle de proteiner, der produceres.
- Metabolomics: Analyse af små molekyler (metabolitter), som er produkterne af kroppens stofskifte.
Ved at kombinere data fra disse felter kan forskere identificere komplekse mønstre, der er specifikke for tuberkulose. Potentialet er enormt. Fremtidige tests baseret på disse biomarkører kunne:
- Give en hurtig og tidlig diagnose: En simpel blodprøve kunne give svar på få timer.
- Skelne mellem latent og aktiv TB: Noget, som nuværende tests kæmper med.
- Overvåge behandlingseffekt: Ved at måle hvordan biomarkørerne ændrer sig, kan læger hurtigt se, om en patient reagerer på medicinen.
- Forudsige risiko: Identificere hvilke personer med latent TB, der har størst risiko for at udvikle aktiv sygdom, så man kan tilbyde forebyggende behandling.
Sammenligning af Diagnostiske Metoder
| Metode | Hastighed | Følsomhed | Information |
|---|---|---|---|
| Mikroskopi | Hurtig (timer) | Lav | Påviser syrefaste stave |
| Dyrkning | Meget langsom (uger) | Høj (guldstandard) | Bekræfter levende bakterier, muliggør resistenstest |
| Molekylære Tests | Hurtig (timer) | Høj | Påviser bakterielt DNA, kan teste for resistens |
| Biomarkør-tests (Fremtid) | Meget hurtig (timer) | Potentielt meget høj | Kan skelne sygdomsstadier, overvåge behandling |
Ofte Stillede Spørgsmål (FAQ)
Er tuberkulose stadig et problem i Danmark?
Ja, selvom det er sjældent sammenlignet med mange andre lande, diagnosticeres der stadig tilfælde af tuberkulose i Danmark hvert år, primært blandt ældre, socialt udsatte og personer fra lande med høj forekomst af TB. Overvågning og hurtig behandling er fortsat vigtigt for at forhindre spredning.
Hvad er forskellen på latent og aktiv tuberkulose?
Ved latent tuberkulose er personen smittet med bakterien, men immunforsvaret holder den under kontrol. Personen er ikke syg og smitter ikke. Ved aktiv tuberkulose er bakterierne aktive og formerer sig, hvilket fører til symptomer som langvarig hoste, feber, vægttab og nattesved. En person med aktiv lungetuberkulose kan smitte andre.
Hvordan smitter tuberkulose?
Tuberkulose smitter næsten udelukkende gennem luften, når en person med aktiv lungetuberkulose hoster, nyser, taler eller synger. For at blive smittet kræves det som regel, at man opholder sig i tæt kontakt med den smittede person over længere tid. Det smitter ikke ved almindeligt håndtryk eller ved at dele mad og drikke.
Konklusion
Mycobacterium tuberculosis-komplekset repræsenterer en af menneskehedens ældste og mest vedholdende fjender. Dets evne til at manipulere og undvige vores immunforsvar, kombineret med manglerne i vores nuværende diagnostiske værktøjer, gør kampen mod tuberkulose til en vedvarende global udfordring. Men forskningen står ikke stille. Fremkomsten af kraftfulde "multi-omics"-teknologier og den intensive jagt på pålidelige biomarkører giver et reelt håb. Ved at opnå en dybere, mere holistisk forståelse af det komplekse samspil mellem MTBC og den menneskelige krop, er vi på vej mod en fremtid, hvor hurtig og præcis diagnose kan redde utallige liv og endelig bringe os et skridt tættere på at udrydde denne sygdom.
Hvis du vil læse andre artikler, der ligner MTBC: Forstå den komplekse tuberkulosebakterie, kan du besøge kategorien Sundhed.