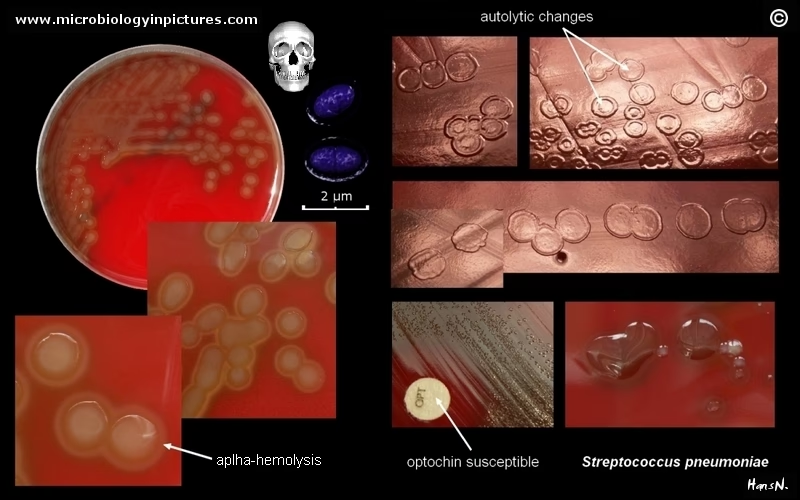
16/10/1999
Bakteriel lungebetændelse er en alvorlig infektion i de nedre luftveje, der bidrager markant til sygdomsbyrde og dødelighed på verdensplan. Den rammer mennesker i alle aldre og med forskellige risikoprofiler. For at forstå de komplekse interaktioner mellem den menneskelige krop og de sygdomsfremkaldende bakterier, samt for at teste effektiviteten og sikkerheden af nye lægemidler, er forskere afhængige af laboratoriemodeller. Traditionelt har man brugt simple todimensionelle cellekulturer og dyremodeller, men disse har deres begrænsninger. I de senere år er mere avancerede humane cellekulturmodeller kommet i fokus. Disse modeller bygger bro mellem de klassiske metoder og kan give en langt mere præcis efterligning af de forhold, der findes i en menneskelig lunge under en infektion.
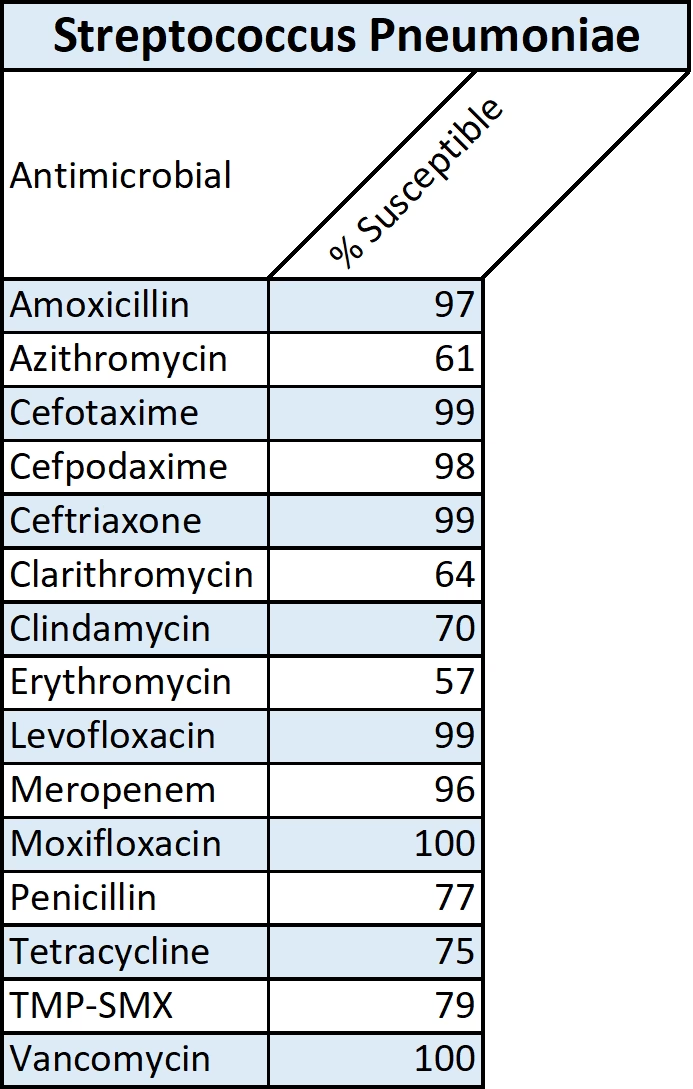
Hvorfor er avancerede modeller nødvendige?
Den menneskelige lunge er et utroligt komplekst organ. Den er ansvarlig for gasudveksling, men spiller også en afgørende rolle i immunsystemet, hvor den beskytter os mod skadelige partikler og patogener fra luften. At genskabe denne komplekse struktur og funktion i et laboratorium er en enorm udfordring. Traditionelle cellemodeller, hvor celler dyrkes i et enkelt lag på en plastikoverflade, mangler den tredimensionelle arkitektur og de interaktioner mellem forskellige celletyper, som findes i rigtigt lungevæv. Dyremodeller, oftest mus, har været et vigtigt redskab, men der er betydelige anatomiske og fysiologiske forskelle mellem muselunger og menneskelunger. Mange bakterier, der forårsager alvorlig sygdom hos mennesker, er ikke lige så skadelige for mus, hvilket gør det svært at oversætte resultater direkte. Derfor er der et stort behov for modeller, der bedre efterligner den menneskelige situation. Dette er også i tråd med det globale initiativ kendt som '3R-strategien' (Replace, Reduce, Refine), som sigter mod at erstatte, reducere og forfine brugen af dyr i videnskabelig forskning.
Forskellige Typer af Avancerede Lungeinfektionsmodeller
Forskningen har udviklet flere sofistikerede modeller, der hver især tilbyder unikke fordele i studiet af bakteriel lungebetændelse. De mest fremtrædende inkluderer Air-Liquid Interface (ALI) modeller, sfæroider, organoider og Lung-on-a-Chip systemer.
Air-Liquid Interface (ALI) Modeller
I ALI-modeller dyrkes lungeepitelceller på en porøs membran. Når cellerne har dannet et tæt lag, fjernes mediet fra den øverste side, så cellerne udsættes for luft, mens de stadig får næring fra mediet på undersiden. Denne metode skaber et mere fysiologisk relevant miljø, der efterligner luftvejene. Det tillader cellerne at differentiere sig og udvikle specialiserede funktioner, såsom produktion af slim og dannelse af cilier – de små fimrehår, der hjælper med at rense luftvejene. ALI-modeller er særligt velegnede til at studere, hvordan bakterier interagerer med luftvejens første forsvarslinje, herunder slimlaget og den mukociliære clearance.
Tredimensionelle Modeller: Sfæroider og Organoider
For at opnå endnu større kompleksitet er tredimensionelle (3D) modeller blevet udviklet. Selvom begreberne 'sfæroid' og 'organoid' ofte bruges i flæng, er der vigtige forskelle.
- Sfæroider: Disse er simple 3D-strukturer, der dannes, når celler samler sig i kugleformede aggregater. De mangler ofte den komplekse organisering og selvfornyende kapacitet, som findes i rigtige organer.
- Organoider: Disse er langt mere avancerede og kan beskrives som 'mini-organer' dyrket i laboratoriet. De udvikles fra stamceller (enten fra voksne patienter eller pluripotente stamceller) og kan selvorganisere sig til strukturer, der efterligner arkitekturen og funktionen af et rigtigt organ. Lunge-organoider kan indeholde flere forskellige celletyper, danne luftvejslignende lumen og endda udføre funktioner som produktion af surfaktant, et stof der er afgørende for alveolernes stabilitet.
Lung-on-a-Chip (LOC)
Den måske mest teknologisk avancerede model er Lung-on-a-Chip. Disse er mikrofluidiske enheder, typisk på størrelse med et USB-stik, der indeholder små kanaler foret med levende menneskelige celler. En typisk LOC-model består af to kanaler adskilt af en porøs membran. Den øverste kanal er foret med lungeepitelceller og udsættes for luft, mens den nederste kanal er foret med blodkarendotelceller og perfunderes med et medium, der simulerer blodgennemstrømning. Systemet kan endda udsættes for mekanisk stræk for at efterligne åndedrætsbevægelser. Dette skaber et dynamisk mikromiljø, der gør det muligt at studere komplekse processer som immuncellers reaktion på infektion, og hvordan bakterier krydser barrieren fra lungen til blodbanen.
Valget af Celler er Afgørende
Succesen af enhver model afhænger af de celler, der bruges. Forskere kan vælge mellem primære celler, der er isoleret direkte fra patientvæv, eller etablerede, udødeliggjorte cellelinjer.
Primære Celler vs. Cellelinjer
Primære celler bevarer de fysiologiske egenskaber fra det oprindelige væv og kan differentiere til et fuldt funktionelt pseudostratificeret epitel, der indeholder både cilierede celler, slimproducerende bægerceller og basale stamceller. Ulempen er, at der kan være stor variation mellem donorer, og cellerne har en begrænset levetid. Cellelinjer, derimod, er nemme at dyrke, reproducerbare og har en næsten ubegrænset levetid. Dog kan de have mistet nogle af de specialiserede funktioner fra det oprindelige væv, hvilket kan kompromittere modellens realisme.
| Egenskab | Primære Celler | Etablerede Cellelinjer |
|---|---|---|
| Fysiologisk Relevans | Høj (efterligner tæt det oprindelige væv) | Variabel (kan have mistet funktioner) |
| Reproducerbarhed | Lav (stor donor-til-donor variation) | Høj (stabil fænotype over tid) |
| Levetid i Kultur | Begrænset (få passager) | Næsten ubegrænset (udødeliggjort) |
| Tilgængelighed | Kræver vævsdonation, kan være dyrt | Let tilgængelige fra cellebanker, billigere |
Udfordringer ved at Simulere en Bakteriel Infektion
Når cellemodellen er etableret, er næste skridt at introducere bakterier for at simulere en infektion. Dette er dog ikke så ligetil, som det lyder. Der er stor variation i de metoder, forskere bruger, hvilket gør det svært at sammenligne resultater på tværs af studier. To kritiske parametre er infektionsvarighed og den infektiøse dosis.
- Infektionsvarighed: De fleste studier fokuserer på akutte infektioner, hvor interaktioner observeres inden for 24 timer. Dette er nyttigt til at studere de tidlige faser af en infektion, såsom bakteriel vedhæftning og den indledende immunrespons. Kroniske infektioner, som er relevante for sygdomme som cystisk fibrose, er meget sværere at modellere, da det kræver en balance, hvor både celler og bakterier kan overleve i længere tid.
- Infektiøs dosis: Den mængde bakterier, der tilføjes, er afgørende. Dette måles ofte som MOI (Multiplicity of Infection), som er forholdet mellem antallet af bakterier og antallet af værtsceller. En for lav dosis giver måske ingen infektion, mens en for høj dosis hurtigt kan dræbe alle cellerne i modellen og ødelægge eksperimentet. Forskellige bakterier er også meget forskellige i deres evne til at forårsage celleskade. For eksempel er Pseudomonas aeruginosa kendt for at være meget cytotoksisk, hvilket kræver nøje optimering af MOI.
Analyse og Validering af Modellerne
For at vurdere, hvordan en infektion påvirker modellen, bruger forskere en række analysemetoder. Nogle metoder er ikke-destruktive og kan udføres i realtid, mens andre kræver, at modellen afsluttes.
En vigtig ikke-destruktiv måling for ALI- og LOC-modeller er TEER (Transepithelial Elektrisk Modstand). Dette er en måling af, hvor tæt cellebarrieren er. Et fald i TEER indikerer, at bakterierne har beskadiget barrieren. Andre metoder inkluderer live-celle mikroskopi for at observere interaktioner i realtid og måling af ciliebevægelsesfrekvens (Ciliary Beat Frequency, CBF). Efter eksperimentet kan destruktive metoder anvendes. Dette kan omfatte elektronmikroskopi for at se detaljerede billeder af celleskader, eller analyse af cellerne for gen- og proteinudtryk for at forstå, hvordan cellerne reagerer på infektionen. Antallet af levende bakterier, både dem der sidder fast på cellerne og dem der er trængt ind i dem, kan kvantificeres ved hjælp af traditionelle dyrkningsmetoder.
En stor udfordring for feltet er manglen på standardiserede protokoller og validering. Forskellige laboratorier bruger forskellige metoder, celler og infektionsparametre, hvilket gør det svært at opnå reproducerbare resultater. En større gennemsigtighed og deling af detaljerede, validerede protokoller er afgørende for at fremme brugen af disse kraftfulde modeller.
Ofte Stillede Spørgsmål
Hvad er en 'organoid'?
En organoid er en tredimensionel cellestruktur, der dyrkes fra stamceller i et laboratorium. Den efterligner arkitekturen og funktionen af et rigtigt organ i en miniaturiseret form. Lungeorganoider kan for eksempel udvikle luftvejslignende strukturer og indeholde flere af de celletyper, der findes i en menneskelig lunge.
Hvorfor kan vi ikke bare bruge dyremodeller til at studere lungebetændelse?
Dyremodeller, især mus, har været nyttige, men der er betydelige biologiske forskelle mellem dyr og mennesker. Lungernes anatomi, immunsystemet og modtageligheden over for specifikke bakterier kan variere meget. Dette betyder, at resultater fra dyreforsøg ikke altid kan oversættes direkte til mennesker. Avancerede humane cellemodeller kan overvinde nogle af disse begrænsninger.
Er disse avancerede modeller klar til at erstatte dyreforsøg fuldstændigt?
Ikke endnu. Selvom modellerne er meget avancerede, mangler de stadig vigtige elementer af en levende organisme, såsom et komplet og funktionelt immunsystem og interaktioner mellem forskellige organer. I øjeblikket bruges de ofte som et supplement til dyreforsøg, med det langsigtede mål at reducere og potentielt erstatte brugen af dyr i forskningen.
Hvad er den største udfordring ved at bruge disse modeller?
Den største udfordring er kompleksiteten og manglen på standardisering. Det kan være dyrt, tidskrævende og teknisk svært at etablere og vedligeholde disse modeller. Variation i celler, materialer og protokoller mellem laboratorier gør det også svært at opnå reproducerbare resultater, hvilket er afgørende for videnskabelig validitet.
Hvis du vil læse andre artikler, der ligner Avancerede modeller for lungebetændelse, kan du besøge kategorien Sundhed.