14/04/2010
- En Dybdegående Gennemgang af Ziehl-Neelsen Farvning
- Historien og Princippet bag Syrefast Farvning
- Trin-for-Trin Guide til Ziehl-Neelsen Procedure
- Fortolkning og Rapportering af Resultater
- Fordele, Ulemper og Moderne Alternativer
- Modificeret ZN-Farvning: En Lovende Udvikling
- Ofte Stillede Spørgsmål (FAQ)
- Konklusion
En Dybdegående Gennemgang af Ziehl-Neelsen Farvning
I over 120 år har diagnosen af aktiv tuberkulose i store dele af verden været afhængig af en fundamental, men utrolig robust mikroskopisk test: Ziehl-Neelsen (ZN) farvningen. Selvom moderne diagnostiske metoder vinder frem, forbliver denne teknik, udviklet af de tyske læger Franz Ziehl og Friedrich Neelsen i 1882, en hjørnesten i globale tuberkulosekontrolprogrammer. Dens evne til at identificere de mest smitsomme former for sygdommen hurtigt og billigt gør den uundværlig, især i ressourcebegrænsede områder. Denne artikel dykker ned i principperne bag ZN-farvning, dens procedure, fortolkning, begrænsninger og de moderne tilpasninger, der fortsat holder denne klassiske metode relevant i kampen mod Mycobacterium tuberculosis.
Historien og Princippet bag Syrefast Farvning
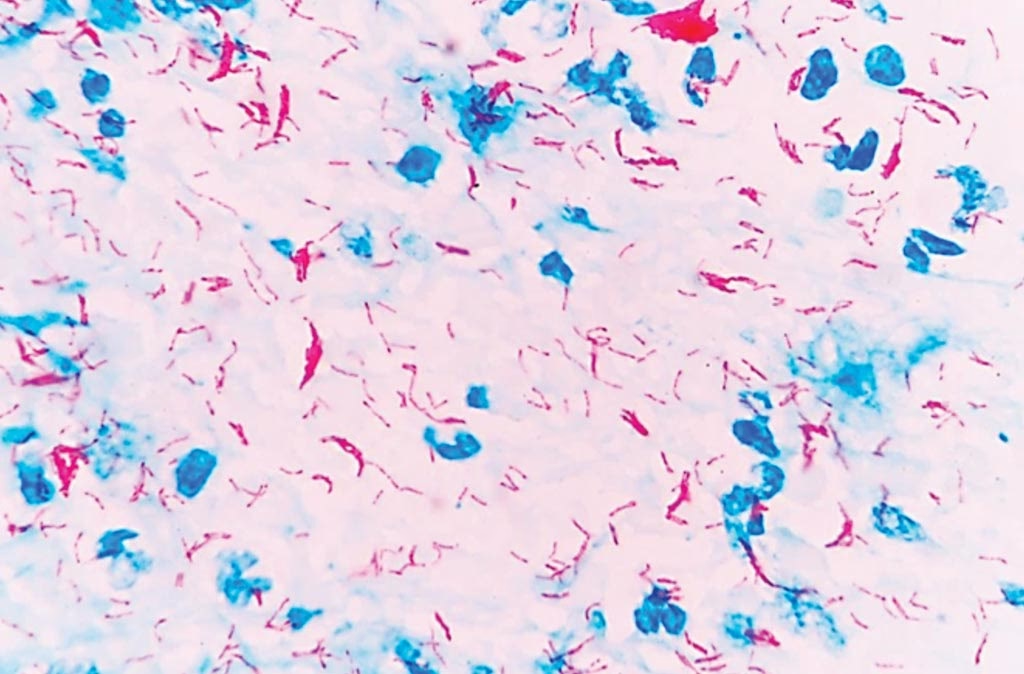
Fundamentet for ZN-farvningen blev lagt af Paul Ehrlich i 1882, da han først opdagede de unikke 'syre-alkoholfaste' egenskaber ved tuberkulosebacillen. Denne egenskab betyder, at bakterien, når den først er farvet, modstår affarvning med en syre-alkohol-opløsning. Det var dog Ziehl og Neelsen, der forfinede metoden til den form, vi kender i dag. Neelsen introducerede brugen af det primære farvestof, carbolfuchsin, og opdagede, at opvarmning af præparatet forbedrede farvestoffets evne til at trænge igennem bakteriens voksagtige cellevæg. Han tilføjede også en kontrastfarve, methylenblåt, for at farve baggrunden og andre ikke-syrefaste celler blå, hvilket fik de røde tuberkulosebaciller til at fremstå klart og tydeligt.
Hemmeligheden bag denne syrefaste egenskab ligger i den komplekse struktur af mykobakteriernes cellevæg. Den er rig på lipider, især mykolsyre, som danner en voksagtig, uigennemtrængelig barriere. Denne barriere gør det svært for almindelige farvestoffer at trænge ind, men når carbolfuchsin opvarmes, kan det penetrere cellevæggen. Når præparatet afkøles, fanges carbolfuchsinet inde i cellen. Den efterfølgende behandling med en stærk affarvningsmiddel (typisk en blanding af syre og alkohol) fjerner farvestoffet fra alle andre celler og materiale på objektglasset, men mykobakteriernes voksagtige væg holder fast på den røde farve. Til sidst farves de affarvede elementer blå med kontrastfarven, hvilket skaber den karakteristiske visuelle kontrast.

Trin-for-Trin Guide til Ziehl-Neelsen Procedure
Udførelsen af en ZN-farvning kræver præcision og omhyggelighed for at sikre pålidelige resultater. Processen kan opdeles i følgende trin:
- Præparation af udstrygning: En prøve, typisk opspyt (sputum) fra patienten, smøres tyndt ud på et rent, fedtfrit objektglas. Prøven lufttørres derefter helt.
- Varmefiksering: Objektglasset føres hurtigt gennem en flamme et par gange for at fiksere cellerne til glasset, hvilket forhindrer dem i at blive vasket af under farvningsprocessen.
- Primær farvning: Hele objektglasset dækkes med carbolfuchsin. Glasset opvarmes forsigtigt nedefra, indtil der stiger damp op fra farvestoffet. Det er afgørende, at farvestoffet ikke koger. Varmen opretholdes i cirka 5 minutter for at sikre, at farven trænger ind i bacillerne.
- Skylning: Efter opvarmning afkøles objektglasset, og overskydende farvestof skylles forsigtigt af med vand.
- Affarvning: Objektglasset dækkes med en affarvningsopløsning (f.eks. 20% svovlsyre eller 3% syre-alkohol) i et par minutter, indtil udstrygningen fremstår svagt lyserød. Dette trin fjerner carbolfuchsin fra alt andet end de syrefaste baciller.
- Skylning: Affarvningsmidlet skylles grundigt af med vand.
- Kontrastfarvning: Objektglasset dækkes med en kontrastfarve, som regel methylenblåt, og efterlades i 1-2 minutter. Dette farver baggrunden, humane celler og andre bakterier blå.
- Endelig skylning og tørring: Objektglasset skylles en sidste gang med vand og lufttørres.
- Mikroskopi: Præparatet undersøges under et mikroskop med olieimmersion ved 1000x forstørrelse for at identificere de røde, stavformede syrefaste baciller mod den blå baggrund.
Fortolkning og Rapportering af Resultater
En korrekt fortolkning af ZN-farvningen er afgørende for diagnosen. Syrefaste baciller (AFB) vil fremstå som lyserøde til røde stave, ofte let bøjede og kan ligge enkeltvis eller i små klynger. Alt andet på objektglasset vil være farvet blåt. For at standardisere rapporteringen anvendes ofte en skala fastsat af organisationer som WHO. Nedenstående tabel viser et eksempel på en sådan rapporteringsguide.
| Antal syrefaste baciller (AFB) observeret | Rapportering | Grad |
|---|---|---|
| Ingen AFB set i 100 synsfelter | Negativ | 0 |
| 1-9 AFB pr. 100 synsfelter | Rapporter det præcise antal | sparsom |
| 10-99 AFB pr. 100 synsfelter | Positiv | 1+ |
| 1-10 AFB pr. synsfelt (i mindst 50 felter) | Positiv | 2+ |
| >10 AFB pr. synsfelt (i mindst 20 felter) | Positiv | 3+ |
Fordele, Ulemper og Moderne Alternativer
Trods sin alder har ZN-farvningen flere klare fordele, der sikrer dens fortsatte brug. Den er hurtig, billig og kræver relativt simpelt udstyr, hvilket gør den ideel til laboratorier med begrænsede ressourcer. En positiv test har desuden en høj prædiktiv værdi for tuberkulose, især i områder med høj forekomst af sygdommen.

Metoden har dog også betydelige begrænsninger. Den primære ulempe er dens lave følsomhed, som ligger på omkring 50-60%. Det kræver en relativt høj koncentration af bakterier i prøven (mindst 10.000 baciller pr. milliliter sputum) for at opnå et positivt resultat. Derfor kan en negativ test ikke udelukke tuberkulose, og det anbefales ofte at undersøge mindst tre separate prøver. Ydermere kan ZN-farvning ikke skelne mellem forskellige arter af Mycobacterium eller mellem levende og døde baciller, hvilket gør den uegnet til at monitorere behandlingseffekt.
Alternativer og Forbedringer
For at imødekomme disse begrænsninger er der udviklet flere alternative metoder:
- Fluorescensmikroskopi: Ved brug af farvestoffer som auramin-rhodamin lyser bacillerne op under UV-lys. Dette gør dem lettere at se, og screeningen af objektglas kan ske hurtigere ved lavere forstørrelse. Metoden er mere følsom end ZN, men kræver et fluorescensmikroskop og kan give falsk-positive resultater fra fluorescerende snavs.
- Dyrkning: Dyrkning af mykobakterier er den gyldne standard for diagnose. Det bekræfter tilstedeværelsen af levende bakterier og muliggør artsidentifikation og resistensbestemmelse. De mest anvendte medier er æg-baserede som Löwenstein-Jensen. Ulempen er, at M. tuberculosis er en langsomt voksende bakterie, og det kan tage 4-8 uger at få et resultat.
- Molekylære metoder: Teknikker som PCR (Polymerase Chain Reaction) kan påvise bakteriens DNA direkte i en prøve. Disse tests er meget hurtige (resultater på få timer) og yderst følsomme, men de er også dyrere og kræver avanceret udstyr.
- Maskinlæring (AI): Nyere forskning fokuserer på at bruge kunstig intelligens til automatisk at analysere digitale billeder af ZN-farvede præparater. Dette kan potentielt øge nøjagtigheden, reducere den subjektive faktor og aflaste travle laboratorieteknikere.
Modificeret ZN-Farvning: En Lovende Udvikling
En spændende ny udvikling er en modificeret ZN-farvningsmetode, specielt designet til prøver med meget få bakterier, såsom cerebrospinalvæske (CSF) fra patienter med tuberkuløs meningitis. Denne metode kombinerer cytospin-centrifugering for at koncentrere celler og baciller på et lille område af objektglasset med brugen af et rengøringsmiddel (Triton X-100) i farvestofferne. Triton X-100 øger permeabiliteten af både humane cellemembraner og mykobakteriernes cellevæg, hvilket forbedrer farveoptagelsen markant. Resultater har vist, at denne modificerede teknik kan øge detektionsraten dramatisk og endda gøre det muligt at se intracellulære baciller inde i immunceller som neutrofiler og monocytter, hvilket er næsten umuligt med den konventionelle metode.

Ofte Stillede Spørgsmål (FAQ)
- Hvorfor kaldes det en "syrefast" farvning?
- Navnet stammer fra bakteriens evne til at modstå affarvning med en stærk syre-alkohol-opløsning, efter den er blevet farvet med carbolfuchsin. Denne modstandsdygtighed skyldes det høje indhold af mykolsyre i cellevæggen.
- Kan Ziehl-Neelsen farvning bruges til andre sygdomme end tuberkulose?
- Ja. Metoden kan påvise andre medlemmer af Mycobacterium-slægten, såsom M. leprae (årsag til spedalskhed), samt andre syrefaste organismer som bakterieslægten Nocardia og visse parasitter (f.eks. Cryptosporidium oocyster).
- Er en negativ ZN-farvning nok til at udelukke tuberkulose?
- Nej, absolut ikke. På grund af metodens lave følsomhed kan en patient stadig have aktiv tuberkulose, selv med flere negative sputumprøver. Hvis der er stærk klinisk mistanke, skal der altid suppleres med andre tests som dyrkning eller PCR.
- Hvad er forskellen på "varm" og "kold" ZN-farvning?
- Den klassiske ("varme") Ziehl-Neelsen metode kræver opvarmning for at få farvestoffet til at trænge ind i cellevæggen. En modificeret version, kendt som Kinyoun-metoden ("kold" farvning), bruger en højere koncentration af phenol i carbolfuchsin-opløsningen, hvilket eliminerer behovet for opvarmning. Dette kan være en fordel i felten eller i laboratorier uden adgang til en varmekilde.
Konklusion
Ziehl-Neelsen farvningen er et vidnesbyrd om genialiteten i tidlig mikrobiologi. På trods af fremkomsten af højteknologiske diagnostiske værktøjer, forbliver denne mere end et århundrede gamle teknik en uundværlig del af den globale indsats mod tuberkulose. Dens enkelhed, hurtighed og lave omkostninger sikrer, at diagnostik er tilgængelig, hvor der er mest brug for den. Selvom dens begrænsninger, især den lave følsomhed, er velkendte, fortsætter den med at tjene som et afgørende første skridt i diagnosen af de mest smitsomme patienter. Med innovative modifikationer og i samspil med moderne teknologier som AI og molekylærbiologi, vil arven fra Ziehl og Neelsen utvivlsomt fortsætte med at spille en vigtig rolle i folkesundheden i mange år fremover.
Hvis du vil læse andre artikler, der ligner Ziehl-Neelsen Farvning: Nøglen til TB-Diagnose, kan du besøge kategorien Sundhed.
