24/12/2010
Inden for moderne bioteknologi og medicinsk forskning er evnen til at producere specifikke proteiner i store mængder afgørende. Fra insulin til vacciner og industrielle enzymer er rekombinant proteinproduktion en hjørnesten. Et af de mest kraftfulde og udbredte værktøjer til dette formål er T7-ekspressionssystemet, som anvendes i bakterien Escherichia coli (E. coli). Dette system er kendt for sin utrolige effektivitet, men dets succes afhænger af en meget præcis kontrolmekanisme. Uden denne kontrol kan systemet blive utæt, hvilket fører til uønsket proteinproduktion med potentielt skadelige konsekvenser for værtscellen. Denne artikel dykker ned i, hvordan T7-systemet kontrolleres af Lac-repressoren, og udforsker en overraskende årsag til, hvorfor denne kontrol nogle gange svigter: de skjulte ingredienser i bakteriens vækstmedium.
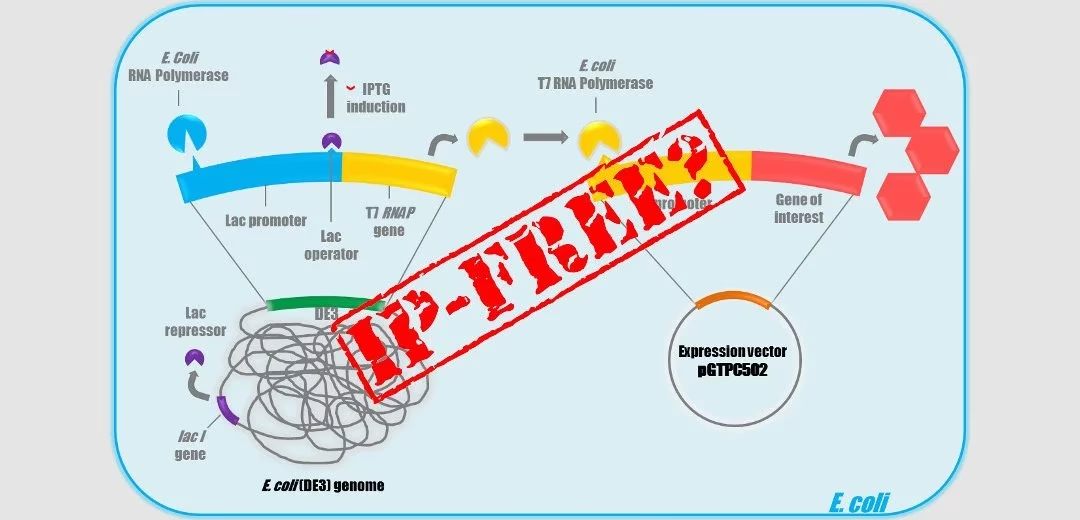
Hvordan fungerer T7-ekspressionssystemet?
For at forstå problemet med lækage er det vigtigt først at forstå, hvordan T7-systemet er designet til at fungere. Systemet er en genial ingeniørbedrift, der kombinerer elementer fra en virus (bakteriofag T7) og bakteriens egen genreguleringsmaskineri. Det består af flere nøglekomponenter:
- Ekspressionsvektoren (pET-vektor): Dette er et lille, cirkulært stykke DNA (et plasmid), der indsættes i E. coli. Vektoren indeholder to vigtige elementer: T7-promotoren og genet af interesse, som er det gen, vi ønsker at udtrykke for at producere et specifikt protein. T7-promotoren fungerer som et startsignal, men kun for et bestemt enzym.
- T7 RNA Polymerase: Dette er det specielle enzym, der genkender T7-promotoren og starter transkriptionen (aflæsningen) af genet af interesse. I modsætning til E. colis egen RNA-polymerase er T7 RNA-polymerasen ekstremt hurtig og effektiv, hvilket resulterer i en massiv produktion af det ønskede protein. Genet, der koder for T7 RNA-polymerasen, er ikke på plasmidet, men er integreret direkte i E. colis kromosom.
- Lac-operatorkontrollen: Her ligger nøglen til systemets tænd/sluk-kontakt. Produktionen af T7 RNA-polymerase er under kontrol af en lac-promotor. Denne promotor er normalt blokeret af et protein kaldet Lac-repressor (LacI). Så længe Lac-repressoren er bundet til DNA'et, kan T7 RNA-polymerase ikke produceres, og dermed kan vores gen af interesse heller ikke udtrykkes.
Processen for at tænde for systemet er som følger:
- En kemisk inducer, typisk IPTG (Isopropyl β-D-1-thiogalactopyranosid), tilsættes til bakteriekulturen.
- IPTG binder sig til Lac-repressorproteinet. Denne binding ændrer repressorens form, så den ikke længere kan binde sig til DNA'et.
- Når repressoren er fjernet, kan E. colis egen RNA-polymerase transkribere genet for T7 RNA-polymerase.
- Den nyproducerede T7 RNA-polymerase finder T7-promotoren på ekspressionsvektoren.
- En eksplosiv transkription af genet af interesse begynder, og cellen omdannes til en lille proteinfabrik.
Problemet med "Lækage": Utilsigtet Proteindannelse
I en ideel verden ville T7-systemet være fuldstændig slukket, indtil IPTG tilsættes. Men i virkeligheden er der ofte en lille mængde basal ekspression, et fænomen kendt som "lækage". Dette betyder, at selv uden en inducer produceres der en lille smule T7 RNA-polymerase, hvilket fører til en lav, men konstant produktion af det rekombinante protein. For mange proteiner er dette ikke et problem. Men hvis det protein, man ønsker at producere, er toksiske for E. coli, kan selv en lille lækage have katastrofale følger. Konsekvenserne kan omfatte:
- Langsommere vækst: Cellen bruger energi på at producere et unødvendigt og potentielt skadeligt protein, hvilket hæmmer dens vækstrate.
- Celledød (lysis): Hvis proteinet er meget giftigt, kan det dræbe cellen, hvilket fører til en lav celledensitet og et dårligt udbytte.
- Akkumulering af mutanter: Celler, der tilfældigvis får en mutation, som deaktiverer produktionen af det giftige protein, vil have en overlevelsesfordel og vil hurtigt udkonkurrere de producerende celler.
- Tab af plasmid: Celler kan simpelthen smide ekspressionsvektoren ud for at overleve, hvilket resulterer i en kultur uden det ønskede gen.
At opretholde en stram kontrol over ekspressionen er derfor afgørende for succes, især ved produktion af udfordrende proteiner.
En Overraskende Kilde til Lækage: Vækstmediets Komponenter
Forskere observerede, at selv under identiske forhold opførte E. coli-kulturer sig nogle gange forskelligt. Nogle kulturer viste tegn på lækage, mens andre var tæt kontrollerede. Efter nøje undersøgelse viste synderen sig at være en uventet faktor: sammensætningen af vækstmediet, specifikt typen af pepton, der blev brugt. Peptoner er en blanding af aminosyrer og små peptider, der fungerer som en rig næringskilde for bakterier.
I et afgørende eksperiment blev et gen for Grønt Fluorescerende Protein (GFPuv) brugt som reporter. Da GFPuv produceres, lyser bakteriekolonierne grønt under UV-lys, hvilket gør det let at visualisere genekspression. Resultaterne var slående:
- Når bakterierne voksede på et medium indeholdende sojapepton, lyste kolonierne kraftigt grønt, selvom der ikke var tilsat IPTG. Dette indikerede en massiv lækage.
- En lignende, men svagere, effekt blev set med maltekstrakt.
- Når bakterierne derimod voksede på medier med peptoner af animalsk oprindelse (f.eks. tryptone, kaseinpepton, gelatinepepton), var der ingen eller meget lidt fluorescens. Systemet var tæt reguleret.
Dette pegede klart på, at noget i de plantebaserede peptoner fungerede som en uønsket inducer af T7-systemet.
Hvorfor forårsager Sojapepton Lækage? De molekylære syndere
Forskellen mellem animalske og plantebaserede peptoner ligger i deres kemiske sammensætning ud over aminosyrer. Mens animalske peptoner primært består af protein-nedbrydningsprodukter, indeholder plantemateriale som sojabønner også betydelige mængder kulhydrater.
Yderligere analyser afslørede, at de specifikke sukkerarter i sojapepton, der var ansvarlige for lækagen, var raffinose og stachyose. For at forstå, hvorfor disse sukkerarter kan aktivere systemet, må vi se på den naturlige funktion af Lac-repressor. I naturen regulerer Lac-repressoren bakteriens evne til at nedbryde laktose (mælkesukker). Den naturlige inducer, der fjerner repressoren, er allolaktose, et biprodukt af laktosemetabolismen. Allolaktose tilhører en kemisk gruppe kaldet β-D-galactosider.
Det viser sig, at både raffinose og stachyose også er β-D-galactosider. Deres molekylære struktur er tilstrækkeligt lig den for allolaktose og IPTG til, at de kan binde sig til Lac-repressoren og få den til at slippe sit greb om DNA'et. Når sojapepton, rigt på raffinose og stachyose, er til stede i mediet, fungerer disse sukkerarter som en utilsigtet, konstant inducer, der tænder for produktionen af T7 RNA-polymerase og dermed forårsager lækage.

Praktiske Konsekvenser og Anbefalinger
Denne opdagelse har vigtige praktiske implikationer for alle, der arbejder med T7-ekspressionssystemet. Valget af mediekomponenter er ikke trivielt og kan være forskellen mellem succes og fiasko. Nedenstående tabel opsummerer effekterne af forskellige komponenter.
| Mediekomponent | Effekt på T7-lac systemet | Anbefalet brug |
|---|---|---|
| Sojapepton | Stærk induktion (lækage) på grund af indhold af raffinose og stachyose. | Undgå ved ekspression af toksiske proteiner. Kan overvejes som et billigt alternativ til IPTG for ikke-toksiske proteiner. |
| Maltekstrakt | Moderat induktion (lækage). | Bør generelt undgås, hvis stram kontrol er påkrævet. |
| Trypton / Kaseinpepton (animalsk) | Ingen eller meget lav lækage. Giver stram regulering. | Ideel til ekspression af toksiske proteiner og når præcis kontrol er nødvendig. |
| IPTG | Meget stærk, kontrolleret og specifik inducer. | Standardinduceren til at starte ekspression på et bestemt tidspunkt. |
Anbefalinger til forskeren:
- Test dine medier: Før du starter en stor produktion, er det klogt at udføre små pilotforsøg med forskellige mediekompositioner for at tjekke for lækage.
- Vælg pepton med omhu: Hvis du arbejder med et potentielt toksisk protein, bør du som standard vælge peptoner af animalsk oprindelse for at sikre den strammest mulige kontrol.
- Overvej alternative kontrolmekanismer: Hvis lækage fortsat er et problem, kan systemet strammes yderligere ved f.eks. at få cellerne til at co-udtrykke T7-lysozym, som er en naturlig hæmmer af T7 RNA-polymerase, eller ved at bruge stammer, der producerer ekstra Lac-repressor.
Ofte Stillede Spørgsmål (FAQ)
Hvad er T7-ekspressionssystemet?
Det er et molekylærbiologisk system, der bruges i E. coli til at producere store mængder af et specifikt protein. Det udnytter den høje effektivitet af T7 RNA-polymerase fra en bakteriofag til at transkribere et ønsket gen, der er placeret bag en T7-promotor.
Hvorfor er "lækage" et problem i genekspression?
Lækage er uønsket, basal produktion af et protein, selv når systemet skulle være slukket. Dette er især problematisk, hvis proteinet er giftigt for værtscellen, da det kan føre til dårlig vækst, celledød og generel ustabilitet i kulturen, hvilket resulterer i et lavt udbytte.
Kan jeg bruge sojapepton i stedet for IPTG?
For ikke-toksiske proteiner kan sojapepton potentielt fungere som et omkostningseffektivt alternativ til IPTG, da det inducerer ekspression markant. Det giver dog ikke den samme præcise tidsmæssige kontrol som IPTG, og induktionsniveauet kan variere mellem forskellige partier af pepton. Det frarådes kraftigt til toksiske proteiner.
Er alle plantebaserede peptoner problematiske?
Det er sandsynligt, at andre plantebaserede peptoner (fra ærter, ris, kartofler osv.) også kan forårsage lækage, da de ofte indeholder komplekse kulhydrater. Effekten vil dog variere afhængigt af plantens art og forarbejdningsteknologien. Derfor anbefales det altid at teste mediet i lille skala, før man skalerer op.
Sammenfattende er T7-ekspressionssystemet et utroligt kraftfuldt værktøj, men dets effektivitet er dybt afhængig af omhyggelig kontrol. Opdagelsen af, at simple mediekomponenter som sojapepton kan underminere denne kontrol ved at fungere som skjulte inducere, understreger vigtigheden af at forstå alle aspekter af sit eksperimentelle setup. Ved at vælge de rigtige næringsstoffer og være opmærksom på potentielle faldgruber kan forskere sikre en mere robust, forudsigelig og succesfuld produktion af rekombinante proteiner.
Hvis du vil læse andre artikler, der ligner T7-promotor: Kontrol og utilsigtet lækage, kan du besøge kategorien Sundhed.
