31/03/2019
- Fremtiden for Kræftbehandling: En Dybdegående Gennemgang af Datadrevne Værktøjer
- OncoPredict R: Forfinelse af Jagten på Biomarkører
- CancerDR: Et Digitalt Bibliotek over Kræftens Svagheder
- Fra Laboratorie til Klinik: En Patients Hypotetiske Rejse
- Sammenligning af Tilgange: Traditionel vs. Personlig Behandling
- Ofte Stillede Spørgsmål (FAQ)
- Konklusion: Et Paradigmeskifte i Onkologi
Fremtiden for Kræftbehandling: En Dybdegående Gennemgang af Datadrevne Værktøjer
I årtier har kræftbehandling ofte fulgt en "one-size-fits-all" tilgang, hvor patienter med samme kræfttype modtager den samme standardbehandling, såsom kemoterapi. Selvom denne metode har reddet utallige liv, reagerer patienter meget forskelligt. Nogle oplever fremragende resultater, mens andre ser ringe effekt og lider under alvorlige bivirkninger. Årsagen til denne variation ligger dybt i vores gener. Hver kræftsvulst er unik, med sit eget sæt af genetiske mutationer, der driver dens vækst. I dag står vi over for en revolution inden for onkologi, drevet af vores evne til at afkode disse genetiske forskelle. Velkommen til æraen for personlig medicin, hvor behandlingen skræddersys til den enkelte patients unikke genetiske profil. To centrale brikker i dette komplekse puslespil er avancerede analytiske metoder som OncoPredict R og omfattende databaser som CancerDR, der tilsammen former fremtiden for kræftbehandling.
OncoPredict R: Forfinelse af Jagten på Biomarkører
For at kunne praktisere personlig medicin er forskere og læger afhængige af såkaldte biomarkører. En biomarkør er et målbart tegn – for eksempel en specifik genmutation – der kan forudsige, hvordan en patient vil reagere på en bestemt behandling. At finde pålidelige biomarkører er som at finde en nål i en høstak. Det kræver analyse af enorme mængder data, der forbinder tusindvis af gener med hundredvis af lægemidler på tværs af utallige kræftcellelinjer. Et af de største projekter på dette område er GDSC (Genomics of Drug Sensitivity in Cancer), som har skabt et gigantisk datasæt til netop dette formål.
Men disse data er ikke uden støj. En af de store udfordringer er et fænomen kendt som GLDS (Gene-Level Drug Sensitivity), som kan forstyrre resultaterne. Man kan forestille sig det som baggrundsstøj i en telefonsamtale, der gør det svært at høre, hvad der reelt bliver sagt. GLDS repræsenterer en generel følsomhed, som et gen måtte have over for et lægemiddel, uafhængigt af de specifikke mutationer, man leder efter. Denne baggrundsstøj kan skjule ægte sammenhænge mellem en mutation og et lægemiddels effektivitet, eller endda skabe falske positive resultater.
Det er her, et værktøj som OncoPredict R kommer ind i billedet. Det fungerer som en avanceret støjreduktionsteknologi for genetiske data. Ved at korrigere for GLDS kan forskere rense datasættet og se de underliggende sammenhænge meget klarere. Resultaterne er bemærkelsesværdige. Gene-lægemiddel-associationer, der tidligere ikke blev anset for statistisk signifikante, kan pludselig vise sig at være stærke og pålidelige biomarkører efter denne korrektion. Omvendt kan formodede sammenhænge vise sig at være falske alarmer. Denne forfinelse er afgørende for at udvikle præcise diagnostiske tests, der kan guide læger til at vælge den rigtige medicin til den rigtige patient første gang.
CancerDR: Et Digitalt Bibliotek over Kræftens Svagheder
Hvis OncoPredict R er specialværktøjet til at finde de rigtige ledetråde, så er CancerDR det enorme bibliotek, hvor alle ledetrådene er samlet og organiseret. CancerDR er en omfattende database, der fungerer som et opslagsværk for forskere inden for kræftmedicin. Den indeholder detaljeret information om kræftlægemidler, deres molekylære mål (de proteiner i cellen, som medicinen påvirker) og et bredt udvalg af kræftcellelinjer.
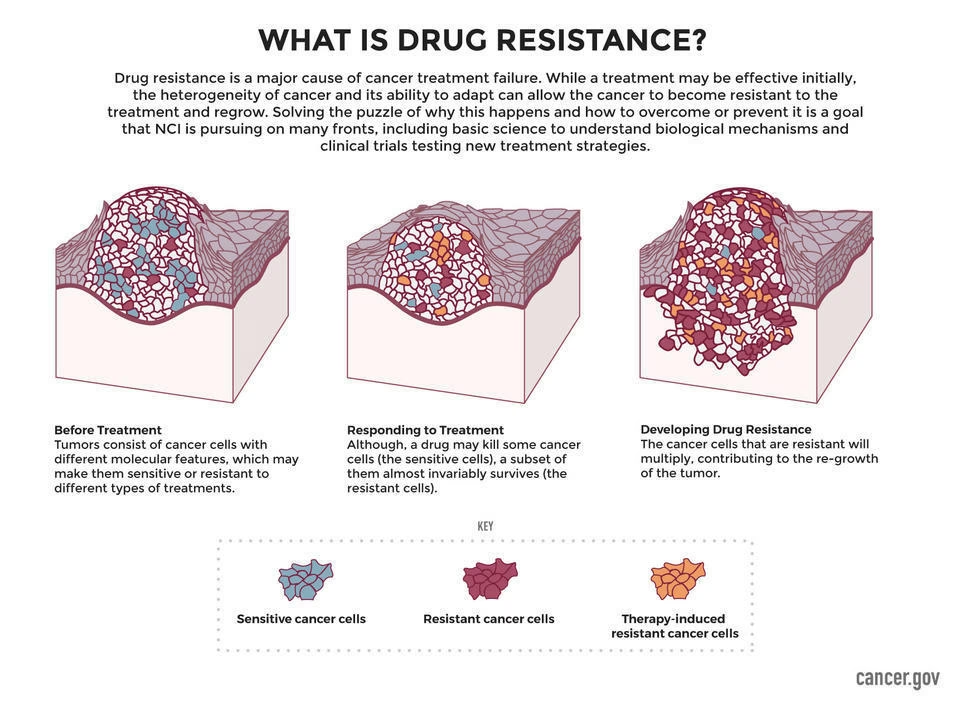
En af de mest presserende udfordringer i moderne kræftbehandling er lægemiddelresistens. En patient kan i starten reagere godt på en behandling, men over tid kan kræftcellerne udvikle nye mutationer, der gør dem resistente over for medicinen. CancerDR er designet specifikt til at tackle dette problem. Databasen har en indbygget funktion til sekvensanalyse, der gør det muligt for forskere at sammenligne gen-sekvenser fra resistente tumorer med dem fra følsomme tumorer. Dette kan afsløre præcis hvilke mutationer der er ansvarlige for resistensen, hvilket er uvurderlig viden for udviklingen af nye lægemidler, der kan omgå disse resistensmekanismer.
Yderligere funktioner i CancerDR inkluderer:
- Klyngeanalyse af Cellelinjer: Værktøjet kan gruppere (klynge) cellelinjer baseret på deres følsomhed over for forskellige lægemidler. Dette hjælper med at identificere grupper af kræftformer, der deler fælles sårbarheder, og kan afsløre, hvorfor nogle kræfttyper er naturligt resistente over for en bestemt behandling.
- Identifikation af Bredspektrede Lægemidler: Ved at analysere, hvilke lægemidler der er effektive mod et bredt spektrum af forskellige cellelinjer, kan forskere identificere "promiskuøse" eller bredspektrede lægemidler. Disse kan potentielt bruges til at behandle flere forskellige kræfttyper.
- Understøttelse af Personlig Medicin: En af de mest spændende anvendelser er muligheden for at uploade en patients egne genetiske data (f.eks. fra en tumorbiopsi) til systemet. Ved at sammenligne patientens gensekvenser med de kendte sekvenser i databasen, kan man teoretisk forudsige, om en given behandling vil være effektiv eller ej. Dette er kernen i målrettet behandling og er et stort skridt væk fra gætværk og hen imod datadrevet præcision.
Fra Laboratorie til Klinik: En Patients Hypotetiske Rejse
For at gøre disse abstrakte koncepter mere konkrete, lad os forestille os en patients rejse i fremtidens sundhedssystem. En patient, lad os kalde hende Anna, diagnosticeres med lungekræft. I stedet for straks at starte standard kemoterapi, tager lægen en lille vævsprøve (biopsi) fra Annas tumor.
Denne prøve sendes til et laboratorium, hvor dens DNA bliver fuldt sekventeret ved hjælp af genomisk sekventering. De resulterende data – en komplet kortlægning af tumorens genetiske kode – analyseres ved hjælp af avancerede computerprogrammer. Disse programmer, der bygger på principper fra værktøjer som OncoPredict R og databaser som CancerDR, scanner Annas tumor-DNA for specifikke mutationer, der er kendt for at påvirke lægemiddelrespons.
Analysen afslører, at Annas tumor har en sjælden mutation i et gen kaldet ALK. Databaserne viser, at patienter med netop denne mutation reagerer ekstremt godt på en bestemt type målrettet medicin. Samtidig viser analysen, at hendes tumor har andre markører, der indikerer, at traditionel kemoterapi sandsynligvis vil have ringe effekt. Bevæbnet med denne viden kan Annas onkolog ordinere den målrettede ALK-hæmmer. Resultatet er en behandling, der er langt mere effektiv og har færre bivirkninger, end standardbehandlingen ville have haft. Dette er ikke længere science fiction, men en virkelighed for et voksende antal kræftpatienter.
Sammenligning af Tilgange: Traditionel vs. Personlig Behandling
Den transformative effekt af denne nye tilgang kan bedst illustreres ved en direkte sammenligning.
| Karakteristik | Traditionel Tilgang | Personlig, Datadrevet Tilgang |
|---|---|---|
| Diagnosegrundlag | Baseret på organ (f.eks. lungekræft) og celletype set i mikroskop. | Baseret på organ, celletype OG tumorens molekylære og genetiske profil. |
| Valg af Behandling | Standardiserede protokoller for en given kræfttype. | Skræddersyet til de specifikke genetiske drivere og sårbarheder i patientens tumor. |
| Forudsigelse af Effekt | Baseret på statistiske gennemsnit fra store patientgrupper. | Forudsiges af biomarkører, der giver en højere sandsynlighed for succes. |
| Håndtering af Resistens | Skift til en anden standardbehandling, når den første fejler. | Analyse af nye biopsier for at forstå resistensmekanismer og vælge en ny, målrettet behandling. |
Ofte Stillede Spørgsmål (FAQ)
Er disse værktøjer tilgængelige for min læge i dag?
OncoPredict R og CancerDR er primært forskningsværktøjer, der bruges i laboratorier til at drive opdagelser fremad. De er typisk ikke programmer, som en onkolog bruger direkte i klinikken. Dog er de principper og den viden, der genereres fra dem, fundamentale for udviklingen af de kliniske tests og målrettede behandlinger, som læger bruger i dag. Så selvom lægen ikke logger ind på CancerDR, er den viden, der ligger til grund for patientens behandling, i stigende grad hentet fra denne type forskning.
Hvad er et "drug target"?
Et "drug target" eller et lægemiddelmål er det specifikke molekyle i kroppen – oftest et protein – som et lægemiddel er designet til at interagere med. I kræftceller er disse mål ofte proteiner, der er overaktive på grund af en genmutation og som sender konstante signaler til cellen om at vokse og dele sig ukontrolleret. Målrettet medicin virker ved at blokere disse specifikke proteiner og dermed stoppe kræftens vækstsignal.
Betyder personlig medicin, at der findes en kur mod min specifikke kræft?
Det er vigtigt at have realistiske forventninger. Personlig medicin er ikke altid ensbetydende med en kur. Målet er at finde den mest effektive behandling blandt de eksisterende muligheder, forlænge overlevelsen og forbedre livskvaliteten ved at undgå ineffektive behandlinger med unødvendige bivirkninger. For nogle patienter kan det føre til langvarig sygdomskontrol, hvor kræften behandles som en kronisk sygdom. For andre kan det markant forlænge livet. Det er et kraftfuldt våben, men ikke en magisk løsning på alle kræftformer.
Konklusion: Et Paradigmeskifte i Onkologi
Vi befinder os midt i et paradigmeskifte. Overgangen fra en bred, uspecifik tilgang til en præcis, datadrevet og personlig kræftbehandling er i fuld gang. Værktøjer som OncoPredict R forbedrer vores evne til at finde de afgørende genetiske signaler i en overvældende mængde data, mens platforme som CancerDR giver forskere og lægemiddeludviklere det nødvendige bibliotek til at omsætte denne viden til handling. Selvom der stadig er store udfordringer forbundet med omkostninger, datakompleksitet og kræftens evne til at udvikle sig, er retningen klar. Fremtiden for kræftbehandling ligger i at forstå og udnytte den unikke biologi i hver enkelt patients sygdom for at levere en mere intelligent, mere effektiv og mere skånsom behandling.
Hvis du vil læse andre artikler, der ligner Genetisk Data Revolutionerer Kræftmedicin, kan du besøge kategorien Kræft.
