17/06/2017
I hjertet af Europas sundhedssystem ligger et komplekst, men afgørende netværk af regler og agenturer, der arbejder for at sikre, at den medicin, vi bruger, er både sikker og effektiv. Centralt i dette system står Det Europæiske Lægemiddelagentur (EMA), som spiller en afgørende rolle i den videnskabelige evaluering, tilsyn og overvågning af lægemidler inden for Den Europæiske Union (EU). Samtidig er det farmaceutiske landskab i konstant forandring, med nye lovgivningsmæssige reformer på vej i 2025, der vil påvirke alt fra kliniske forsøg til håndtering af lægemiddelmangel. Denne artikel giver dig en dybdegående forståelse af EMA's processer og de kommende ændringer, så du er bedre rustet til at navigere i fremtidens sundhedssystem.
Det Europæiske Lægemiddelagenturs (EMA) afgørende rolle
EMA blev oprettet i 1995 for at harmonisere og centralisere godkendelsen af lægemidler på tværs af EU. Agenturets primære funktion er at koordinere den videnskabelige evaluering af ansøgninger om markedsføringstilladelse. Dette system gør det muligt for medicinalvirksomheder at opnå en enkelt markedsføringstilladelse, der er gyldig i alle EU-medlemsstater samt Island, Liechtenstein og Norge. Dette fremmer ikke kun et fælles marked for lægemidler, men sikrer også, at alle europæiske borgere har adgang til medicin, der lever op til de samme høje standarder for kvalitet, sikkerhed og effekt.
EMA evaluerer lægemidler gennem to primære procedurer: standardproceduren og den accelererede procedure. Valget af procedure afhænger af lægemidlets art og det medicinske behov, det adresserer.
Standardproceduren: Den grundige vej til godkendelse
Standardproceduren er den mest almindelige vej for nye lægemidler. Den følger en nøje fastlagt tidsplan på 210 dage. Det er dog vigtigt at bemærke, at denne tidslinje kan blive sat på pause, hvilket er kendt som "klokstop".
Processen er opdelt i flere faser:
- Dag 1: Den officielle evaluering begynder. Rapporteuren og medrapporteuren, udpeget af Udvalget for Humanmedicinske Lægemidler (CHMP), starter deres grundige gennemgang af den indsendte dokumentation.
- Dag 70: De første foreløbige evalueringsrapporter indsendes.
- Dag 100: Fristen for kommentarer fra andre CHMP-medlemmer udløber.
- Dag 115-120: CHMP diskuterer de indledende fund og vedtager en liste af spørgsmål, som medicinalvirksomheden skal besvare.
- Dag 120: Et "klokstop" indledes. Tidslinjen på 210 dage sættes på pause for at give virksomheden tid til at forberede fyldestgørende svar på udvalgets spørgsmål.
- Dag 121 (genoptagelse): Når virksomhedens svar er modtaget, genoptages evalueringen.
- Dag 150: En samlet endelig evalueringsrapport præsenteres for CHMP.
- Dag 180: CHMP holder en afsluttende diskussion og forbereder sin endelige udtalelse (opinion).
- Dag 210: CHMP vedtager sin endelige udtalelse og sender den til Europa-Kommissionen.
Hvorfor kan godkendelsesprocessen overstige 300 dage?
Selvom den teoretiske tidslinje er 210 dage, kan den samlede proces ofte strække sig over 300 dage eller mere. Dette skyldes primært to faktorer:
- Klokstop (Clock Stops): Varigheden af et klokstop afhænger udelukkende af, hvor lang tid medicinalvirksomheden bruger på at indsamle data og formulere svar på CHMP's spørgsmål. Disse pauser kan tilføje adskillige uger eller endda måneder til den samlede proces.
- Europa-Kommissionens behandlingstid: Efter at have modtaget en positiv udtalelse fra CHMP, har Europa-Kommissionen i gennemsnit 67 dage til at træffe den endelige juridiske beslutning og udstede markedsføringstilladelsen.
Accelereret Procedure: Hurtigere adgang til vital medicin
For lægemidler, der adresserer udækkede medicinske behov eller repræsenterer en betydelig terapeutisk innovation, findes der en accelereret procedure. Denne mekanisme er designet til at give patienter hurtigere adgang til banebrydende behandlinger af stor interesse for folkesundheden.
Under den accelererede procedure reduceres evalueringstiden fra 210 til 150 dage (eksklusive klokstop). For at komme i betragtning skal et lægemiddel opfylde strenge kriterier, herunder at være af stor interesse for folkesundheden, især set fra et terapeutisk innovationsperspektiv. Virksomheden skal indsende en begrundet anmodning, som EMA vurderer, før proceduren kan accepteres. Selvom tidslinjen er kortere, kan processen stadig omfatte klokstop, og i tilfælde af komplekse problemstillinger kan EMA beslutte at vende tilbage til standardproceduren.
Sammenligning af procedurer: Standard vs. Accelereret
For at give et klart overblik er her en sammenligning af de to godkendelsesprocedurer hos EMA.
| Funktion | Standardprocedure | Accelereret Procedure |
|---|---|---|
| Tidsramme (evaluering) | 210 dage (ekskl. klokstop) | 150 dage (ekskl. klokstop) |
| Anvendelse | Gælder for de fleste ansøgninger om markedsføringstilladelse. | Reserveret for lægemidler af stor interesse for folkesundheden og/eller terapeutisk innovation. |
| Krav til berettigelse | Ingen specifik begrundelse påkrævet. | Kræver en velbegrundet anmodning, der skal godkendes af EMA. |
| Formål | Sikre en grundig og robust evaluering af alle nye lægemidler. | Fremskynde adgangen til livsvigtige og innovative behandlinger. |
Fremtidens Regulering: EU's Farmaceutiske Reform i 2025
EU's lovgivningsmæssige rammer for den farmaceutiske sektor står over for betydelige ændringer, der vil træde i kraft fra 2025 og fremefter. Disse reformer sigter mod at modernisere systemet, styrke forsyningskæderne og forbedre patientadgangen til medicin i hele Europa.
Styrkelse af Kliniske Forsøg
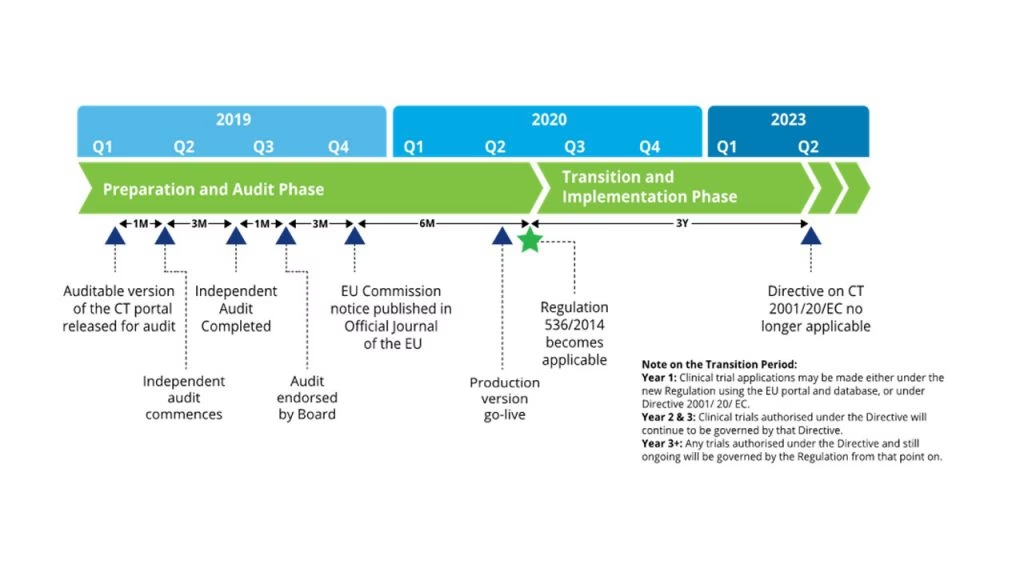
En central del af reformen er den fulde implementering af forordningen om kliniske forsøg (EU 536/2014) og det tilhørende informationssystem, CTIS (Clinical Trials Information System). Siden januar 2025 skal alle nye ansøgninger om kliniske forsøg indsendes via denne centrale digitale platform. Målet er at øge gennemsigtigheden og effektiviteten i udførelsen af kliniske forsøg på tværs af landegrænser i EU. Dette er især vigtigt for patienter med sjældne sygdomme, da det letter adgangen til forsøg, der måske ikke er tilgængelige i deres hjemland.

Bekæmpelse af Lægemiddelmangel
Den globale sundhedskrise og geopolitiske spændinger har sat fokus på sårbarheden i Europas forsyningskæder for medicin. Lægemiddelmangel er blevet et presserende problem. Som reaktion herpå har Kommissionen foreslået en "Critical Medicines Act" for at styrke forsyningskæderne for kritiske lægemidler. Samtidig er European Shortages Monitoring Platform (ESMP) blevet obligatorisk. Denne platform giver realtidsdata om tilgængeligheden af medicin, hvilket gør det muligt for myndighederne at handle proaktivt for at forhindre og afbøde mangelsituationer. Indehavere af markedsføringstilladelser er nu forpligtet til at rapportere data om udbud og efterspørgsel direkte til platformen.
Nye Regler for Substanser af Menneskelig Oprindelse (SoHO)
En ny forordning om substanser af menneskelig oprindelse (SoHO) vil indføre strenge kvalitets- og sikkerhedsstandarder for alt fra blod og væv til celler, der anvendes i behandlinger og i produktionen af lægemidler. Formålet er at sikre en robust beskyttelse af både donorer og modtagere og at styrke forsyningssikkerheden for disse kritiske substanser. En central EU SoHO-platform vil blive udviklet for at strømline dataudveksling og administration.
Fælles Vurdering af Sundhedsteknologi (HTA)
Forordningen om medicinsk teknologivurdering (HTA) trådte i kraft i januar 2025. Den indfører en ny æra af samarbejde mellem medlemslandene om vurdering af sundhedsteknologier, herunder nye lægemidler. Visse typer medicin, såsom nye kræftbehandlinger og avancerede terapier, skal nu gennemgå en fælles klinisk vurdering af flere EU-lande, før de kommer på markedet. Dette skal sikre en mere ensartet og effektiv vurdering af nye behandlingers sikkerhed og effekt, hvilket i sidste ende gavner patientsikkerhed.
Ofte Stillede Spørgsmål (OSS)
Hvad er den primære rolle for Det Europæiske Lægemiddelagentur (EMA)?
EMA's primære rolle er at beskytte og fremme folke- og dyresundheden gennem videnskabelig evaluering og overvågning af lægemidler. Agenturet centraliserer godkendelsesprocessen for medicin i EU, hvilket sikrer, at alle lægemidler på det europæiske marked lever op til de samme høje standarder for sikkerhed, kvalitet og virkning.
Hvad er den største forskel på standard- og accelereret procedure?
Den største forskel ligger i tidsrammen og formålet. Standardproceduren tager 210 dage og er den normale vej for de fleste lægemidler. Den accelererede procedure tager 150 dage og er forbeholdt lægemidler, der dækker et stort, udækket medicinsk behov eller udgør en markant terapeutisk forbedring. Målet med den accelererede procedure er at give patienter hurtigere adgang til banebrydende behandlinger.
Hvorfor kan godkendelse af medicin tage længere tid end den officielle tidsplan?
Processen kan blive forlænget på grund af såkaldte "klokstop", hvor evalueringstiden sættes på pause. Dette sker, når EMA's ekspertudvalg (CHMP) stiller spørgsmål til medicinalvirksomheden, som kræver yderligere data eller afklaringer. Varigheden af pausen afhænger af, hvor hurtigt virksomheden kan levere de nødvendige oplysninger. Derudover tager Europa-Kommissionens endelige beslutningsproces også tid.
Hvad er de vigtigste mål med de nye EU-regler for lægemidler i 2025?
De nye regler sigter mod at modernisere det europæiske lægemiddelsystem. Hovedmålene er at forbedre patienters adgang til innovative lægemidler, bekæmpe og forebygge lægemiddelmangel ved at styrke forsyningskæderne, øge gennemsigtigheden i kliniske forsøg og sikre høje sikkerhedsstandarder for alle sundhedsrelaterede produkter, herunder substanser af menneskelig oprindelse.
Konklusion
Forståelsen af EU's regulatoriske landskab for lægemidler er afgørende for både medicinalindustrien og for patienterne. EMA's etablerede og grundige godkendelsesprocedurer sikrer, at kun sikker og effektiv medicin når markedet. Samtidig viser de kommende reformer i 2025 en klar ambition om at skabe et mere robust, gennemsigtigt og patientcentreret sundhedssystem i Europa. Ved at styrke overvågningen, fremme innovation og tackle udfordringer som lægemiddelmangel arbejder EU målrettet for at sikre en sundere fremtid for alle sine borgere.
Hvis du vil læse andre artikler, der ligner EU's Lægemiddelregulering: En Komplet Guide, kan du besøge kategorien Sundhed.
