15/11/2016
Den Overraskende Sandhed om Energiens Små Hjælpere
I vores konstante søgen efter renere og mere effektive energikilder spiller videnskaben en afgørende rolle. En af de mest lovende teknologier er brændselsceller, som kan omdanne kemisk energi direkte til elektricitet med vand som det eneste biprodukt. Hjertet i enhver brændselscelle er en såkaldt katalysator – et materiale, der fremskynder de kemiske reaktioner uden selv at blive forbrugt. I årtier har dyre ædelmetaller som platin været guldstandarden, men forskere arbejder utrætteligt på at finde billigere og mere tilgængelige alternativer. En nylig undersøgelse har kastet lys over en familie af materialer, spineloxider, og afsløret et fascinerende mysterium, der udfordrer vores måde at teste og forstå disse vigtige komponenter på.
Jagten på den Perfekte Katalysator
Forskere har rettet deres opmærksomhed mod oxider baseret på almindelige metaller som mangan (Mn) og cobalt (Co). Disse materialer er ikke kun billigere end platin, men de har også vist et stort potentiale. I et specifikt studie syntetiserede et forskerhold nanokrystaller af forskellige spineloxider: et baseret på rent mangan (Mn₃O₄), et på rent cobalt (Co₃O₄) og et blandet oxid (Co₁.₅Mn₁.₅O₄). Disse bittesmå krystaller, kun få nanometer i størrelse, blev fastgjort til et kulstofmateriale for at skabe en stabil og effektiv katalysator.
Målet var klart: at sammenligne disse kandidater og finde ud af, hvilken der var bedst til at drive den kritiske iltreduktionsreaktion (ORR), en fundamental proces i en brændselscelle. Ved hjælp af avancerede teknikker som røntgendiffraktion og elektronmikroskopi bekræftede forskerne materialernes struktur og partikelstørrelse, hvilket sikrede, at de havde et solidt grundlag for deres sammenlignende tests.
Den Første Test: Laboratoriets Dom
Den første runde af tests fandt sted under kontrollerede laboratorieforhold ved hjælp af en standardmetode kendt som RDE (Rotating Disk Electrode). Denne teknik giver forskerne mulighed for hurtigt at vurdere en katalysators iboende aktivitet. Resultaterne tegnede et klart billede: Den blandede cobalt-mangan katalysator (Co₁.₅Mn₁.₅O₄/C) var den ubestridte vinder. Den viste en højere effektivitet og hurtigere reaktionskinetik sammenlignet med den rene mangan-katalysator (Mn₃O₄/C), som virkede træg og mindre potent.
Baseret på disse indledende resultater ville den logiske konklusion være at kassere den rene mangan-katalysator og fokusere udelukkende på den overlegne blandede version. Men videnskab handler om at stille spørgsmål og teste antagelser, især når man bevæger sig fra et idealiseret laboratorium til den komplekse virkelighed i en fungerende enhed.
Overraskelsen: Fra Laboratorium til Virkelighed
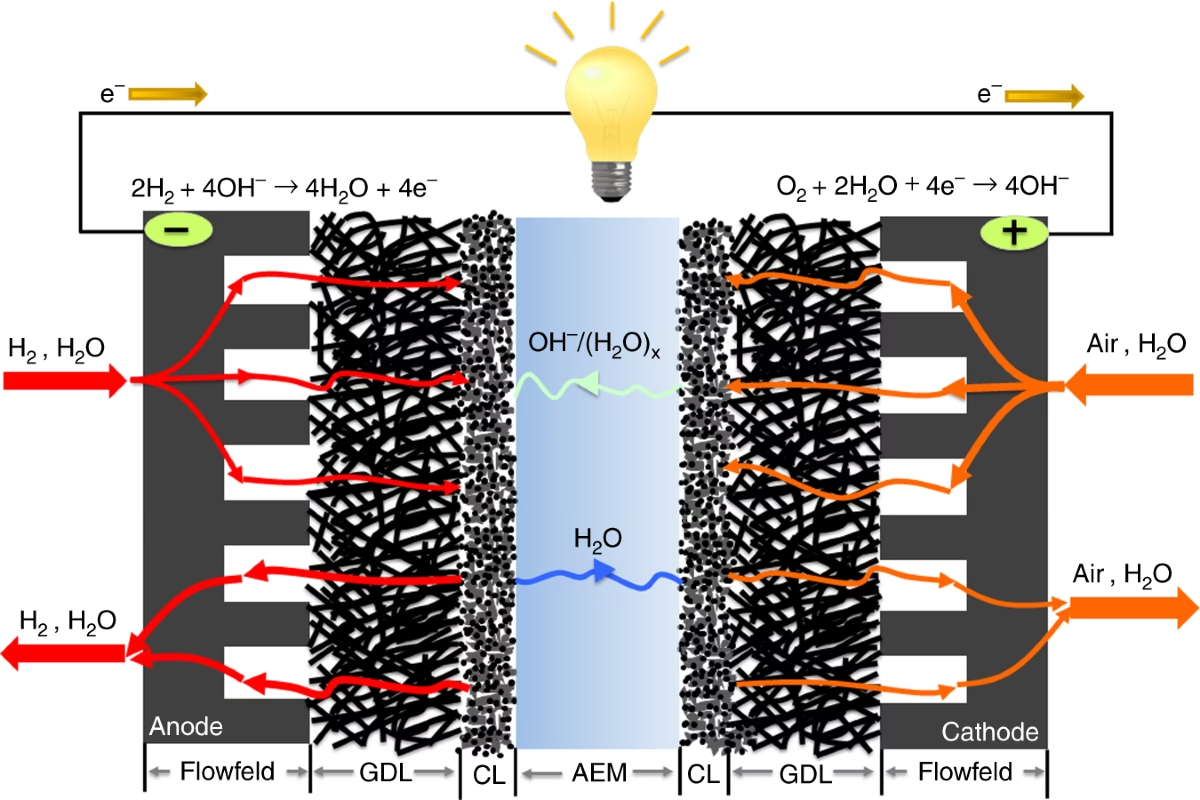
Det næste skridt var at bygge og teste en rigtig anionbyttermembran-brændselscelle (AEMFC). Dette er springet fra teori til praksis, hvor katalysatoren skal præstere under høje temperaturer, tryk og i et intenst kemisk miljø. Forskerne samlede brændselsceller med både den "svage" mangan-katalysator og den "stærke" blandede katalysator.
Resultaterne var intet mindre end forbløffende. I modsætning til alle forventninger leverede brændselscellen med den rene mangan-katalysator en præstation, der var fuldstændig på højde med cellen med den anerkendte mester, den blandede cobalt-mangan katalysator. Begge opnåede en imponerende spidseffekttæthed på 1,5 W/cm² og en maksimal strømtæthed på 3,5 A/cm². Den katalysator, der var blevet dømt ude i laboratoriet, var pludselig en stjernespiller på banen. Dette skabte et presserende spørgsmål: Hvad skete der inde i brændselscellen, som fuldstændig ændrede spillereglerne?
Sammenligning af Resultater
| Katalysator | RDE Test (Laboratorium) | AEMFC Test (Brændselscelle) |
|---|---|---|
| Mn₃O₄/C (Ren Mangan) | Lavere ydeevne | Høj ydeevne |
| Co₁.₅Mn₁.₅O₄/C (Mangan-Cobalt) | Høj ydeevne | Høj ydeevne |
Under Luppen: Avanceret Teknologi Afslører Sandheden
For at løse mysteriet måtte forskerne se, hvad der skete med katalysatoratomerne i realtid, mens de arbejdede. De anvendte en utrolig kraftfuld teknik kaldet X-ray Absorption Spectroscopy (XAS) under både laboratorieforhold (in-situ) og under reelle driftsbetingelser i brændselscellen (operando). Tænk på det som et ultra-avanceret røntgenkamera, der kan fotografere den kemiske tilstand og den lokale struktur af specifikke atomer, mens de udfører deres arbejde.
Disse operando-målinger er afgørende, fordi mange materialer, især katalysatorer, ikke er statiske. De kan ændre sig, tilpasse sig og transformere sig som reaktion på deres omgivelser. At studere en katalysator i hvile er som at bedømme en atlet, mens de sover – man ser ikke deres sande potentiale, før de er i fuld aktion.
Transformationen af Mangan: En Kemisk Kamæleon
XAS-analysen gav det chokerende, men klare svar. Under de milde laboratorieforhold bestod den rene mangan-katalysator af manganatomer i en lavere gennemsnitlig oxidationstilstand (en blanding af Mn²⁺ og Mn³⁺). Det var denne tilstand, der førte til den dårligere ydeevne.
Men inde i den varme, iltrige og elektrisk aktive brændselscelle skete der en dramatisk transformation. Det barske miljø tvang manganatomerne i Mn₃O₄/C-katalysatoren til at ændre sig. De blev oxideret til en højere gennemsnitlig tilstand (overvejende Mn³⁺) og omarrangerede deres atomare nabolag. Denne nye, energirige konfiguration viste sig at være den aktive tilstand – den ideelle form for at katalysere iltreduktionsreaktionen med høj effektivitet.
Den blandede cobalt-mangan katalysator, derimod, havde allerede sine manganatomer i denne fordelagtige, høje oxidationstilstand fra starten. Derfor præsterede den godt i begge tests. Mysteriet var løst: Den rene mangan-katalysator var ikke svag; den var en "sovende kæmpe", der kun vågnede og afslørede sin sande styrke under de krævende driftsbetingelser i en rigtig enhed.
Hvad Betyder Det for Fremtiden?
Denne opdagelse har vidtrækkende konsekvenser. For det første understreger den en kritisk pointe i materialevidenskab: simple screeninger i et laboratorium kan være vildledende. For at finde de bedste materialer til virkelige anvendelser, er det essentielt at teste dem under de forhold, de rent faktisk skal fungere under. Operando-analyseteknikker er ikke længere en luksus, men en nødvendighed for at forstå og designe fremtidens højtydende materialer.
For det andet åbner det op for nye designstrategier. Måske er den bedste katalysator ikke en, der er perfekt fra syntesen, men en, der er designet til at transformere sig til den perfekte tilstand, når den tages i brug. Ved at forstå disse transformationsprocesser kan forskere nu skabe endnu bedre og mere holdbare katalysatorer baseret på billige og rigelige grundstoffer som mangan. Dette arbejde er et afgørende skridt på vejen mod en fremtid drevet af ren, effektiv og tilgængelig energi.
Ofte Stillede Spørgsmål (FAQ)
- Hvad er en katalysator?
En katalysator er et stof, der øger hastigheden af en kemisk reaktion uden selv at blive ændret permanent i processen. I en brændselscelle hjælper den med at omdanne brændstof (som brint) og ilt til elektricitet meget hurtigere, end det ellers ville ske.
- Hvorfor er denne forskning vigtig?
Den er vigtig, fordi den hjælper os med at finde billigere alternativer til de dyre ædelmetaller, der i øjeblikket bruges i teknologier som brændselsceller. Desuden viser den, hvor afgørende det er at teste materialer under realistiske forhold for at forstå deres sande potentiale.
- Hvad er en brændselscelle?
En brændselscelle er en elektrokemisk enhed, der konverterer den kemiske energi fra et brændstof (ofte brint) og et oxidationsmiddel (ofte ilt) direkte til elektricitet, varme og vand. Den fungerer som et batteri, der konstant kan genoplades med brændstof.
- Hvorfor var der forskel på resultaterne i laboratoriet og i den rigtige enhed?
Forskellen opstod, fordi den rene mangan-katalysator ændrede sin kemiske og strukturelle tilstand under de barske driftsbetingelser (høj temperatur, ilt) i den rigtige brændselscelle. Denne transformation "aktiverede" katalysatoren og gjorde den lige så effektiv som den anden katalysator, noget der ikke skete under de mildere laboratorieforhold.
Hvis du vil læse andre artikler, der ligner Fremtidens Energi: Et Nyt Katalysatormysterium Løst, kan du besøge kategorien Sundhed.