03/01/2024
Når vi taler om effekten af et lægemiddel, er det let at tænke på den maksimale virkning – det øjeblik, hvor medicinen virker kraftigst. Men i virkeligheden er den samlede effekt over tid ofte langt mere informativ. Inden for farmakologi og medicinsk forskning er et af de mest kraftfulde værktøjer til at kvantificere denne samlede eksponering kendt som Area Under the Curve (AUC). Traditionelt brugt til at måle, hvor meget af et lægemiddel der er i blodbanen over en periode, men konceptet er nu ved at blive udvidet til at afdække komplekse biologiske reaktioner, såsom hvordan vores gener reagerer på behandling. En nyudviklet algoritme tager højde for biologisk støj og variabilitet, hvilket giver forskere et hidtil uset præcist billede af et lægemiddels sande effekt.

Hvad er Area Under the Curve (AUC)?
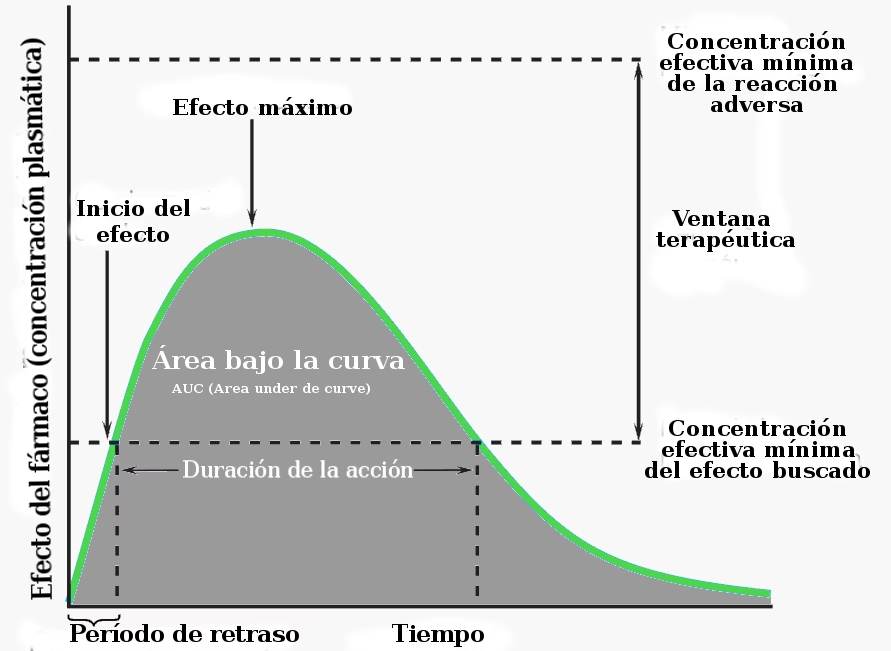
Forestil dig, at du tager en pille. Efter indtagelse vil koncentrationen af lægemidlet i dit blod stige, nå et højdepunkt og derefter gradvist falde, efterhånden som din krop metaboliserer og udskiller det. Hvis man plotter denne koncentration over tid på en graf, vil man få en kurve. Area Under the Curve, eller AUC, er bogstaveligt talt det matematiske areal under denne kurve.
Denne værdi er ekstremt nyttig, fordi den repræsenterer den samlede eksponering, kroppen har haft for lægemidlet. To forskellige lægemidler kan have samme maksimale koncentration, men hvis det ene bliver i kroppen i længere tid, vil det have en meget større AUC. Derfor giver AUC indsigt i:
- Total lægemiddeleksponering: Hvor meget medicin kroppen samlet set har håndteret.
- Clearance rate: Hvor hurtigt kroppen fjerner lægemidlet. En langsom clearance fører til en højere AUC.
- Bioækvivalens: Man kan sammenligne generiske lægemidler med originallægemidler ved at se, om de producerer en lignende AUC, hvilket indikerer, at de leverer samme mængde aktivt stof til kroppen over tid.
Denne metode har været en hjørnesten i farmakokinetik – studiet af, hvordan kroppen påvirker et lægemiddel.
Udfordringen med en Variabel Baseline
Mens AUC-konceptet er relativt ligetil for et lægemiddel, der introduceres udefra (hvor startkoncentrationen er nul), bliver billedet langt mere kompliceret, når vi vil måle effekten på processer, der allerede foregår i kroppen. Et perfekt eksempel er genekspression – processen, hvor information fra et gen bruges til at skabe et funktionelt produkt som et protein.
Vores gener er ikke blot 'tændt' eller 'slukket'. Deres aktivitetsniveau, eller ekspression, svinger konstant. Denne naturlige tilstand kaldes en baseline eller grundlinje. Problemet er, at denne baseline sjældent er en flad, konstant linje. Den påvirkes af utallige faktorer:
- Døgnrytmer: Mange gener er mere aktive på bestemte tidspunkter af dagen.
- Biologisk støj: Tilfældige udsving er en normal del af cellulære processer.
- Miljømæssige faktorer: Kost, stress og andre faktorer kan forårsage små ændringer.
Denne iboende variabilitet skaber en stor udfordring. Hvis en forsker giver et lægemiddel og ser, at et gens ekspression stiger, hvordan kan de så være sikre på, at det er en reel effekt af lægemidlet og ikke bare en del af genets normale, støjende udsving? At beregne en meningsfuld AUC i forhold til en bevægelig og usikker baseline har hidtil været en betydelig videnskabelig forhindring.
En Ny Algoritme til Præcis Måling
For at løse dette problem har forskere udviklet en avanceret algoritme, der gentænker, hvordan AUC beregnes i komplekse biologiske systemer. I stedet for at antage en baseline på nul eller en fast værdi, gør algoritmen noget smartere: den måler og sammenligner AUC for selve responsen med AUC for den estimerede baseline, alt imens den tager højde for usikkerheden i begge målinger.
Kernen i metoden er at afgøre, om afvigelsen fra baselinen er statistisk signifikant. Algoritmen kan estimere baselinen på forskellige måder afhængigt af de tilgængelige data:
- Kun starttidspunkt (t=0): Hvis kun data før behandling er tilgængelige, antages baselinen at være konstant baseret på disse startværdier.
- Start- og sluttidspunkt: Hvis responsen forventes at vende tilbage til normalen (f.eks. efter en enkelt dosis), bruges både de første og sidste målinger til at skabe en mere præcis baseline.
- Separat kontrolgruppe: Den ideelle, men ressourcekrævende, metode er at have en ubehandlet kontrolgruppe, der måles på alle tidspunkter, hvilket giver den mest nøjagtige baseline.
Sammenligning af Metoder
| Egenskab | Traditionel AUC-beregning | Avanceret AUC med Variabel Baseline |
|---|---|---|
| Baseline Antagelse | Antager en fast eller nul-baseline. | Behandler baselinen som variabel og usikker. |
| Fokus | Måler den samlede, absolutte eksponering. | Måler den signifikante afvigelse fra den forventede normale tilstand. |
| Håndtering af Støj | Kan blive forvirret af naturlige biologiske udsving. | Inkorporerer statistisk usikkerhed for at skelne signal fra støj. |
| Anvendelsesområde | Primært simpel farmakokinetik. | Ideel til kompleks farmakodynamik og genekspressionsanalyse. |
Identifikation af Bifasiske Reaktioner: Et Gennembrud
En af de mest spændende funktioner ved den nye algoritme er dens evne til at identificere en bifasisk reaktion. Dette er en to-faset respons, hvor et system først reagerer i én retning og derefter i den modsatte. For eksempel kan et lægemiddel i første omgang undertrykke (nedregulere) et gens aktivitet for derefter senere at forårsage en kraftig stigning i aktiviteten (opregulering), før det vender tilbage til normalen.
Med en traditionel AUC-beregning ville disse to effekter kunne ophæve hinanden. Det negative areal (under baselinen) og det positive areal (over baselinen) ville blive lagt sammen, og nettoresultatet kunne være tæt på nul. Forskeren ville fejlagtigt konkludere, at lægemidlet ingen signifikant effekt havde, og dermed overse en vigtig biologisk mekanisme.
Den nye algoritme løser dette ved at beregne de positive og negative bidrag til AUC separat. Den summerer de absolutte værdier af afvigelserne, hvilket giver et sandt mål for den *samlede forstyrrelse* væk fra baselinen. Dette gør det muligt at klassificere genresponser præcist som:
- Opreguleret: En overvejende positiv afvigelse fra baselinen.
- Nedreguleret: En overvejende negativ afvigelse fra baselinen.
- Bifasisk: Både en signifikant positiv og negativ afvigelse.
Denne evne til at afdække komplekse responsprofiler er et kæmpe skridt fremad for at forstå de nuancerede måder, hvorpå lægemidler interagerer med vores kroppe.
Validering og Anvendelse i Forskning
For at sikre pålideligheden er algoritmen blevet grundigt testet. Først blev den anvendt på syntetiske data genereret af computermodeller, hvor det korrekte resultat var kendt på forhånd. Dette beviste, at algoritmen fungerede som forventet under kontrollerede forhold. Derefter blev den anvendt på rigtige eksperimentelle data fra en undersøgelse af rotteleveres genrespons på kortikosteroidbehandling. Her demonstrerede metoden sin evne til at udvælge biologisk relevante gener og korrekt identificere deres responsprofiler, herunder komplekse bifasiske mønstre.
Metoden bruger robuste statistiske teknikker som bootstrapping, hvor computeren genererer tusindvis af nye datasæt ved at trække tilfældigt fra de originale målinger. Dette skaber en fordeling af mulige AUC-værdier, hvorfra man kan beregne et gennemsnit og et konfidensinterval – et mål for, hvor sikker man er på resultatet.
Ofte Stillede Spørgsmål (FAQ)
Hvad betyder AUC i simple termer?
Tænk på det som den samlede 'dosis' af en effekt over en given tidsperiode. For et lægemiddel er det den samlede mængde, din krop har været udsat for, ikke kun den maksimale koncentration på et enkelt tidspunkt. Det giver et mere komplet billede af virkningen.
Hvorfor kan man ikke bare måle effekten på ét tidspunkt?
Fordi biologiske systemer som genekspression er i konstant forandring. En enkelt måling kan være misvisende og afspejle et tilfældigt udsving snarere end en reel tendens. AUC fanger den samlede effekt over hele tidsforløbet, hvilket er langt mere pålideligt.
Hvad er en bifasisk reaktion, og hvorfor er den vigtig?
Det er en to-faset reaktion, for eksempel et fald efterfulgt af en stigning. Den er vigtig, fordi den afslører komplekse virkningsmekanismer, hvor et lægemiddel kan have forskellige effekter på forskellige tidspunkter. Traditionelle metoder kan let overse disse nuancerede reaktioner.
Er denne metode kun for genforskning?
Selvom den er særligt kraftfuld til analyse af genekspression, kan princippet anvendes på enhver kvantitativ biologisk måling, der afviger fra en variabel baseline. Dette kunne for eksempel være hormonniveauer, blodsukkermålinger eller inflammationsmarkører over tid.
Hvis du vil læse andre artikler, der ligner AUC: Forståelse af Lægemiddelrespons over Tid, kan du besøge kategorien Sundhed.