12/09/2007
Allergiske sygdomme som høfeber, astma, eksem og fødevareallergi er blevet en folkesygdom i Danmark og resten af den vestlige verden. For mange er det en livslang kamp med symptomer, der påvirker livskvaliteten, søvnen og den daglige funktion. I årtier har behandlingen primært fokuseret på at lindre symptomer med antihistaminer, næsesprays og cremer, eller i mere alvorlige tilfælde, immunterapi. Men hvad nu hvis vi kunne se ind i fremtiden? Hvad nu hvis vi, baseret på en persons unikke genetiske kode, kunne forudsige deres risiko, skræddersy deres behandling og måske endda forhindre allergien i at udvikle sig? Dette er ikke længere science fiction, men den spændende virkelighed, som genetisk forskning inden for allergiske sygdomme åbner døren for.
Vores arvemateriale, DNA'et, indeholder opskriften på, hvordan vores krop fungerer, inklusiv hvordan vores immunsystem reagerer på verden omkring os. Forskere afdækker i stigende grad de specifikke genvariationer, der gør nogle mennesker mere modtagelige for at udvikle allergier end andre. Denne viden er ved at transformere allergologien fra en reaktiv disciplin til en proaktiv og personlig medicinsk specialitet.
Forståelsen af Allergiens Genetiske Rødder
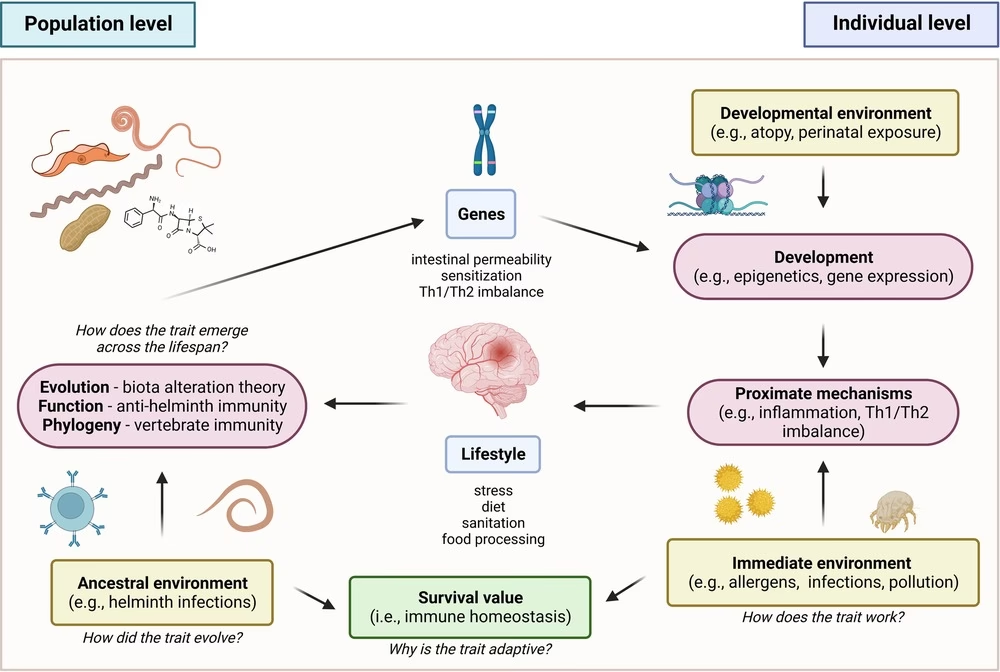
Det er længe blevet observeret, at allergier ofte løber i familier. Hvis begge forældre har en allergisk sygdom, er risikoen for, at deres barn også udvikler en, markant forhøjet. Dette peger tydeligt på en stærk genetisk komponent. Det er dog vigtigt at forstå, at der ikke findes ét enkelt 'allergigen'. I stedet er det et komplekst samspil mellem hundredvis af forskellige genvarianter, som hver især bidrager med en lille smule til den samlede risiko. Dette polygeniske landskab kompliceres yderligere af miljømæssige faktorer. En person kan have en genetisk disposition for allergi, men det er ofte eksponering for specifikke allergener, forurening, infektioner eller ændringer i livsstil, der 'tænder' for den genetiske kontakt og udløser sygdommen. Denne interaktion mellem arv og miljø er kernen i forståelsen af, hvorfor allergiforekomsten er eksploderet i de seneste årtier.
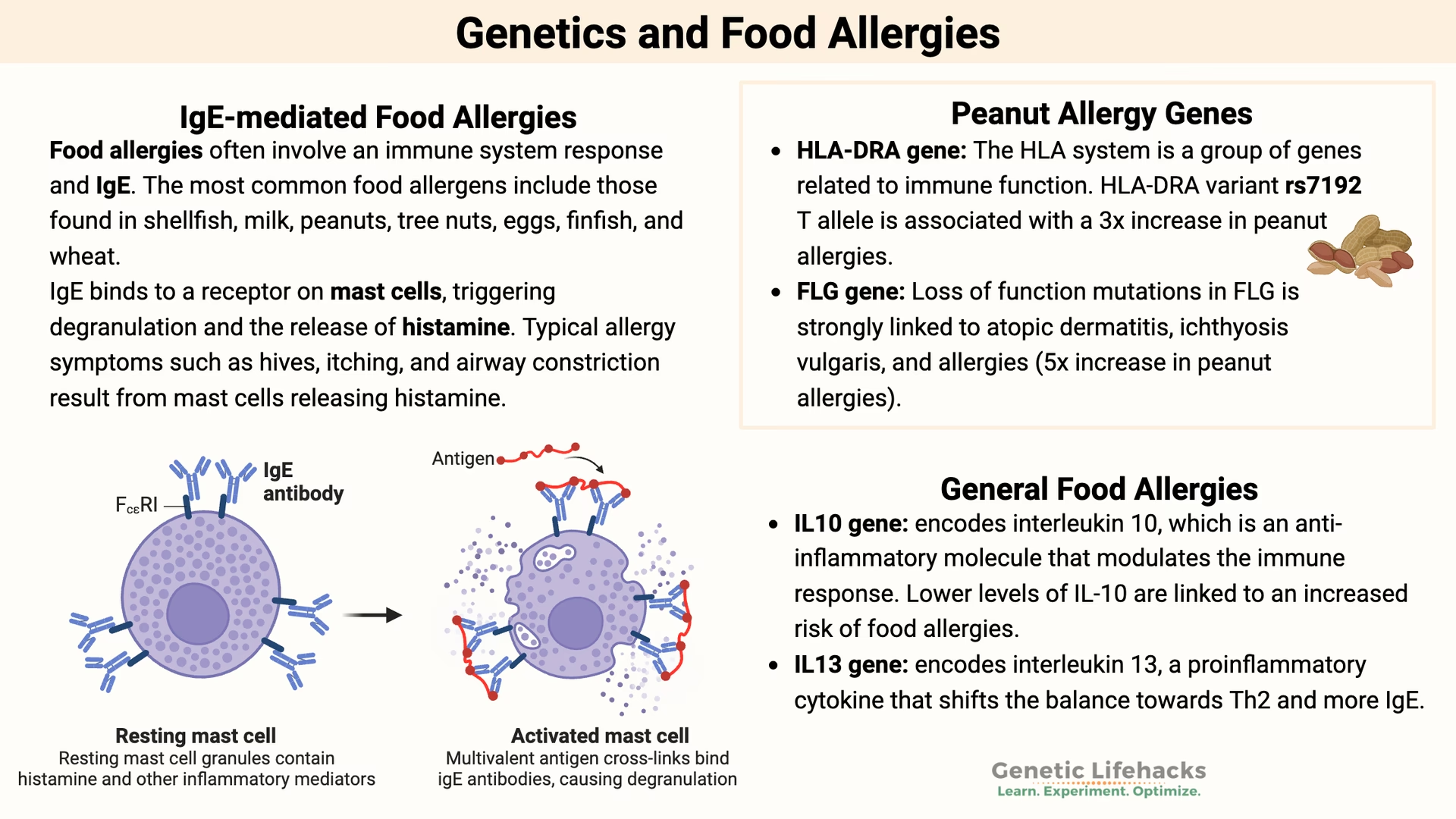
Et af de mest kendte eksempler er genet for proteinet filaggrin (FLG). Mutationer i dette gen er stærkt forbundet med udviklingen af atopisk eksem (børneeksem). Filaggrin er afgørende for at opretholde en sund hudbarriere. Når denne barriere er svækket på grund af en genfejl, kan allergener lettere trænge ind i huden og aktivere immunsystemet, hvilket ikke kun fører til eksem, men også øger risikoen for senere at udvikle fødevareallergi og astma – et fænomen kendt som 'den atopiske march'. Identifikation af sådanne nøglegener giver os konkrete biologiske mekanismer, vi kan målrette med fremtidig behandling.
Bedre Diagnostik gennem Endofænotyping
I dag stilles diagnosen 'astma' eller 'høfeber' primært baseret på en patients symptomer og kliniske tests. Men to personer med astma kan have vidt forskellige sygdomsforløb og reagere forskelligt på den samme medicin. Dette skyldes, at 'astma' ikke er én sygdom, men en paraplybetegnelse for flere forskellige underliggende sygdomsmekanismer. Her kommer begrebet endofænotyping ind i billedet.
Endofænotyping handler om at klassificere en sygdom baseret på dens specifikke molekylære og cellulære årsag, frem for kun at se på de ydre symptomer. Ved at analysere en patients genetiske markører kan læger i fremtiden identificere, hvilken specifik biologisk 'sti' der er gået galt. For eksempel kan én astmapatient have en type, der er drevet af høje niveauer af eosinofile celler (en type hvide blodlegemer), mens en anden har en type, der er drevet af neutrofile celler. Disse to typer kræver helt forskellig behandling. Genetisk information vil gøre det muligt at stille en langt mere præcis diagnose og dermed vælge den mest effektive behandling fra starten.
Forudsigelse af Sygdomsforløb og Behandlingsrespons
En af de største frustrationer for både patienter og læger er uforudsigeligheden ved allergiske sygdomme. Vil et barn med mild eksem vokse fra det, eller vil det udvikle alvorlig astma? Vil en patient med høfeber have gavn af immunterapi (allergivaccination), eller vil det være spild af tid og ressourcer? Genetisk information rummer potentialet til at give os svar på disse spørgsmål.
Ved at identificere genetiske profiler forbundet med en mere alvorlig prognose, kan læger iværksætte en mere intensiv og forebyggende indsats tidligt i forløbet. Dette gælder især for 'den atopiske march', hvor tidlig og effektiv behandling af eksem potentielt kan forhindre udviklingen af senere og mere alvorlige allergiske lidelser.
Lige så vigtigt er forudsigelsen af behandlingsrespons. Farmakogenomik er feltet, der studerer, hvordan vores gener påvirker vores reaktion på medicin. I fremtiden kan en simpel gentest afgøre, om en patient vil have god effekt af standardinhalatorer til astma, eller om de har brug for en mere avanceret biologisk behandling. Dette vil spare patienter for måneder eller år med ineffektiv 'prøv-dig-frem'-medicinering, reducere bivirkninger og sikre, at dyre, målrettede lægemidler kun gives til dem, der rent faktisk vil have gavn af dem.
Sammenligning: Nuværende vs. Fremtidig Allergibehandling
| Aspekt | Nuværende Tilgang (One-size-fits-all) | Fremtidig Genetisk Tilgang (Personlig Medicin) |
|---|---|---|
| Diagnose | Baseret på symptomer og generelle tests (priktest, lungefunktion). | Baseret på symptomer suppleret med genetisk profilering for at bestemme den specifikke endotype (sygdomsundertype). |
| Behandling | Standardiserede behandlinger gives til brede patientgrupper. Ofte en trial-and-error proces. | Behandling skræddersyes til patientens genetiske profil og forventede respons. Målrettet medicin fra start. |
| Prognose | Generelle forudsigelser baseret på statistikker og sygdommens sværhedsgrad. | Specifik risikovurdering for sygdomsprogression og udvikling af følgesygdomme baseret på genetik. |
| Forebyggelse | Generelle råd om at undgå kendte allergener. | Tidlig identifikation af højrisikoindivider med mulighed for proaktiv intervention for at forhindre sygdomsudvikling. |
Udvikling af Ny, Målrettet Terapi
Måske er det mest spændende potentiale ved genetisk forskning evnen til at afdække helt nye angrebspunkter for medicin. Når forskere identificerer et gen, der spiller en central rolle i den inflammatoriske proces, der driver en allergi, identificerer de samtidig et potentielt mål for et nyt lægemiddel. I stedet for at bruge bredspektrede lægemidler som steroider, der dæmper hele immunsystemet og kan have mange bivirkninger, kan man udvikle medicin, der meget præcist blokerer ét specifikt protein eller én specifik signalvej. Denne type målrettet terapi er allerede en realitet inden for f.eks. kræftbehandling og er nu på vej ind i behandlingen af svære allergiske sygdomme som astma og eksem. De såkaldte biologiske lægemidler er et eksempel på dette, og med en dybere genetisk forståelse vil vi se mange flere og endnu mere effektive behandlinger i fremtiden.
Udfordringer på Vejen Frem
Selvom fremtiden ser lys ud, er der stadig udfordringer. Det genetiske landskab for allergi er ekstremt komplekst, og vi er kun lige begyndt at forstå det fulde billede. Implementering af genetisk testning i den daglige kliniske praksis kræver store investeringer i teknologi, uddannelse af sundhedspersonale og udvikling af robuste systemer til at tolke de komplekse data. Derudover er der vigtige etiske overvejelser omkring datasikkerhed og risikoen for genetisk diskrimination. Det er afgørende, at denne udvikling sker på en ansvarlig måde, hvor patientens privatliv og rettigheder er i højsædet.
Ofte Stillede Spørgsmål (OSS)
- Betyder det, at hvis mine forældre har allergi, får jeg det helt sikkert også?
- Nej, ikke nødvendigvis. Du arver en øget risiko eller disposition, men ikke selve sygdommen. Miljøfaktorer spiller en afgørende rolle for, om din genetiske risiko bliver til en aktiv allergi. Du kan se det som at arve en 'ladt pistol', men miljøet afgør, om der bliver 'trykket på aftrækkeren'.
- Hvornår kan jeg forvente, at min læge tilbyder en gentest for min allergi?
- Det er en gradvis proces. Specialiserede genetiske tests bruges allerede på hospitalsafdelinger til at guide behandlingen af meget svære tilfælde af f.eks. astma. For mere almindelige allergier i almen praksis vil der sandsynligvis gå nogle år, før det bliver standardprocedure. Forskningen bevæger sig dog hurtigt.
- Kan denne forskning fjerne allergier helt fra verden?
- Det er usandsynligt, at allergier helt vil forsvinde, da de er et resultat af et komplekst samspil mellem mange gener og et stadigt skiftende miljø. Målet er snarere at opnå en langt bedre kontrol, at kunne forebygge de mest alvorlige tilfælde og at give hver enkelt patient en behandling, der er så effektiv og skånsom som muligt.
Konklusion: En Personlig Revolution
Genetiske opdagelser inden for allergiske sygdomme varsler en revolution inden for diagnostik, behandling og forebyggelse. Vi bevæger os væk fra en reaktiv, symptom-baseret tilgang og hen imod en proaktiv, personlig og præcisionsbaseret medicin. Ved at forstå den enkelte patients unikke genetiske profil kan vi i fremtiden tilbyde en behandling, der ikke bare er mere effektiv, men også har færre bivirkninger. Det vil give millioner af mennesker med allergi håb om en fremtid med færre symptomer og en markant forbedret livskvalitet. Den genetiske kode er nøglen, og forskerne er i fuld gang med at låse op for dens hemmeligheder.
Hvis du vil læse andre artikler, der ligner Allergiens Genetiske Fremtid: En Ny Æra, kan du besøge kategorien Sundhed.