14/12/2004
Psoriasis er en kronisk, autoimmun hudsygdom, der påvirker millioner af mennesker verden over. Den er kendetegnet ved røde, skællende plamager på huden, som kan være kløende og smertefulde. Årsagen er en overaktivitet i immunsystemet, der får hudceller til at dele sig alt for hurtigt. Selvom der findes mange behandlinger, er der stadig et stort behov for at udvikle nye og mere effektive lægemidler. En af de største udfordringer i denne proces er at finde præcise og pålidelige metoder til at teste potentielle lægemidler, før de gives til mennesker. Her kommer en banebrydende teknologi ind i billedet: 3D-hudmodeller. Disse avancerede laboratoriemodeller efterligner menneskelig hud på en utrolig realistisk måde og giver forskere en unik mulighed for at studere psoriasis og teste behandlinger i et kontrolleret miljø.
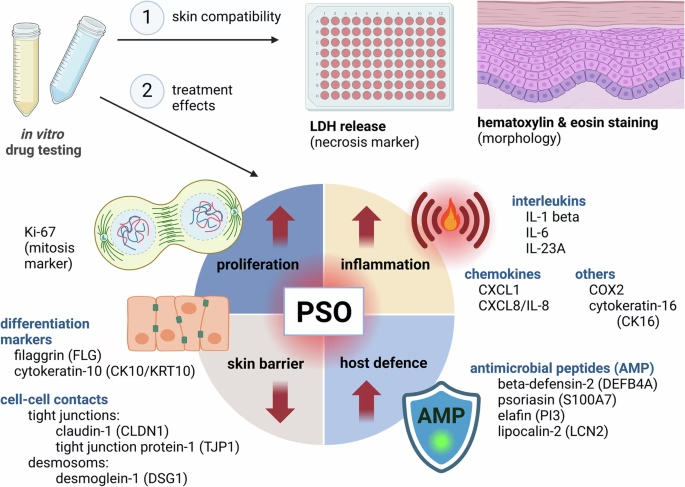
Hvad er en 3D-hudmodel, og hvordan skabes psoriasis?
Forestil dig at kunne bygge et lille stykke menneskehud i en petriskål. Det er i bund og grund, hvad en 3D-hudmodel er. Forskere tager humane hudceller – primært keratinocytter (de celler, der udgør det yderste hudlag, epidermis) og fibroblaster (celler fra det dybere hudlag, dermis) – og dyrker dem i lag på et stillads, ofte lavet af kollagen. Over tid organiserer cellerne sig og danner en struktur, der ligner ægte hud med både et dermis- og et epidermis-lag. Denne model er langt mere avanceret end traditionelle 2D-cellekulturer, hvor celler blot vokser i et fladt lag, da 3D-strukturen bedre afspejler hudens komplekse biologi og barrierefunktion.
For at omdanne denne sunde, laboratoriedyrkede hud til en model for psoriasis, udsætter forskerne den for en specifik 'cocktail' af inflammatoriske signalstoffer, kendt som cytokiner. Denne cocktail indeholder stoffer som TNF-α, IL-17A, IL-22 og andre, som alle spiller en central rolle i den betændelsesreaktion, der driver psoriasis hos patienter. Når modellen udsættes for disse cytokiner, begynder den at udvikle de klassiske tegn på psoriasis:
- Hyperproliferation: Hudcellerne i det basale lag begynder at dele sig ukontrolleret, hvilket fører til en fortykkelse af huden. Dette kan måles ved at kigge efter en markør kaldet Ki67, som kun findes i celler, der er i gang med at dele sig.
- Inflammation: Huden begynder at producere og frigive sine egne inflammatoriske stoffer, såsom IL-6 og IL-8, hvilket skaber en ond cirkel af betændelse.
- Nedsat barrierefunktion: Produktionen af vigtige strukturproteiner som Filaggrin (FLG) og Keratin 10 (CK10) falder drastisk. Disse proteiner er afgørende for at opretholde en sund og stærk hudbarriere. Uden dem bliver huden svag og sårbar.
- Overproduktion af antimikrobielle peptider (AMPs): Som en del af et overaktivt immunforsvar begynder huden at producere høje niveauer af proteiner som S100A7 (også kendt som psoriasin). Selvom disse er designet til at bekæmpe infektioner, bidrager de i forhøjede mængder til inflammationen.
Resultatet er en 3D-model, der ikke kun ligner psoriasis histologisk, men også opfører sig som det på et molekylært niveau. Dette giver et kraftfuldt værktøj til at undersøge sygdommens mekanismer og teste effekten af nye lægemidler.
Test af topiske behandlinger: Steroider mod naturmedicin
En af de mest almindelige behandlingsformer for psoriasis er topiske cremer og salver, der påføres direkte på huden. For at validere 3D-modellen testede forskerne to forskellige topiske stoffer: Dexamethason (DEX), et velkendt og potent syntetisk glukokortikoid (steroid), og Celastrol (CEL), et naturligt stof udvundet fra en plante, der bruges i traditionel kinesisk medicin.
Begge stoffer blev påført psoriasismodellerne over en periode. Resultaterne var oplysende. Både DEX og CEL viste sig at have en stærk anti-inflammatorisk effekt, idet de markant reducerede hudens udskillelse af IL-6 og IL-8. Interessant nok var Celastrol endnu mere potent end steroidet til at dæmpe udtrykket af flere inflammationsrelaterede gener.
Dog viste testen også modellens begrænsninger og realisme. Ingen af de to behandlinger formåede på den korte behandlingstid (6 dage) at genoprette hudens struktur markant. Produktionen af Filaggrin forblev lav, og den overaktive celledeling (hyperproliferation) fortsatte. Dette afspejler virkeligheden for mange patienter, hvor inflammationen kan dæmpes relativt hurtigt, mens selve helingen af hudens struktur og normalisering af cellevæksten er en meget langsommere proces, der kan tage uger eller måneder. Modellen viser altså, hvilke aspekter af sygdommen der reagerer hurtigt, og hvilke der er mere genstridige.
Sammenligning af Topiske Behandlinger i Modellen
| Egenskab | Dexamethason (DEX) | Celastrol (CEL) |
|---|---|---|
| Reduktion af inflammation (IL-6 & IL-8) | God effekt | Meget god effekt |
| Dæmpning af AMP-gener (f.eks. S100A7) | Minimal eller ingen effekt | Stærk dæmpende effekt |
| Genopretning af hudstruktur (Filaggrin) | Ingen effekt på kort sigt | Ingen effekt på kort sigt |
| Reduktion af celledeling (Ki67) | Ingen effekt på kort sigt | Ingen effekt på kort sigt |
Biologiske lægemidler: Målrettet behandling under luppen
For patienter med moderat til svær psoriasis er biologiske lægemidler ofte den mest effektive behandling. Disse er antistoffer designet til at blokere meget specifikke cytokiner i immunsystemet. I studiet blev to moderne biologiske lægemidler testet: Adalimumab (en TNF-α-hæmmer) og Bimekizumab (en IL-17A/F-hæmmer). Disse blev tilføjet til vækstmediet under hudmodellen for at simulere en systemisk behandling (som en injektion).

Resultaterne var igen meget lig det, man ser i kliniske studier med patienter:
- Stærk anti-inflammatorisk virkning: Begge lægemidler reducerede effektivt produktionen af inflammatoriske signalstoffer. En kombination af de to viste sig at have en endnu stærkere, synergistisk effekt, der næsten normaliserede niveauerne af IL-6 og IL-8.
- Effekt på AMPs: Bimekizumab var særligt effektiv til at nedregulere de gener, der koder for antimikrobielle peptider som DEFB4A og S100A7. Adalimumab havde en mere begrænset effekt på disse, hvilket tyder på, at IL-17 er den primære drivkraft bag AMP-produktionen i keratinocytter.
- Begyndende strukturel forbedring: I modsætning til de topiske behandlinger viste de biologiske lægemidler tegn på at forbedre hudens struktur. Især Bimekizumab øgede produktionen af Keratin 10 (KRT10) og gener relateret til celle-til-celle-kontakter, hvilket er første skridt mod en stærkere hudbarriere.
Ligesom med de topiske behandlinger var den 6-dages behandlingsperiode dog for kort til fuldt ud at normalisere huden. Den forhøjede celledeling og de høje niveauer af S100A7-protein forblev, hvilket igen understreger, at disse er 'langsomt reagerende' markører for sygdommen. Dette stemmer overens med patientdata, hvor det ofte tager 12 uger eller mere med biologisk behandling, før huden er fuldstændig helet.
Hvorfor er disse modeller en revolution for fremtiden?
Brugen af 3D-psoriasismodeller repræsenterer et kvantespring inden for dermatologisk forskning. De bygger bro mellem simple cellekulturer og komplekse, dyre og tidskrævende kliniske studier i mennesker. Fordelene er mange:
- Menneskelig relevans: Modellerne er bygget af humane celler, hvilket giver mere pålidelige data om, hvordan et lægemiddel vil virke i mennesker, sammenlignet med dyremodeller.
- Reduktion af dyreforsøg: Ved at muliggøre screening af lægemidler i et tidligt stadie kan disse modeller markant reducere antallet af nødvendige dyreforsøg.
- Hastighed og effektivitet: Forskere kan teste dusinvis af stoffer og koncentrationer på relativt kort tid, hvilket accelererer udviklingsprocessen for nye lægemidler.
- Dybdegående indsigt: Modellerne giver mulighed for at studere de molekylære mekanismer bag både sygdommen og behandlingen i detaljer, som ikke altid er mulige at undersøge direkte i patienter.
Selvom modellerne har begrænsninger – de inkluderer eksempelvis ikke immunceller fra blodet, som også spiller en afgørende rolle in vivo – har de vist sig at være et utroligt værdifuldt værktøj. De kan forudsige anti-inflammatoriske effekter, belyse lægemidlers virkningsmekanismer og efterligne den tidsafhængige helingsproces, man ser hos patienter. De er et klart bevis på, at fremtidens medicin udvikles ved at bringe patientens biologi ind i laboratoriet.
Ofte Stillede Spørgsmål (FAQ)
Er disse 3D-hudmodeller lavet af rigtig menneskehud?
Nej, de er ikke transplanteret hud. De er bygget fra bunden i et laboratorium ved hjælp af primære humane hudceller (keratinocytter og fibroblaster), som dyrkes til at danne en flerlaget struktur, der efterligner rigtig hud.
Kan disse modeller helt erstatte dyreforsøg?
De kan ikke erstatte alle dyreforsøg endnu, især ikke når det kommer til at forstå et lægemiddels effekt på hele kroppen. Men de er et kraftfuldt værktøj inden for de 3 R'er (Replacement, Reduction, Refinement) og kan markant reducere behovet for dyreforsøg, især i de tidlige faser af lægemiddeludvikling og til test af hudirritation.
Hvorfor tager det længere tid at se fuld effekt i en patient end i modellen?
Modellen afspejler faktisk denne tidsforskel. Selvom inflammationen i modellen kan dæmpes på få dage, viser den også, at dybere strukturelle problemer som overdreven cellevækst og en ødelagt hudbarriere tager meget længere tid at reparere. Dette stemmer overens med klinisk erfaring, hvor patienter ofte har brug for uger eller måneders behandling for at opnå fuldstændig heling af huden.
Hvad er den største fordel ved at bruge disse modeller frem for almindelige cellekulturer?
Den tredimensionelle struktur og tilstedeværelsen af et differentieret ydre lag (stratum corneum) gør, at 3D-modellen opfører sig meget mere som rigtig hud. Den har en barrierefunktion, cellerne kommunikerer med hinanden i lag, og den kan modstå højere koncentrationer af stoffer, ligesom in vivo hud. Dette giver langt mere realistiske og pålidelige resultater end flade 2D-cellekulturer.
Hvis du vil læse andre artikler, der ligner 3D Hudmodeller: Fremtiden for Psoriasisforskning, kan du besøge kategorien Sundhed.
