12/11/2017
I den komplekse verden af menneskelig biologi findes der mikroskopiske budbringere, der konstant rejser mellem vores celler. Disse budbringere, kendt som ekstracellulære vesikler (EVs), er små, membranindpakkede partikler frigivet af næsten alle celletyper. Engang betragtet som cellulært affald, ved vi nu, at de spiller en afgørende rolle i intercellulær kommunikation ved at transportere proteiner, lipider og nukleinsyrer. Denne utrolige funktion har åbnet døren for en revolution inden for moderne medicin, hvor EVs undersøges som nøglen til tidlig sygdomsdiagnose, målrettet behandling og regenerativ medicin. Denne artikel vil udforske den fascinerende verden af EVs, fra deres grundlæggende biologi til deres banebrydende anvendelser, der former fremtiden for sundhedspleje.
Hvad er Ekstracellulære Vesikler (EVs)?
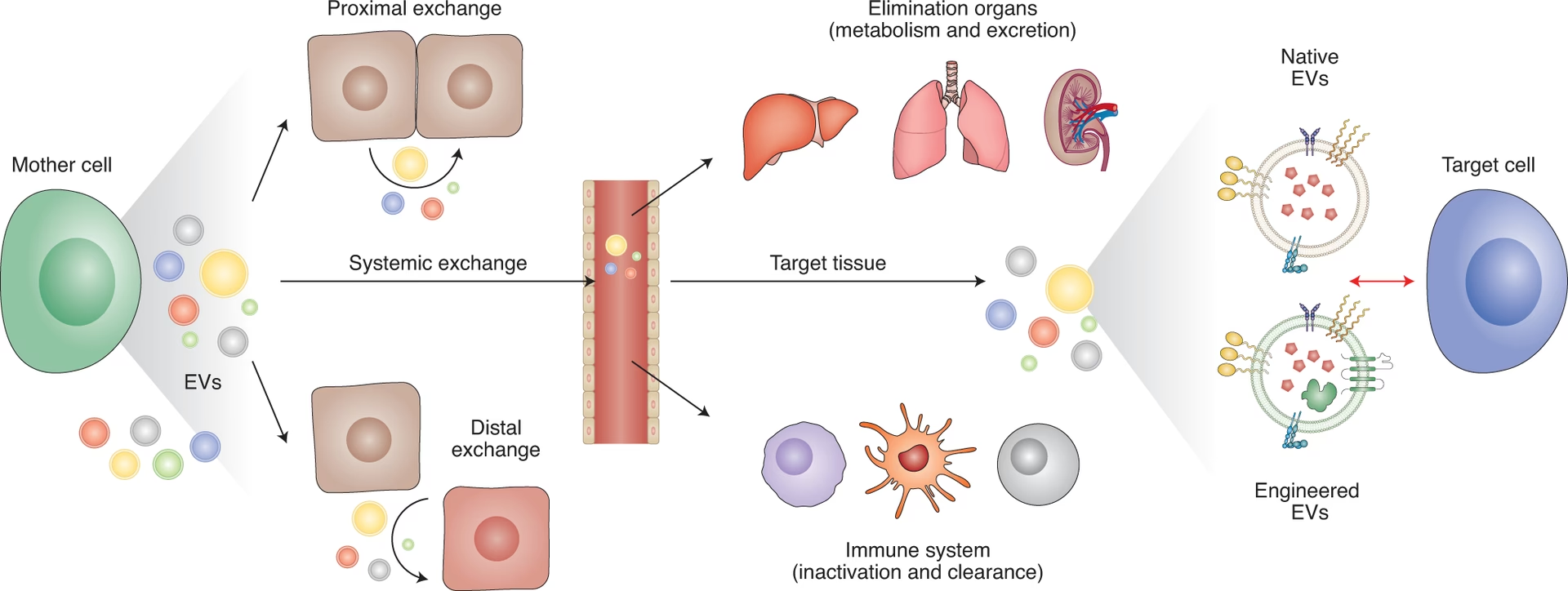
Ekstracellulære vesikler er en bred betegnelse for partikler i nanostørrelse, der naturligt frigives fra en celle og er omgivet af en dobbeltlaget lipidmembran. Deres primære funktion er at fungere som et transportsystem mellem celler, hvor de leverer deres molekylære last og derved påvirker modtagercellens adfærd og funktion. Denne evne gør dem til centrale aktører i utallige biologiske processer, både i sundhed og sygdom. For at forstå deres fulde potentiale er det vigtigt at kende til de forskellige typer, hvordan de dannes, og hvad de indeholder.
Typer af Ekstracellulære Vesikler
EVs er ikke en ensartet gruppe. De klassificeres primært i tre hovedtyper baseret på deres oprindelse, størrelse og dannelsesmekanisme. Hver type har unikke egenskaber og funktioner.
- Exosomer: De mindste af vesiklerne, typisk med en diameter på 30-150 nanometer. De dannes inde i cellen i en struktur kaldet et multivesikulært legeme (MVB). Når MVB'et fusionerer med cellemembranen, frigives exosomerne til det ekstracellulære rum. De er særligt vigtige for præcis signalering mellem celler.
- Mikrovesikler (eller Ektosomer): Disse er større, med en diameter fra 100 til 1.000 nanometer. I modsætning til exosomer dannes de ved direkte udposning og afsnøring fra cellemembranen. De er involveret i overførsel af membranproteiner og lipider.
- Apoptotiske legemer: De største vesikler, der varierer fra 1.000 til 5.000 nanometer. De frigives, når en celle gennemgår programmeret celledød (apoptose) og indeholder rester af cellen, såsom DNA-fragmenter og organeller.
Sammenligning af EV-typer
| Egenskab | Exosomer | Mikrovesikler | Apoptotiske legemer |
|---|---|---|---|
| Størrelse (diameter) | 30-150 nm | 100-1000 nm | 1000-5000 nm |
| Oprindelse | Endosomal (indefra cellen) | Direkte knopskydning fra cellemembranen | Fragmentering af en døende celle |
| Primær funktion | Finjusteret cellesignalering | Overførsel af membran-komponenter | Fjernelse af cellulære rester |
Molekylær Sammensætning: Vesiklernes Værdifulde Last
Den sande kraft i EVs ligger i deres last. De er som små pakker fyldt med bioaktive molekyler, der afspejler den celle, de kom fra. Denne last kan omfatte:
- Proteiner: Membranproteiner, enzymer og signalmolekyler, der kan igangsætte processer i modtagercellen.
- Lipider: Specifikke lipider som kolesterol og ceramid, der ikke kun udgør vesiklens struktur, men også kan deltage i signalering.
- Nukleinsyrer: Forskellige former for RNA, såsom messenger RNA (mRNA) og mikroRNA (miRNA), som kan ændre genekspressionen i modtagercellen. Der er også fundet DNA-fragmenter i EVs.
Denne rige molekylære sammensætning gør EVs til potente regulatorer af cellulær adfærd og giver forskere et vindue ind i cellens helbredstilstand.
EVs' Dobbeltrolle i Kræft
Inden for onkologi er EVs et tveægget sværd. På den ene side spiller de en afgørende rolle i udviklingen og spredningen af kræft, men på den anden side tilbyder de enestående muligheder for diagnose og behandling.
Hvordan Kræftceller Udnytter EVs
Kræftceller er mestre i at manipulere deres omgivelser, og de bruger EVs som et centralt værktøj. Tumor-afledte EVs kan:
- Fremme tumorvækst: Ved at sende vækstfaktorer til naboceller.
- Skabe et gunstigt mikromiljø: De kan omdanne normale celler til at understøtte tumoren, f.eks. ved at stimulere dannelsen af nye blodkar (angiogenese).
- Undgå immunsystemet: EVs kan bære proteiner som PD-L1 på deres overflade, som undertrykker T-celler og lader kræften undslippe immunforsvaret.
- Mediere metastase: De kan forberede fjerne organer på ankomsten af kræftceller og dermed skabe en "niche" for metastaser.
- Skabe kemoresistens: EVs kan overføre molekyler mellem kræftceller, der gør dem modstandsdygtige over for kemoterapi.
EVs som Værktøj mod Kræft
På trods af deres mørke side i kræftbiologi, er forskere ved at vende EVs' egenskaber til en fordel.
- Diagnostiske Biomarkører: Da EVs cirkulerer i kropsvæsker som blod og urin, kan de isoleres og analyseres. Deres indhold afspejler tumorens tilstedeværelse og karakteristika. Dette åbner for "flydende biopsier", en ikke-invasiv metode til at opdage kræft tidligt, overvåge behandlingsrespons og identificere mutationer. kommercielt tilgængelige tests, som ExoDx Prostate, bruger allerede EV-baseret mRNA-analyse til tidlig opsporing af prostatakræft.
- Målrettet Lægemiddellevering: EVs' naturlige evne til at levere last til specifikke celler gør dem til ideelle transportkøretøjer for kræftmedicin. Ved at fylde EVs med kemoterapi og modificere deres overflade til at genkende kræftceller, kan man opnå en mere præcis lægemiddellevering, der øger effektiviteten og reducerer bivirkninger.
EVs og Neurodegenerative Sygdomme
Hjernen er et andet område, hvor EVs spiller en afgørende rolle, både i sygdomsprogression og som et potentielt terapeutisk værktøj. Deres evne til at krydse blod-hjerne-barrieren gør dem særligt interessante.
- Alzheimers Sygdom: EVs menes at bidrage til spredningen af de giftige proteiner amyloid-beta og tau i hjernen, hvilket er kendetegnende for sygdommen. Ved at transportere disse proteiner fra celle til celle kan de accelerere den neurodegenerative proces.
- Parkinsons Sygdom: Ligeledes kan EVs transportere proteinet α-synuclein, hvis ophobning fører til dannelsen af Lewy-legemer og tab af dopamin-producerende neuroner.
Forskere arbejder på strategier til at blokere denne spredning. Samtidig undersøges muligheden for at bruge specialdesignede EVs til at levere terapeutiske midler direkte til de berørte hjerneområder, hvilket potentielt kan bremse eller stoppe sygdomsudviklingen.
Fremstilling og Modificering af EVs til Terapi
For at EVs kan blive en standardbehandling, kræves der robuste metoder til at producere, isolere og modificere dem i stor skala. Dette er et hurtigt voksende felt inden for bioteknologi.
Isolering og Rensning
At adskille de bittesmå EVs fra komplekse biologiske væsker er en stor udfordring. Flere teknikker anvendes, hver med sine fordele og ulemper.

| Metode | Fordele | Ulemper |
|---|---|---|
| Differential Ultracentrifugering | Guldstandard, kan håndtere store volumener. | Tidskrævende, kan beskadige vesikler, lav renhed. |
| Størrelseseksklusionskromatografi (SEC) | Skånsom, høj renhed og reproducerbarhed. | Begrænset prøvevolumen, kræver specialudstyr. |
| Polymer-baseret Præcipitation | Enkel, hurtig, intet specialudstyr nødvendigt. | Lavere renhed, med-udfælder forurenende stoffer. |
| Mikrofluidik | Høj præcision, hurtig, kan integreres med analyse. | Svær at skalere op, komplekst at udvikle. |
Engineering af EVs for Præcisionsmedicin
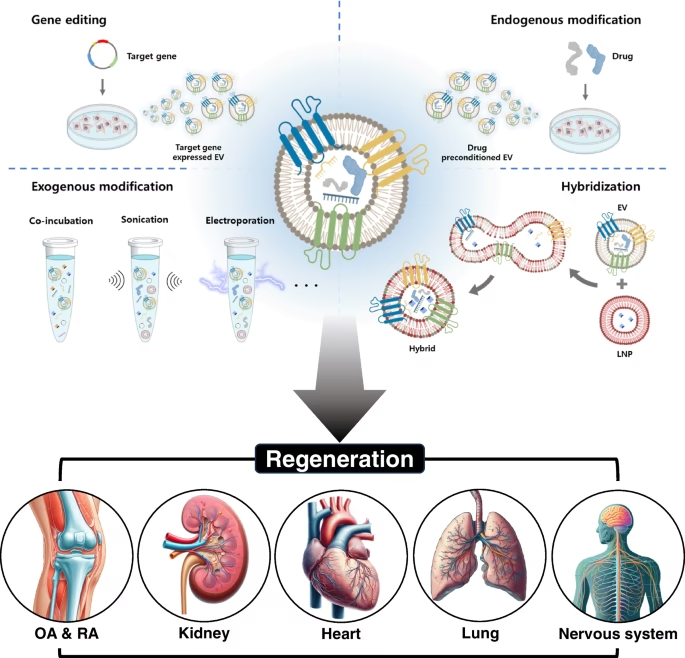
For at maksimere det terapeutiske potentiale kan EVs "designes" eller modificeres. Dette omfatter to hovedstrategier:
- Lastning af cargo (Post-loading): Efter isolering kan EVs fyldes med terapeutiske molekyler. Metoder som elektroporering (bruger elektriske impulser til at skabe midlertidige porer i membranen) og sonikering (bruger ultralyd) anvendes til at indføre lægemidler, siRNA eller proteiner i vesiklerne.
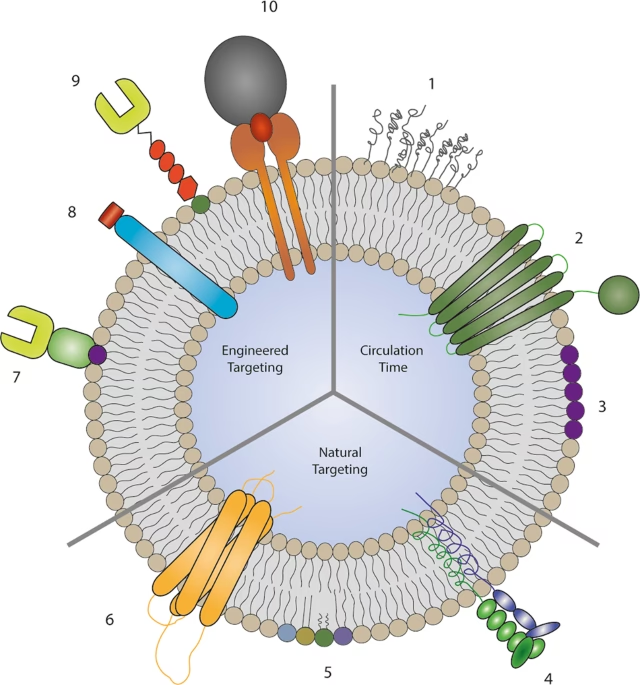
- Overflademodifikation: For at sikre, at EVs kun leverer deres last til de rigtige celler, kan deres overflade dekoreres med målrettede ligander, såsom antistoffer eller peptider, der genkender specifikke receptorer på målcellernes overflade.
Disse fremskridt driver udviklingen af personlig medicin, hvor behandlinger kan skræddersys til den enkelte patients sygdomsprofil.
Fremtiden for EV-forskning og Klinisk Anvendelse
Feltet for EV-forskning er i eksplosiv vækst, men der er stadig udfordringer, der skal overvindes, før EV-baserede terapier bliver almindelige. Standardisering af isolations- og karakteriseringsmetoder er afgørende for at sikre reproducerbare og pålidelige resultater. Desuden skal regulatoriske rammer, som dem fra FDA og EMA, udvikles for at sikre sikkerheden og effektiviteten af disse nye biologiske lægemidler. De mange igangværende kliniske forsøg verden over vidner om det enorme potentiale, og de kommende år vil sandsynligvis bringe de første EV-baserede lægemidler på markedet, hvilket vil markere en ny æra inden for medicin.
Ofte Stillede Spørgsmål (FAQ)
Hvad er de tre hovedtyper af ekstracellulære vesikler?
De tre primære typer er exosomer (de mindste, dannet internt), mikrovesikler (større, dannet fra cellemembranen) og apoptotiske legemer (de største, frigivet fra døende celler). De adskiller sig i størrelse, oprindelse og funktion.

Kan EVs bruges til tidlig sygdomsdetektion?
Ja, absolut. Fordi EVs findes i kropsvæsker som blod og bærer molekylære signaturer fra deres oprindelsescelle, er de ideelle biomarkører. Analyse af EVs kan afsløre tilstedeværelsen af sygdomme som kræft og neurodegenerative lidelser på et meget tidligt stadium gennem en simpel blod- eller urinprøve.
Hvordan bidrager EVs til kræftprogression?
EVs fra kræftceller kan fremme tumorvækst, hjælpe med at undgå immunsystemet, stimulere dannelsen af nye blodkar til tumoren, og forberede fjerne organer på metastase. De fungerer som kræftcellens budbringere for at manipulere omgivelserne til deres fordel.
Hvad er det terapeutiske potentiale i EVs?
EVs har et enormt terapeutisk potentiale, især som avancerede systemer til lægemiddellevering. De kan indkapsle og beskytte lægemidler, krydse biologiske barrierer som blod-hjerne-barrieren, og modificeres til at målrette specifikke syge celler, hvilket minimerer bivirkninger og øger behandlingens effektivitet.
Hvis du vil læse andre artikler, der ligner EVs: Små partikler, stort medicinsk potentiale, kan du besøge kategorien Medicin.
