13/02/2004
Acetoneperoxid, ofte forkortet TATP (triacetone triperoxid), er en kemisk forbindelse, der blev opdaget i 1895 af den tyske kemiker Richard Wolffenstein. Hans eksperiment, hvor han blandede acetone og hydrogenperoxid og lod det stå i en uge, resulterede i dannelsen af små krystaller. Hvad han måske ikke fuldt ud forstod på det tidspunkt, var den ekstreme fare, der lurede i disse krystaller. I dag er acetoneperoxid berygtet, ikke for sin kemiske nyskabelse, men for sin ekstreme ustabilitet og anvendelse som et potent, improviseret sprængstof. Denne artikel dykker ned i videnskaben bag acetoneperoxid for at belyse, hvorfor det er en så alvorlig trussel mod folkesundheden og sikkerheden.
Hvad er Acetoneperoxid? En Kemisk Tidsindstillet Bombe
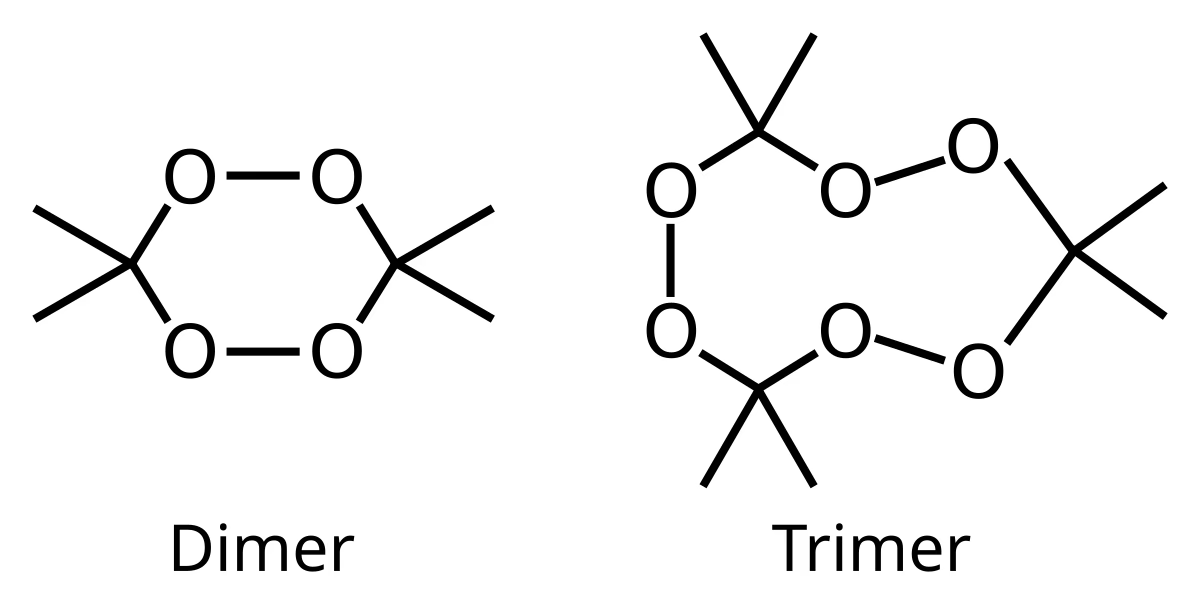
I sin kerne er acetoneperoxid et organisk peroxid. Det dannes gennem en syrekatalyseret nukleofil additionsreaktion mellem hydrogenperoxid og acetone – to kemikalier, der er relativt let tilgængelige. Selvom navnet oftest henviser til den cykliske trimer (TATP), kan reaktionen også producere andre former. Disse inkluderer en monomer og forskellige dimere former (både cykliske og åbne kæder). Den specifikke form, der dannes, afhænger stærkt af reaktionsbetingelserne, såsom koncentrationen af reagenser og den anvendte syrekatalysator. Under neutrale forhold dannes typisk den monomere form, mens den farlige trimer er det primære produkt under specifikke sure forhold.
Fra Dimer til Tetramer: De Forskellige Ansigter af Faren
Kompleksiteten af acetoneperoxid stopper ikke ved trimeren. Forskere har identificeret flere strukturer, hver med deres egne egenskaber:
- Monomer (C₃H₈O₄): En simpel, åben kædestruktur.
- Dimer (DADP): Findes i både en cyklisk (C₆H₁₂O₄) og en åben kædeform. Dimeren er også ustabil og har en højere damptryk end TATP, hvilket betyder, at den lettere fordamper.
- Trimer (TATP): Den mest kendte og studerede form. Dens cykliske struktur er notorisk ustabil.
- Tetramer: En endnu mere kompleks form, som er blevet beskrevet under særlige katalytiske forhold. Syntesen af denne tetramer form, som efter sigende er mere kemisk stabil, blev opnået under neutrale forhold ved hjælp af en tinkatalysator. Dog er dens eksistens og syntese genstand for videnskabelig debat og kontrovers. Selvom den hævdes at være mere stabil, er det afgørende at forstå, at den stadig klassificeres som et yderst farligt primært sprængstof.
Syntese og Ekstrem Ustabilitet: Hvorfor Det er Så Farligt
Fremstillingen af TATP er bedragerisk simpel, hvilket er en væsentlig del af faren. Den mest almindelige metode involverer at blande hydrogenperoxid, acetone og en stærk syre som saltsyre (HCl) eller svovlsyre (H₂SO₄). Valget af syre har dog dramatiske konsekvenser for produktets stabilitet. Krystaller fremstillet med svovlsyre er kendt for at være særligt farlige. Spor af svovlsyre kan blive fanget inde i krystalgitteret, hvilket gør det ekstremt ustabilt. Denne forurening kan forårsage spontan detonation ved temperaturer så lave som 50 °C, hvilket er en sandsynlig årsag til mange ulykker under tørringsprocessen.
En anden lumsk fare er sublimering. Både TATP og DADP har en tendens til at fordampe direkte fra fast form til gas og derefter aflejres igen som faste krystaller andre steder. Dette kan føre til, at farlige, følsomme krystaller vokser på gevindet af en beholder, hvilket kan forårsage en eksplosion, blot ved at man åbner låget. Denne proces kan også skabe større og mere ustabile krystaller over tid.
En Entropisk Eksplosion: Den Unikke Destruktive Kraft
Eksplosionen af TATP er anderledes end for mange traditionelle sprængstoffer. I stedet for en hurtig forbrændingsreaktion (oxidation), gennemgår TATP, hvad der er blevet beskrevet som en 'entropisk eksplosion'. Når det detonerer, nedbrydes et enkelt TATP-molekyle øjeblikkeligt til fire gasmolekyler (primært acetone og ozon). Denne pludselige og massive stigning i volumen (entropi) er den primære drivkraft bag eksplosionen. Selvom den indledende reaktion producerer lidt varme, fører de efterfølgende reaktioner mellem de dannede gasser til en enorm frigivelse af energi, med temperaturer, der når op på 2.300 K (over 2.000 °C) og et enormt tryk. Den samlede energi er nok til at gøre selv små mængder livsfarligt.
Sammenligningstabel: TATP vs. DADP
For at give et klarere billede af forskellene mellem de to mest almindelige former, er her en simpel sammenligning:
| Egenskab | TATP (Triacetone Triperoxid) | DADP (Diacetone Diperoxid) |
|---|---|---|
| Molekylær Form | Cyklisk Trimer (C₉H₁₈O₆) | Cyklisk Dimer (C₆H₁₂O₄) |
| Følsomhed | Ekstremt følsom over for stød, friktion og varme | Meget følsom, men generelt en smule mindre end TATP |
| Tendens til Sublimering | Moderat | Højere (på grund af lavere molekylvægt) |
| Gasvolumen ved Detonation | 855 L/kg | 713 L/kg |
Håndtering og Detektion: En Udfordring for Sikkerheden
På grund af den ekstreme fare er detektion af acetoneperoxid en høj prioritet for sikkerhedsmyndigheder. Der findes flere avancerede analysemetoder, herunder gaskromatografi/massespektrometri (GC/MS) og højtydende væskekromatografi/massespektrometri (HPLC/MS), til at identificere spormængder af stoffet. Håndtering af stoffet er forbeholdt højt specialiserede eksperter. Forsøg på at omkrystallisere acetoneperoxid for at opnå renere krystaller er utroligt risikabelt, da store krystaller kan udvikle interne spændinger og detonere spontant uden nogen åbenlys grund. Dette understreger endnu en gang, hvorfor dette stof aldrig må håndteres af andre end professionelle.
Ofte Stillede Spørgsmål (FAQ)
Er acetoneperoxid et lægemiddel eller har det medicinsk anvendelse?
Absolut ikke. Acetoneperoxid er et højeksplosivt og giftigt kemikalie uden nogen kendt medicinsk eller terapeutisk anvendelse. Det udgør udelukkende en alvorlig sundheds- og sikkerhedsrisiko.
Hvad gør acetoneperoxid så farligt?
Dets fare ligger i den ekstreme ustabilitet. Det er yderst følsomt over for varme, stød, friktion og statisk elektricitet. Selv små, utilsigtede påvirkninger kan udløse en voldsom detonation. Desuden kan det detonere spontant over tid eller ved let opvarmning.
Hvad er den tetramere form af acetoneperoxid?
Det er en teoretisk, mere kompleks molekylær struktur af acetoneperoxid. Selvom dens syntese er blevet beskrevet i videnskabelig litteratur som værende mere stabil, er dens eksistens og reproducerbarhed omstridt. Uanset hvad, betragtes den stadig som et farligt sprængstof.
Hvad skal jeg gøre, hvis jeg har mistanke om, at jeg er stødt på dette stof?
Rør det under ingen omstændigheder. Forlad området øjeblikkeligt og kontakt politiet på alarmnummeret. Forsøg aldrig selv at håndtere, flytte eller bortskaffe et mistænkeligt stof. Overlad det til professionelle sprængstofeksperter.
Hvis du vil læse andre artikler, der ligner Acetoneperoxid: En Dødelig og Skjult Fare, kan du besøge kategorien Sundhed.

