27/07/2015
Streptokokbakterier, især Streptococcus pneumoniae og Viridans-gruppen af streptokokker (VGS), er almindelige mikroorganismer, der findes i vores normale bakterieflora. Selvom de ofte er harmløse, kan de forårsage alvorlige og potentielt livstruende infektioner, især hos personer med svækket immunforsvar eller hjerteproblemer. I årtier har penicillin været et af de mest effektive våben mod disse bakterier. Men en voksende udfordring truer denne effektivitet: antibiotikaresistens. Flere og flere stammer udvikler mekanismer til at modstå penicillin, hvilket gør behandlingen af infektioner som infektiv endokarditis og neutropen feber markant mere kompliceret. Kernen i denne resistens ligger ofte i en fascinerende genetisk forandring i bakteriens egne proteiner.
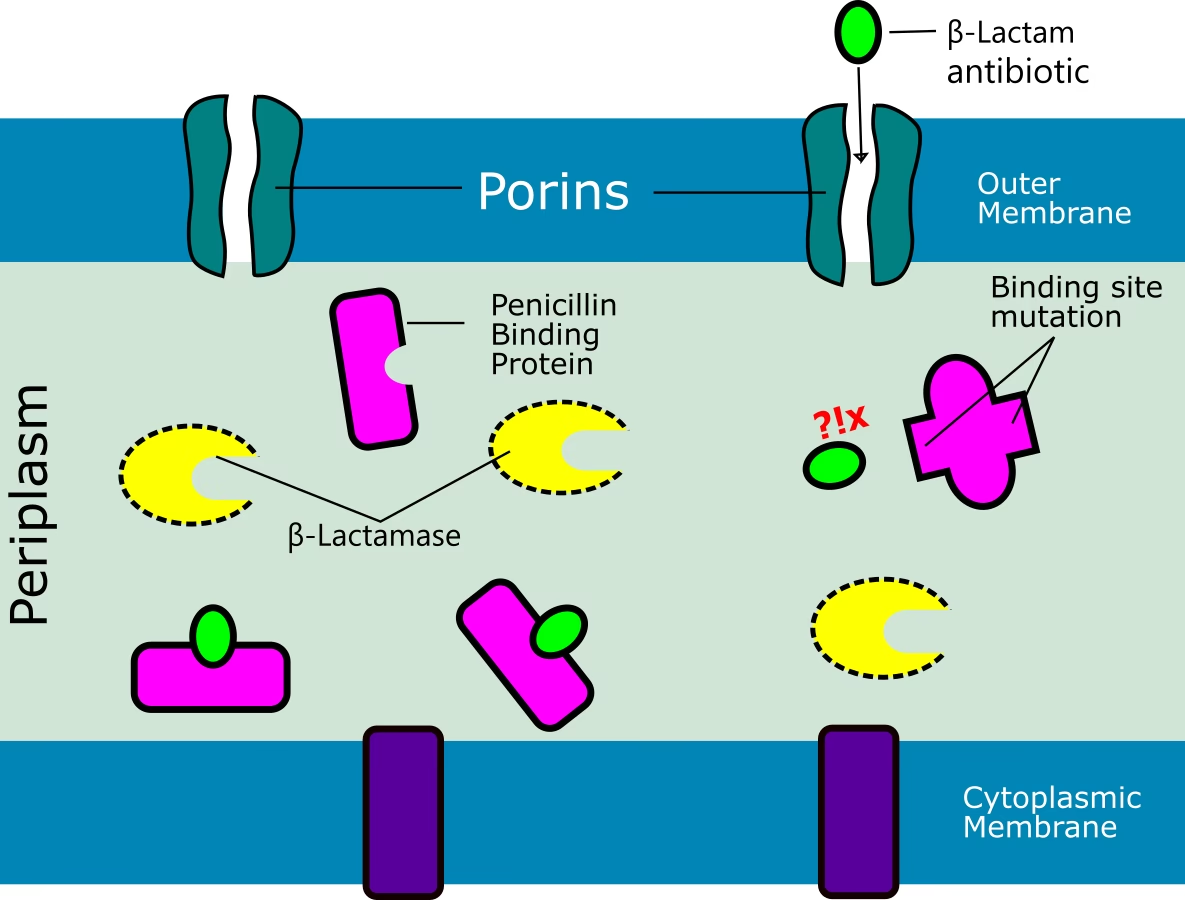
Forståelse af Penicillin og Dets Mål: PBP'er
For at forstå resistens må vi først forstå, hvordan penicillin virker. Penicillin tilhører en gruppe antibiotika kaldet beta-laktamer. Deres primære mål i bakterien er en gruppe enzymer kendt som penicillin-bindende proteiner (PBP'er). Disse proteiner spiller en afgørende rolle i opbygningen og vedligeholdelsen af bakteriens cellevæg, en stærk og beskyttende struktur, der er essentiel for bakteriens overlevelse. Når penicillin binder sig til disse PBP'er, deaktiveres de. Uden funktionelle PBP'er kan bakterien ikke opretholde sin cellevæg, hvilket fører til, at den bliver svag, brister og dør. Denne mekanisme har gjort penicillin til en hjørnesten i behandlingen af bakterielle infektioner i næsten et århundrede.
Den Genetiske Nøgle til Resistens: Ændrede PBP-gener
Så hvordan lykkes det for Streptococcus pneumoniae og VGS at modstå et så effektivt antibiotikum? Svaret ligger i genetisk tilpasning. Den mest udbredte og klinisk signifikante mekanisme for penicillinresistens hos disse bakterier er ikke, at de ødelægger antibiotikummet, men at de ændrer selve målet. Gennem mutationer og genetisk rekombination ændrer bakterierne de PBP-gener, der koder for de penicillin-bindende proteiner.
Disse genetiske ændringer resulterer i produktionen af modificerede PBP'er med en ændret tredimensionel struktur. Denne nye struktur gør det meget sværere for penicillinmolekylet at binde sig effektivt til proteinet. Man kan forestille sig det som at ændre låsen (PBP'et), så den gamle nøgle (penicillin) ikke længere passer. Selvom antibiotikummet er til stede, kan de modificerede PBP'er fortsætte deres arbejde med at bygge cellevæggen, og bakterien overlever. Graden af resistens afhænger af, hvor omfattende ændringerne i PBP-generne er. Små ændringer kan føre til intermediær følsomhed, hvor der kræves højere doser penicillin, mens mere omfattende ændringer kan resultere i fuldstændig resistens, hvor penicillin er praktisk talt virkningsløst.
Kliniske Udfordringer: Behandling af Resistente Infektioner
Fremkomsten af penicillinresistente streptokokker har store konsekvenser for behandlingen af patienter. To alvorlige tilstande, hvor dette er særligt problematisk, er infektiv endokarditis og neutropen feber.
Infektiv Endokarditis
Infektiv endokarditis er en alvorlig infektion i hjertets indre hinder eller hjerteklapper, og VGS er en af de hyppigste årsager. Historisk set var behandlingen relativt ligetil med penicillin. Men med stigende resistens er læger nødt til at justere behandlingsstrategierne markant. Behandlingen afhænger nu kritisk af følsomhedstestning, der bestemmer bakteriens Minimum Inhibitory Concentration (MIC) – den laveste koncentration af et antibiotikum, der kan hæmme bakteriens vækst.

Neutropen Feber
Patienter med neutropeni, en tilstand med et unormalt lavt antal neutrofile granulocytter (en type hvide blodlegemer), er ekstremt sårbare over for infektioner. Dette ses ofte hos kræftpatienter, der modtager kemoterapi. VGS, som normalt er en del af mundhulens flora, kan trænge ind i blodbanen og forårsage alvorlig bakteriæmi (blodforgiftning). Penicillinresistens i disse tilfælde er en alvorlig komplikation, da patienternes immunforsvar er for svagt til at bekæmpe infektionen alene. Dette kræver hurtig og aggressiv behandling med bredspektrede antibiotika, ofte intravenøst, og nogle gange inkluderes vancomycin fra starten, hvis der er mistanke om en resistent stamme.
Behandlingsstrategier i en Æra med Resistens
Retningslinjer fra organisationer som American Heart Association (AHA) giver anbefalinger til behandling baseret på bakteriens følsomhed. Valget af antibiotika, dosis og behandlingsvarighed skal skræddersys nøje.
| Følsomhedsniveau (MIC for Penicillin) | Anbefalet Behandling | Varighed | Alternativer/Kommentarer |
|---|---|---|---|
| Højt følsom (≤0.12 mg/L) | Penicillin G eller Ceftriaxon | 4 uger | For ukomplicerede tilfælde kan en 2-ugers kur med gentamicin i kombination overvejes. Vancomycin ved alvorlig penicillinallergi. |
| Intermediært følsom (>0.12 til ≤0.5 mg/L) | Penicillin G eller Ceftriaxon + Gentamicin | 4 uger | Gentamicin gives typisk i de første 2 uger for at opnå en synergistisk, bakteriedræbende effekt. |
| Resistent (>0.5 mg/L) | Kombinationsbehandling, ofte med Vancomycin | 4-6 uger | Behandlingen er kompleks. Kombinationer kan inkludere et beta-laktam (som penicillin eller ampicillin) i høje doser plus gentamicin. Valg afhænger af specifikke følsomhedsdata. |
Selv med disse strategier er succes ikke garanteret. Der er rapporteret tilfælde, hvor selv kombinationer med vancomycin har fejlet i at udrydde infektionen, hvilket understreger behovet for nye behandlingsmuligheder og en omhyggelig tilgang til hver enkelt patient.
Fremtiden: Overvågning og Forebyggelse
Kampen mod antibiotikaresistens er en vedvarende proces. Kontinuerlig overvågning af resistensmønstre hos streptokokker er afgørende for at kunne opdatere behandlingsvejledninger og sikre, at læger har den bedst mulige information. Desuden er der en voksende bekymring for, at profylaktisk brug af antibiotika, f.eks. før tandlægeprocedurer hos risikopatienter, kan være med til at selektere for resistente stammer i den normale flora. Dette skaber et dilemma mellem at beskytte den enkelte patient mod en potentiel infektion og at bidrage til et større folkesundhedsproblem. Ansvarlig brug af antibiotika, udvikling af nye lægemidler og en dybere forståelse af resistensmekanismer er vores bedste forsvar i denne fortsatte kamp.
Ofte Stillede Spørgsmål
- Hvad er den primære årsag til, at streptokokker bliver resistente over for penicillin?
Den primære årsag er genetiske ændringer i de gener, der koder for bakteriens penicillin-bindende proteiner (PBP'er). Disse ændringer gør, at penicillin ikke længere kan binde sig effektivt til sit mål, og bakterien kan derfor overleve. - Er infektioner med penicillin-resistente streptokokker mere aggressive?
Ikke nødvendigvis. Bakterierne er ikke i sig selv mere aggressive, men infektionerne er markant sværere at behandle. Dette kan føre til længere sygdomsforløb, flere komplikationer, behov for mere giftige antibiotika og i sidste ende en højere dødelighed. - Hvilke andre antibiotika kan bruges, hvis penicillin ikke virker?
Valget afhænger af følsomhedstest. Almindelige alternativer omfatter ceftriaxon (et andet beta-laktam), vancomycin og i nogle tilfælde nyere midler som linezolid eller daptomycin. Ofte anvendes en kombination af flere antibiotika. - Hvorfor er det vigtigt at gennemføre en hel antibiotikakur?
Det er afgørende at tage hele den ordinerede kur for at sikre, at alle de sygdomsfremkaldende bakterier bliver udryddet. Hvis man stopper for tidligt, kan de mest modstandsdygtige bakterier overleve og formere sig, hvilket bidrager til udviklingen af resistens.
Hvis du vil læse andre artikler, der ligner Penicillinresistens: Streptokokkers Skjulte Våben, kan du besøge kategorien Sundhed.
