30/05/2004
Skizofreni er en kompleks og ofte misforstået psykisk lidelse, der påvirker millioner af mennesker verden over. I årtier har forskere arbejdet på at afdække dens rødder, og det har længe stået klart, at genetik spiller en afgørende rolle. Men hvordan identificerer man de specifikke gener ud af de tusindvis, vi alle bærer på? Svaret ligger i en kraftfuld teknologi kendt som genom-dækkende associationsstudier, eller GWAS. Disse studier har i de seneste to årtier transformeret vores viden om det genetiske grundlag for skizofreni og givet et hidtil uset indblik i sygdommens biologi.
Hvad er et Genom-Dækkende Associationsstudie (GWAS)?
For at forstå gennembruddet er det vigtigt først at forstå, hvad et GWAS er. Forestil dig det menneskelige genom som en enorm bog med milliarder af bogstaver. Et GWAS fungerer som en avanceret stavekontrol, der sammenligner "bogen" hos tusindvis af mennesker med en bestemt sygdom (i dette tilfælde skizofreni) med "bogen" hos tusindvis af raske kontrolpersoner. Formålet er at finde små "stavefejl" – eller mere præcist, genetiske varianter kaldet Single Nucleotide Polymorphisms (SNPs) – der optræder hyppigere hos personer med sygdommen.
Disse studier er "genom-dækkende", fordi de ikke fokuserer på et enkelt mistænkt gen, men scanner hele genomet på en upartisk måde. Ved at analysere hundredtusindvis eller endda millioner af SNPs på tværs af genomet kan forskere identificere specifikke kromosomale regioner, der er associeret med en øget risiko for at udvikle skizofreni. Det er en statistisk tung proces, der kræver enorme mængder data og computerkraft, men resultaterne har været banebrydende.
De Store Opdagelser: Skizofreniens Polygeniske Natur
De tidlige genetiske studier af skizofreni havde begrænset succes, primært på grund af for små stikprøvestørrelser. Men i takt med at teknologien blev billigere og internationale samarbejder voksede, eksploderede antallet af deltagere i GWAS-studier fra hundreder til hundredtusinder. Dette markerede et vendepunkt.
Den måske vigtigste opdagelse fra GWAS er, at skizofreni er en yderst polygenisk lidelse. Det betyder, at der ikke findes ét enkelt "skizofreni-gen". I stedet bidrager hundredvis, og sandsynligvis tusindvis, af forskellige genetiske varianter til en persons samlede risiko. Hver af disse varianter har kun en meget lille effekt i sig selv, men når de kombineres, kan de øge sårbarheden for at udvikle sygdommen betydeligt.

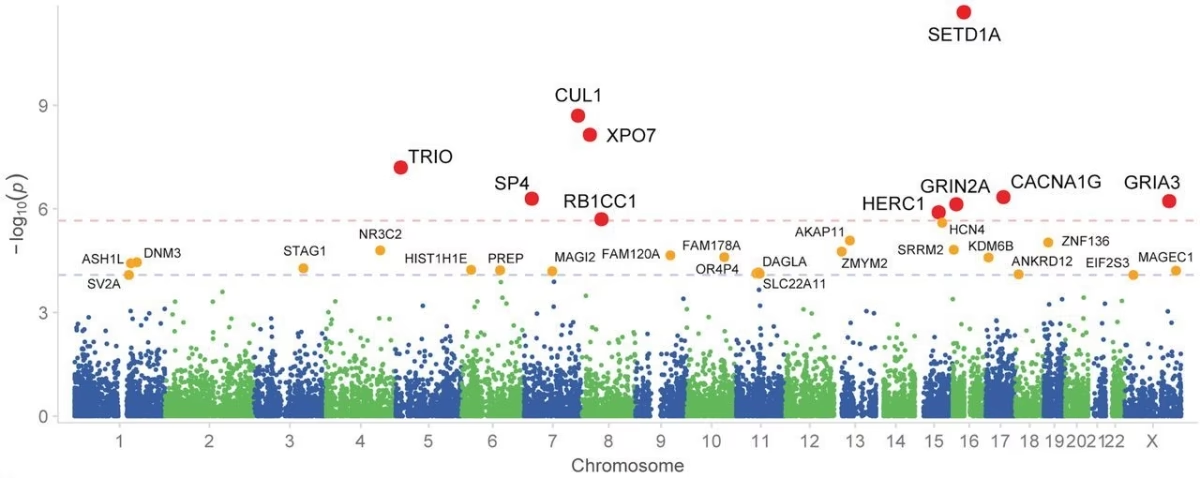
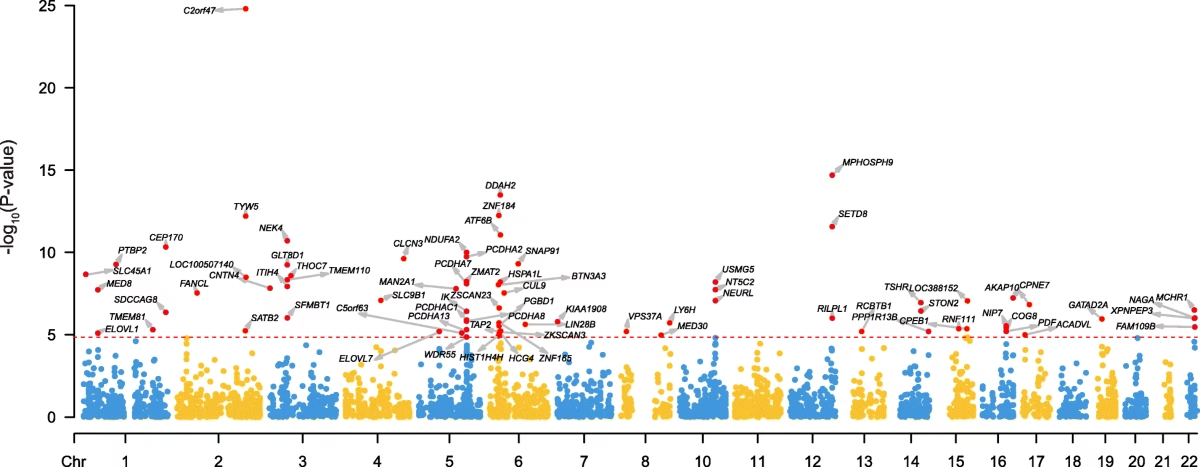
Til dato har forskning, anført af konsortier som Psychiatric Genomics Consortium (PGC), identificeret:
- Over 300 almindelige genetiske varianter (SNPs) associeret med skizofreni.
- 10 specifikke gener, hvor sjældne, mere skadelige mutationer er fundet.
- Mindst 8 kendte kopiantalsvariationer (CNVs), hvor større stykker af DNA enten mangler eller er duplikeret.
Disse fund har leveret det første solide, molekylære bevis for de biologiske processer, der er involveret i skizofreni, og har peget forskere i retning af specifikke cellulære mekanismer og signalveje i hjernen, som kan være mål for fremtidig medicin.
Fra Korrelation til Kausalitet: Udfordringer og Næste Skridt
Selvom GWAS har været en enorm succes, er det vigtigt at forstå studiets begrænsninger. Et GWAS kan identificere en statistisk association mellem en genetisk variant og en sygdom, men det beviser ikke, at varianten er den direkte årsag. Ofte ligger de identificerede SNPs i områder af genomet, der ikke koder for proteiner, men som i stedet regulerer andre geners aktivitet. Det store arbejde, der følger efter et GWAS, er derfor funktionelle studier: at forstå præcis, hvordan disse varianter påvirker genekspression og hjernefunktion.
Projekter som PsychENCODE, GTEx og CommonMind Consortium er afgørende i denne fase. De skaber detaljerede kort over, hvilke gener der er aktive i forskellige dele af hjernen og på forskellige stadier af udviklingen. Ved at kombinere GWAS-data med disse funktionelle kort kan forskere begynde at forbinde en risikovariant med et specifikt gen og en biologisk proces, hvilket bringer os tættere på at forstå sygdommens mekanismer.
Styrker og Svagheder ved GWAS i Skizofreniforskning
For at give et klart overblik er her en tabel, der opsummerer fordele og ulemper ved at bruge GWAS-metoden:
| Styrker | Svagheder |
|---|---|
| Upartisk scanning af hele genomet. | Kræver ekstremt store stikprøver for at opnå statistisk signifikans. |
| Har identificeret hundredvis af risikovarianter for skizofreni. | Viser association, ikke en direkte årsagssammenhæng. |
| Beviste den komplekse og polygeniske natur af sygdommen. | Har svært ved at opdage meget sjældne, men potentielt meget potente, varianter. |
| Skaber et solidt grundlag for videre biologisk og funktionel forskning. | Historisk mangel på etnisk diversitet i studiepopulationer. |
Fremtidsperspektiver: Øget Diversitet og Personlig Medicin
En af de mest presserende udfordringer for genetisk forskning i dag er den manglende diversitet. I 2019 var hele 79% af alle deltagere i GWAS-studier (på tværs af alle sygdomme) af europæisk afstamning. Selvom de seneste skizofreni-studier har forbedret dette tal en smule, er der stadig en markant skævhed. Dette er et alvorligt problem af to årsager. For det første betyder det, at de kliniske fordele, der kan opstå fra forskningen, muligvis ikke er gældende for alle befolkningsgrupper. For det andet kan studier af diverse populationer øge den statistiske kraft til at finde nye gener og hjælpe med at indsnævre de præcise kausale varianter.

Fremtiden for skizofrenigenetik vil derfor fokusere på:
- Større og mere diverse stikprøver: Inkludering af flere individer fra afrikanske, asiatiske og andre ikke-europæiske befolkninger er afgørende.
- Sjældne varianter: I takt med at prisen på helgenomsekventering falder, vil større studier kunne fokusere på sjældne varianter, som kan have en stærkere effekt på sygdomsrisiko.
- Gen-miljø interaktion: Forskning vil i stigende grad undersøge, hvordan genetisk sårbarhed interagerer med miljømæssige faktorer som stress, infektioner eller traumer for at udløse sygdommen.
- Lægemiddeludvikling og personlig medicin: Det ultimative mål er at omsætte den genetiske viden til nye behandlinger. Ved at forstå de specifikke biologiske veje, der er påvirket, kan forskere udvikle mere målrettet medicin. På sigt kan personlig medicin, hvor behandlingen skræddersys til en persons genetiske profil, blive en realitet.
Ofte Stillede Spørgsmål (OSS)
Kan GWAS forudsige, om jeg vil udvikle skizofreni?
Nej, ikke på et individuelt plan. GWAS identificerer risikofaktorer på tværs af populationer, men den individuelle risiko fra hver enkelt genetisk variant er ekstremt lille. En høj polygenisk risikoscore betyder en statistisk øget sårbarhed, men det er på ingen måde en diagnose eller en garanti for, at man vil udvikle sygdommen. Miljømæssige og andre faktorer spiller også en stor rolle.
Hvad er den største opdagelse fra GWAS om skizofreni?
Den vigtigste opdagelse er den utvetydige bekræftelse af, at skizofreni er en yderst polygenisk lidelse. Dette har flyttet fokus væk fra jagten på et enkelt "skizofreni-gen" og mod en mere kompleks forståelse af, hvordan tusindvis af genetiske bidrag tilsammen skaber en sårbarhed i hjernens udvikling og funktion.
Hvorfor er det så vigtigt at inkludere flere ikke-europæiske befolkninger?
Det er vigtigt for både retfærdighed og videnskabelig fremgang. For det første sikrer det, at de medicinske fremskridt, der kommer ud af forskningen, kan gavne alle mennesker, uanset deres herkomst. For det andet har forskellige populationer forskellige mønstre af genetisk variation, hvilket kan give forskerne nye ledetråde og øge styrken til at finde gener, der er svære at identificere i en enkelt population.
Konklusion
Rejsen ind i skizofreniens genetik har været lang og kompleks, men takket være GWAS står vi i dag med en langt dybere forståelse end nogensinde før. Vi ved nu, at skizofreni er en sygdom med et solidt biologisk fundament, rodfæstet i en kompleks arkitektur af tusindvis af genetiske varianter. Selvom vejen fra genetisk opdagelse til klinisk anvendelse stadig er lang, har GWAS lagt et uundværligt fundament. Fremtidig forskning, der bygger på større, mere diverse datasæt og avancerede funktionelle studier, bærer løftet om ikke kun at afkode sygdommens mysterier fuldt ud, men også at bane vejen for nye, mere effektive behandlinger og en bedre fremtid for dem, der lever med skizofreni.
Hvis du vil læse andre artikler, der ligner Afkodning af Skizofreni med GWAS-Studier, kan du besøge kategorien Sundhed.