02/01/2022
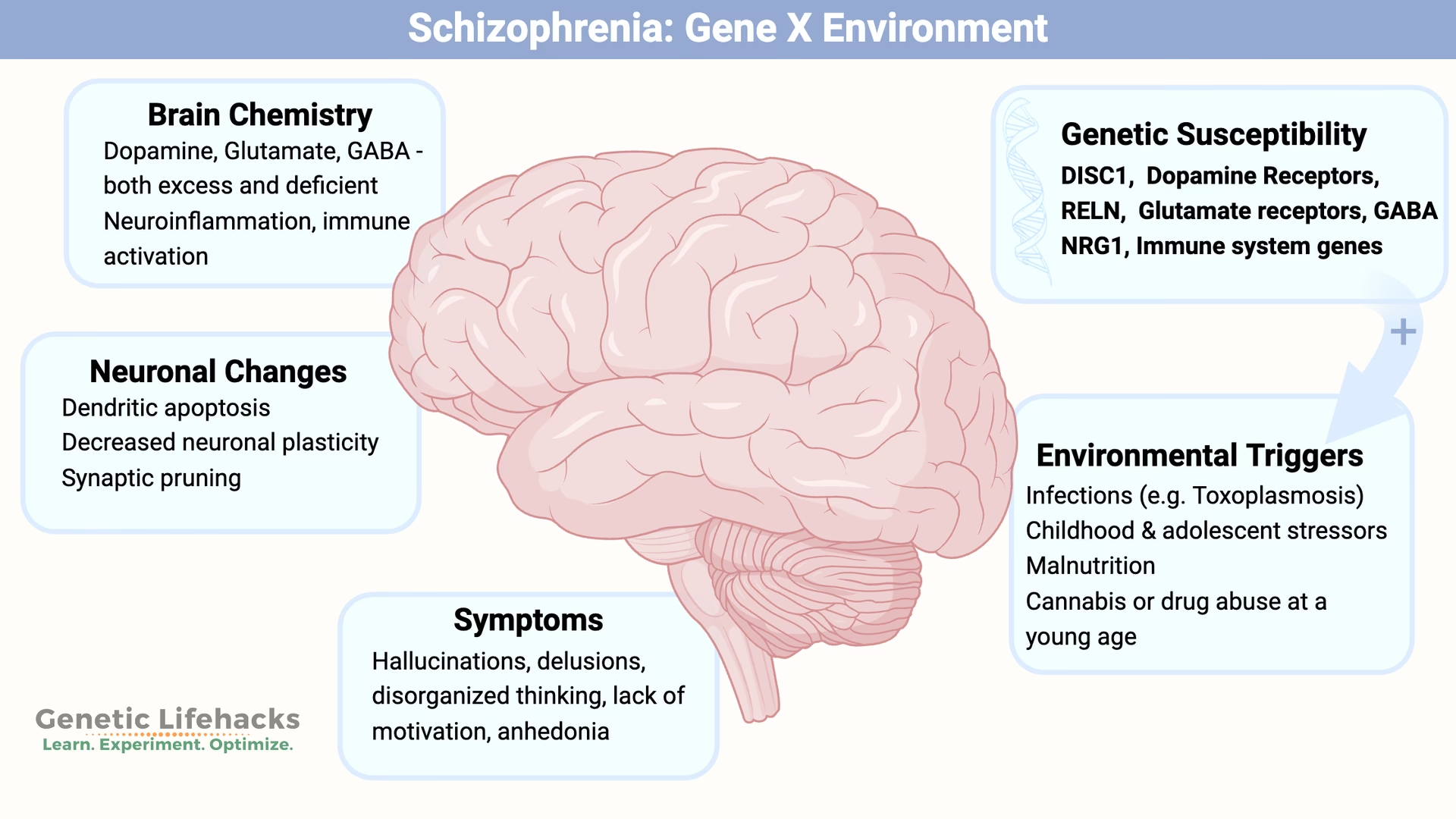
Skizofreni er en dybtgående og ofte invaliderende psykisk lidelse, der påvirker en persons tanker, følelser og adfærd. Den er kendetegnet ved en række symptomer, der kan opdeles i 'positive' symptomer som hallucinationer og vrangforestillinger, og 'negative' symptomer som følelsesmæssig affladning, manglende motivation og social isolation. I årtier har forskere og læger kæmpet for at forstå de underliggende årsager til denne komplekse sygdom. Selvom miljømæssige faktorer spiller en rolle, peger en overvældende mængde beviser i én bestemt retning: genetik. Faktisk anslås arveligheden for skizofreni til at være omkring 80%, hvilket gør det til en af de mest arvelige psykiatriske lidelser. Men at sige, at skizofreni er genetisk, er kun begyndelsen på en langt mere kompliceret historie. Der findes ikke ét enkelt 'skizofreni-gen'. I stedet er det et komplekst samspil af hundredvis, måske tusindvis, af genetiske variationer, der hver især bidrager med en lille smule til den samlede risiko. Denne artikel vil udforske rejsen ind i skizofreniens genetiske landskab, fra de tidligste tvillingestudier til de mest avancerede genomiske teknologier som GWAS.
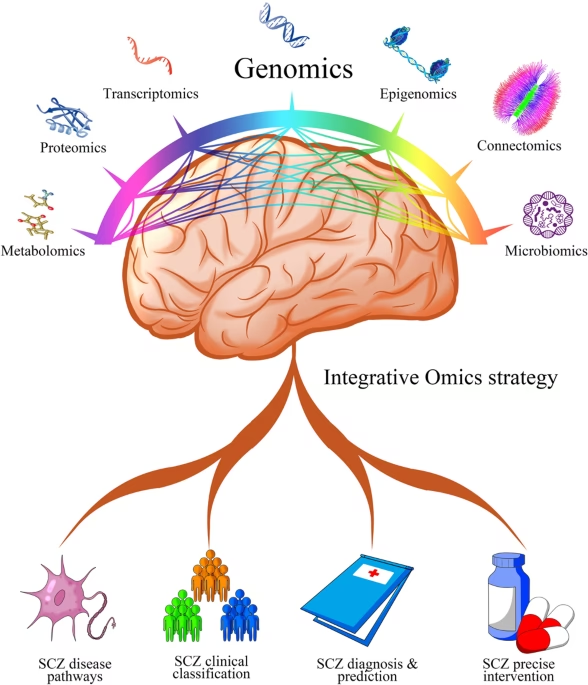
Tvillingestudier: De Første Afgørende Spor
De første solide beviser for en stærk genetisk komponent i skizofreni kom fra tvillinge- og adoptionsstudier. Logikken er enkel: enæggede (monozygote) tvillinger deler 100% af deres gener, mens tveæggede (dizygote) tvillinger, ligesom almindelige søskende, deler omkring 50%. Hvis en sygdom er rent genetisk, burde enæggede tvillinger altid have den samme status – enten er begge syge, eller begge er raske. For skizofreni er billedet ikke helt så enkelt, men resultaterne er alligevel slående. Studier viser, at hvis den ene enæggede tvilling har skizofreni, er risikoen for den anden tvilling helt op til 50%. For tveæggede tvillinger er risikoen betydeligt lavere, omkring 9-17%, hvilket stadig er markant højere end de 0.5-1% i den generelle befolkning.
Disse tal bekræfter en stærk genetisk indflydelse, men de 50% hos enæggede tvillinger fortæller os også noget andet vigtigt: gener er ikke hele historien. Hvis det var rent genetisk, ville tallet være 100%. Dette 'hul' peger på betydningen af ikke-genetiske faktorer, herunder miljøpåvirkninger. En fascinerende, men ofte overset faktor, er det prænatale miljø. De fleste tror, at enæggede tvillinger deler alt i livmoderen, men det er ikke altid tilfældet. Afhængigt af hvornår ægget deler sig, kan tvillingerne udvikle sig med hver deres moderkage (dichorioniske) eller dele en enkelt (monochorioniske). Tvillinger, der deler en moderkage, deler også blodcirkulation mere direkte, hvilket betyder, at de er mere udsatte for de samme prænatale påvirkninger, såsom infektioner eller stress hos moderen. Nogle studier antyder, at monochorioniske tvillinger har en højere konkordansrate (sandsynlighed for at begge får sygdommen) for skizofreni, hvilket understreger, at selv det tidligste miljø spiller en afgørende rolle i samspil med generne.
Jagten på Generne: Fra Kandidater til Hele Genomet
Med den voksende erkendelse af genetikkens betydning begyndte forskere en målrettet jagt på specifikke gener, der kunne være involveret. De tidlige tilgange, kendt som 'kandidatgenstudier', fokuserede på gener, man allerede mistænkte for at have en relevans for hjernens funktion, især dem relateret til neurotransmittere som dopamin og glutamat. Gener som COMT, DRD2 og DISC1 blev grundigt undersøgt. Selvom disse studier gav vigtig indsigt, var resultaterne ofte inkonsistente og svære at reproducere. Det blev hurtigt klart, at man ledte efter en nål i en høstak, og at den traditionelle tilgang var for snæver. Skizofreniens genetiske arkitektur var langt mere kompleks end blot en håndfuld gener med stor effekt.
GWAS: Et Kvantumspring i Genetisk Forskning
Den helt store revolution inden for skizofrenigenetik kom med udviklingen af Genom-dækkende associationsstudier, bedre kendt som GWAS. I stedet for at fokusere på få mistænkte gener, gør GWAS-teknologien det muligt at scanne en persons samlede arvemasse for millioner af små genetiske variationer på én gang. Den mest almindelige type variation, som GWAS undersøger, kaldes Enkeltnukleotidpolymorfier eller SNP'er (udtales 'snips').
En SNP er i bund og grund en enkelt 'stavefejl' i DNA-koden, hvor ét bogstav (en nukleotidbase) er udskiftet med et andet. Disse variationer er ekstremt almindelige og findes i millionvis i vores genomer. De fleste SNP'er har ingen effekt, men nogle kan subtilt påvirke, hvordan et gen fungerer, og dermed øge eller mindske risikoen for en sygdom.
Ved at sammenligne genomerne fra titusindvis af personer med skizofreni med genomerne fra en lige så stor kontrolgruppe af raske individer, kan forskere identificere SNP'er, der er statistisk mere almindelige hos dem med sygdommen. Resultaterne fra store internationale konsortier som Psychiatric Genomics Consortium (PGC) har været banebrydende. De har identificeret over 100 specifikke steder (loci) i genomet, der er robust associeret med skizofreni. Dette bekræfter, at skizofreni er en yderst polygen lidelse – det vil sige, at risikoen er et resultat af den samlede effekt af mange, mange genetiske varianter, hvor hver enkelt kun bidrager med en meget lille risiko. Det er som at bygge en mur, hvor hver SNP er en lille sten; ingen enkelt sten er afgørende, men tilsammen skaber de en solid struktur.
CNV'er: Sjældne Varianter med Stor Indflydelse
Mens GWAS har været en enorm succes i at finde almindelige varianter med lille effekt, har forskningen også afdækket en anden type genetisk variation, der spiller en vigtig rolle: Kopitalvariationer eller CNV'er. I modsætning til en SNP, som er en lille ændring, er en CNV en meget større strukturel ændring, hvor et helt segment af DNA er enten slettet (deletion) eller fordoblet (duplikation). Man kan tænke på en SNP som en enkelt stavefejl i en bog, mens en CNV er som en hel side, der er revet ud eller kopieret ind en ekstra gang.
Disse CNV'er er meget sjældnere end SNP'er, men deres effekt er ofte langt større. En enkelt sjælden CNV kan øge en persons risiko for skizofreni markant. Det mest kendte eksempel er en deletion på kromosom 22, specifikt i regionen 22q11.2. Mennesker med denne deletion har en 20-30% risiko for at udvikle skizofreni, hvilket er en enorm stigning i forhold til den generelle befolkning. Andre CNV'er, der påvirker gener som NRXN1 og CHRNA7, som er vigtige for synapsernes funktion i hjernen, er også blevet stærkt forbundet med sygdommen. Disse fund viser, at mens den generelle risiko i befolkningen primært drives af tusindvis af almindelige SNP'er, kan nogle individuelle tilfælde af skizofreni forklares af en enkelt, kraftfuld, men sjælden genetisk begivenhed.
Sammenligning af SNP'er og CNV'er i Skizofreni
| Egenskab | SNP (Enkeltnukleotidpolymorfi) | CNV (Kopitalvariation) |
|---|---|---|
| Hyppighed i befolkningen | Meget almindelig | Sjælden |
| Genetisk størrelse | Ét enkelt DNA-bogstav (basepar) | Store DNA-segmenter (tusinder til millioner af basepar) |
| Effekt på risiko | Meget lille for hver enkelt variant | Ofte stor og med høj penetrans (stor sandsynlighed for sygdom) |
| Bidrag til sygdomsbyrden | Den samlede effekt af mange SNP'er forklarer en stor del af arveligheden i befolkningen | Forklarer en mindre, men betydelig, andel af tilfældene, ofte med alvorligere symptomer |
Konklusion: Et Komplekst Genetisk Puslespil
Forskningen i skizofreniens genetik har taget gigantiske skridt. Vi er gået fra at vide, at sygdommen er arvelig, til at kunne pege på hundredvis af specifikke genetiske regioner og varianter. Billedet, der tegner sig, er et af enorm kompleksitet. Der er ikke én årsag, men et sammensurium af genetiske sårbarheder. For de fleste mennesker med skizofreni er det den akkumulerede vægt af tusindvis af almindelige SNP'er, der tipper vægtskålen. For en mindre gruppe kan en enkelt, sjælden CNV være den primære genetiske drivkraft. Det er vigtigt at huske, at genetik ikke er skæbne. At have genetiske risikovarianter betyder ikke, at man med sikkerhed vil udvikle skizofreni. Miljømæssige faktorer – lige fra prænatale infektioner til stress og traumer senere i livet – spiller en afgørende rolle i at udløse sygdommen hos dem, der er genetisk sårbare. Den fortsatte forskning, herunder nye teknologier som fuldgenomsekventering, vil utvivlsomt afdække endnu flere brikker i dette komplekse puslespil. Hvert nyt fund bringer os tættere på at forstå de biologiske mekanismer bag skizofreni, hvilket er det afgørende første skridt mod at udvikle mere effektive, målrettede behandlinger og måske en dag endda forebyggelse.
Ofte Stillede Spørgsmål (FAQ)
Er skizofreni arveligt?
Ja, skizofreni er stærkt arveligt. Studier anslår, at omkring 80% af risikoen for at udvikle sygdommen kan tilskrives genetiske faktorer. Dette betyder dog ikke, at hvis en forælder har skizofreni, vil barnet med sikkerhed få det, men risikoen er markant forhøjet.
Hvad er en SNP, og hvordan relaterer det sig til skizofreni?
En SNP (Enkeltnukleotidpolymorfi) er en almindelig variation i en enkelt 'bogstav' i vores DNA-kode. Individuelt har hver SNP kun en meget lille effekt på risikoen for skizofreni. Men den samlede effekt af mange tusinde af disse små variationer kan udgøre en betydelig genetisk sårbarhed.
Hvad er GWAS?
GWAS (Genom-dækkende associationsstudie) er en forskningsmetode, hvor man scanner hele genomet hos tusindvis af mennesker for at finde genetiske variationer (som SNP'er), der er mere almindelige hos personer med en bestemt sygdom sammenlignet med en rask kontrolgruppe. Metoden har været afgørende for at identificere de mange gener, der er involveret i skizofreni.
Hvis jeg har risikogener for skizofreni, betyder det så, at jeg vil få sygdommen?
Nej, slet ikke nødvendigvis. At bære på genetiske risikovarianter er ikke en diagnose eller en dom. Det øger kun din statistiske risiko. Udviklingen af skizofreni er et komplekst samspil mellem genetisk sårbarhed og en række miljømæssige faktorer. Mange mennesker med en høj genetisk risiko udvikler aldrig sygdommen.
Hvis du vil læse andre artikler, der ligner Skizofreni: Genetikkens Rolle og Mysterier, kan du besøge kategorien Sundhed.