22/06/2025
Skizofreni er en alvorlig og invaliderende psykisk sygdom, der påvirker op til 1% af befolkningen globalt. Sygdommen manifesterer sig gennem tre hovedgrupper af symptomer: positive symptomer som hallucinationer og tankeforstyrrelser, negative symptomer som følelsesmæssig affladning og social tilbagetrækning, samt kognitive symptomer, der påvirker indlæring, opmærksomhed og hukommelse. På trods af dens udbredelse er den præcise årsag til skizofreni stadig ikke fuldt ud forstået, og de nuværende behandlinger med antipsykotika har betydelige begrænsninger. Disse lægemidler er kun effektive for omkring halvdelen af patienterne, virker primært på de positive symptomer og er forbundet med alvorlige neurologiske og metaboliske bivirkninger. Denne artikel dykker ned i, hvordan moderne lægemiddeldesign og en dybere forståelse af hjernens neurotransmittersystemer baner vejen for nye og forbedrede behandlingsstrategier.
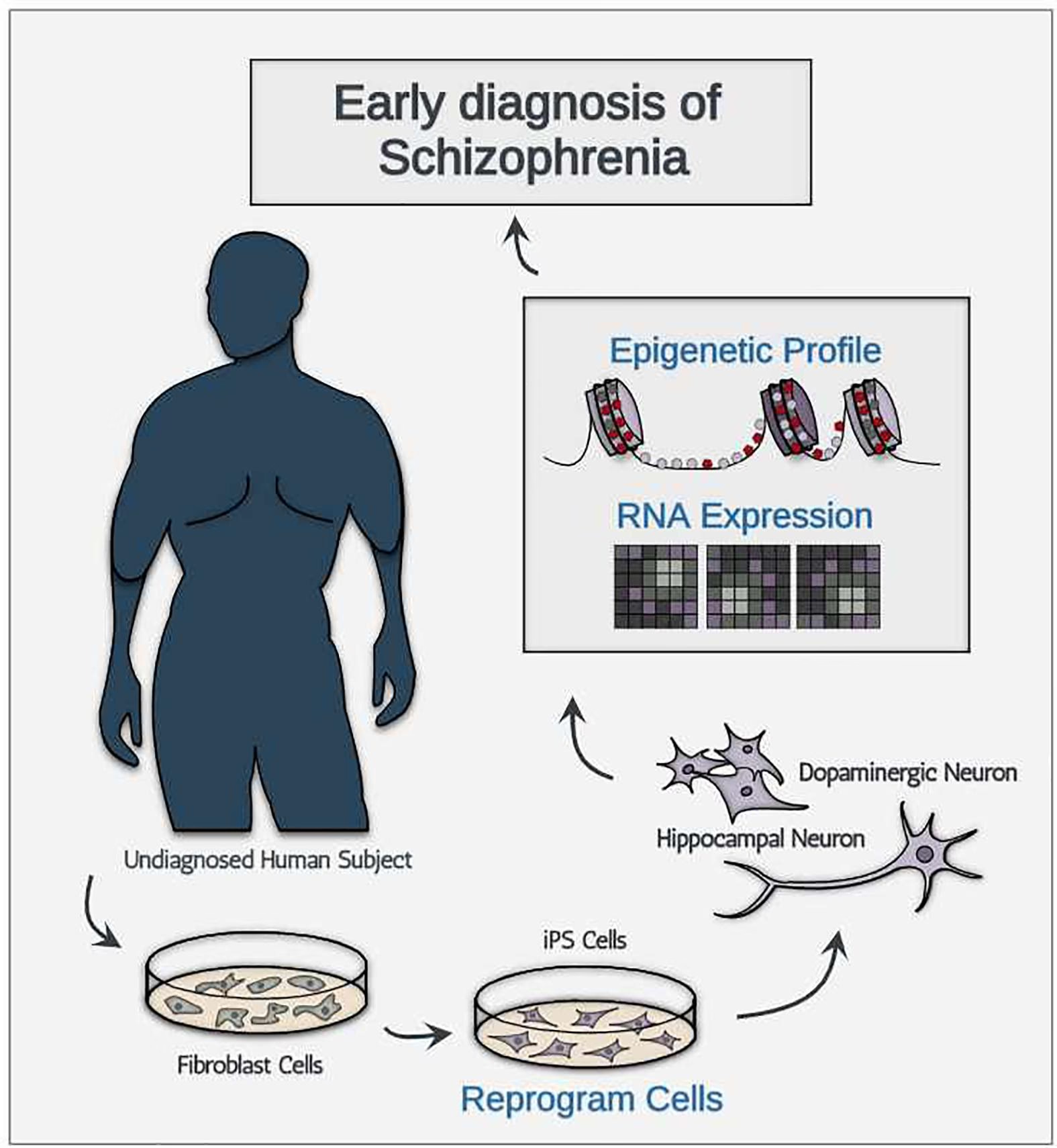
Forståelse af Skizofreni: Neurotransmitter-hypoteser
For at udvikle bedre medicin er det afgørende at forstå de biologiske mekanismer bag skizofreni. Forskningen har ført til flere centrale hypoteser, der fokuserer på forskellige neurotransmittersystemer i hjernen.
Dopaminhypotesen: Den Klassiske Forklaring
Den mest etablerede teori er dopaminhypotesen, som oprindeligt foreslog, at skizofreni skyldtes en overaktivitet af dopamin i hjernen. Denne idé opstod, da man opdagede, at de første antipsykotiske lægemidler virkede ved at blokere dopamin D2-receptorer. Hypotesen er siden blevet mere nuanceret. Man mener nu, at der er en ubalance: for meget dopaminaktivitet i visse hjerneområder (det mesolimbiske system), hvilket forårsager de positive symptomer, og for lidt dopaminaktivitet i andre områder (den præfrontale cortex), hvilket bidrager til de negative og kognitive symptomer. En nyere version, "aberrant salience"-hypotesen, foreslår, at dopamin-dysregulering får patienter til at tillægge irrelevante stimuli en unormal betydning, hvilket kan føre til vrangforestillinger.
Glutamathypotesen: Nøglen til Kognitive Symptomer
Glutamat er den vigtigste excitatoriske neurotransmitter i hjernen og spiller en afgørende rolle for synaptisk plasticitet, læring og hukommelse. Glutamathypotesen for skizofreni postulerer, at en underfunktion af NMDA-receptorer (en type glutamatreceptor) er en central del af sygdomsmekanismen. Denne hypotese understøttes af, at stoffer som phencyclidin (PCP) og ketamin, der blokerer NMDA-receptorer, kan fremkalde psykotiske symptomer, der ligner dem ved skizofreni, især de negative og kognitive. Målretning af glutamatsystemet er derfor et lovende område for udvikling af medicin, der specifikt kan forbedre kognitive funktioner, som nuværende antipsykotika ofte ikke kan afhjælpe.
Serotoninsystemets Rolle
Serotoninsystemet kom i fokus, da man observerede, at hallucinogene stoffer som LSD virker via serotoninreceptorer. Selvom serotonin sandsynligvis ikke er en direkte årsag til skizofreni, spiller det en vigtig modulerende rolle. Andengenerations (atypiske) antipsykotika virker ved at blokere både dopamin D2-receptorer og serotonin 5-HT2A-receptorer. Denne dobbelte virkning menes at være årsagen til, at disse lægemidler har en lavere risiko for motoriske bivirkninger (ekstrapyramidale symptomer) og potentielt en bedre effekt på negative symptomer.
Andre Involverede Systemer
Forskning peger også på dysfunktioner i andre systemer, herunder GABA (den primære hæmmende neurotransmitter), det kolinerge system (hvilket kan forklare den høje forekomst af rygning blandt patienter), samt inflammation og oxidativt stress. Denne kompleksitet understreger, hvorfor en "one-size-fits-all"-tilgang til behandling ofte slår fejl, og hvorfor multimål-lægemidler kan være mere effektive.
Nuværende Behandling: Generationer af Antipsykotika
Behandlingen af skizofreni har udviklet sig gennem flere generationer af lægemidler, hver med sine egne fordele og ulemper.
Førstegenerations (Typiske) Antipsykotika
Introduceret i 1950'erne med klorpromazin, virker disse lægemidler primært ved stærk blokade af dopamin D2-receptorer. De er effektive til at kontrollere positive symptomer som hallucinationer og vrangforestillinger. Deres største ulempe er en høj risiko for alvorlige motoriske bivirkninger, kendt som ekstrapyramidale symptomer (EPS), som kan inkludere stivhed, rysten og ufrivillige bevægelser. Eksempler inkluderer haloperidol og fluphenazin.
Andengenerations (Atypiske) Antipsykotika
Fra 1990'erne og frem kom de atypiske antipsykotika, startende med clozapin. Disse lægemidler har en mere kompleks virkningsmekanisme, der typisk involverer en svagere blokade af D2-receptorer og en stærk blokade af 5-HT2A-receptorer. Dette resulterer i en markant lavere risiko for EPS. De har også vist sig at have en bedre effekt på negative og kognitive symptomer for nogle patienter. Deres akilleshæl er dog en betydelig risiko for metaboliske bivirkninger, såsom markant vægtøgning, forhøjet blodsukker og øget risiko for type 2-diabetes. Eksempler inkluderer clozapin, olanzapin, risperidon og quetiapin.
Sammenligning af Antipsykotika-generationer
| Egenskab | Førstegeneration (Typisk) | Andengeneration (Atypisk) |
|---|---|---|
| Primær mekanisme | Stærk D2-receptorantagonisme | Moderat D2- og stærk 5-HT2A-antagonisme |
| Effektivitet | Primært på positive symptomer | Positive, negative og kognitive symptomer |
| Risiko for EPS | Høj | Lav |
| Risiko for metaboliske bivirkninger | Lav | Høj |
| Eksempler | Haloperidol, Klorpromazin | Clozapin, Olanzapin, Risperidon |
Fremtidens Lægemiddeldesign: Nye Strategier
Begrænsningerne ved nuværende behandlinger har sat skub i forskningen i nye og mere målrettede tilgange. Meget af denne forskning fokuserer på de såkaldte G-protein-koblede receptorer (GPCR'er), som dopamin- og serotoninreceptorerne tilhører.
Funktionel Selektivitet
Traditionelt har man tænkt på lægemidler som enten "tænd" (agonister) eller "sluk" (antagonister) for en receptor. Ny forskning viser, at en receptor kan aktivere flere forskellige signalveje inde i cellen. Funktionel selektivitet, også kendt som "biased agonism", er et koncept, hvor et lægemiddel designes til kun at aktivere de terapeutisk gavnlige signalveje, mens de veje, der fører til bivirkninger, blokeres. Dette kunne teoretisk set føre til lægemidler med samme effekt som nuværende antipsykotika, men med færre eller ingen bivirkninger.
Allosterisk Modulation
I stedet for at binde sig til det primære (ortosteriske) bindingssted på en receptor, hvor kroppens egne neurotransmittere binder sig, kan allosteriske modulatorer binde sig til et andet, separat sted. Fra dette "kontrolpanel" kan de finjustere receptorens følsomhed over for den naturlige neurotransmitter. En positiv allosterisk modulator (PAM) vil forstærke signalet, mens en negativ (NAM) vil dæmpe det. Denne tilgang giver mulighed for en mere subtil og fysiologisk regulering af hjernens kemi, hvilket kan reducere risikoen for overdosering og bivirkninger.
Målretning af Receptor-heterodimerer
En af de mest spændende nye fronter inden for lægemiddeldesign er erkendelsen af, at receptorer ikke altid fungerer alene. De kan danne par, såkaldte heterodimerer (f.eks. en dopamin D2-receptor, der parres med en serotonin 5-HT2A-receptor). Disse receptorpar har unikke farmakologiske egenskaber, der adskiller sig fra de enkelte receptorer. Ved at designe lægemidler, der udelukkende virker på disse specifikke par, kan man opnå en hidtil uset grad af specificitet og potentielt undgå at påvirke receptorer i andre dele af hjernen eller kroppen, hvor de udfører vigtige funktioner. Dette kan dramatisk forbedre bivirkningsprofilen for fremtidens antipsykotika.
Ofte Stillede Spørgsmål
Hvad er de primære symptomer på skizofreni?
Symptomerne inddeles i tre grupper: positive (hallucinationer, vrangforestillinger, desorganiseret tale), negative (apati, manglende glæde, social tilbagetrækning) og kognitive (problemer med hukommelse, opmærksomhed og eksekutive funktioner).
Hvorfor virker antipsykotika ikke for alle patienter?
Skizofreni er en heterogen sygdom med komplekse og varierede årsager. Genetiske forskelle og forskelle i sygdommens underliggende neurobiologi betyder, at en behandling, der virker for én patient, ikke nødvendigvis virker for en anden. Cirka 30% af patienterne betragtes som "behandlingsresistente".
Hvad er den største forskel på typiske og atypiske antipsykotika?
Den største forskel ligger i deres bivirkningsprofil. Typiske (førstegenerations) antipsykotika har en høj risiko for motoriske bivirkninger (EPS), mens atypiske (andengenerations) antipsykotika har en lavere risiko for EPS, men en højere risiko for metaboliske bivirkninger som vægtøgning og diabetes.
Hvorfor er udviklingen af nye lægemidler så vigtig?
Nye lægemidler er nødvendige for at imødekomme de store udækkede behov i behandlingen af skizofreni. Målene er at finde behandlinger, der er mere effektive mod negative og kognitive symptomer, virker for behandlingsresistente patienter og har en markant bedre bivirkningsprofil for at forbedre patienternes livskvalitet og behandlingsadhærens.
Afslutningsvis står vi over for en spændende fremtid inden for behandlingen af skizofreni. Mens nuværende lægemidler har hjulpet utallige mennesker, har deres begrænsninger også understreget behovet for innovation. Gennem avanceret lægemiddeldesign, der udnytter vores voksende viden om hjernens komplekse signalveje, er der et reelt håb om at udvikle en ny generation af antipsykotika, der er både mere effektive og sikrere, og som kan tilbyde en bedre fremtid for mennesker, der lever med denne udfordrende sygdom.
Hvis du vil læse andre artikler, der ligner Nye Håb i Behandling af Skizofreni, kan du besøge kategorien Sundhed.

