09/04/2013
Rabies, en sygdom der har plaget menneskeheden i århundreder, er forårsaget af et virus med en bemærkelsesværdig og yderst velorganiseret indre struktur. Centralt i dette virus' livscyklus og patogenicitet står dets ribonukleoproteinkompleks, ofte forkortet RNP. Men hvad er dette kompleks præcist, og hvordan er det opbygget? Takket være avancerede teknikker som kryo-elektronmikroskopi (cryoEM) er forskere nu i stand til at dissekere virussets arkitektur på et næsten atomart niveau. Denne artikel vil udforske den detaljerede opbygning af rabiesvirussets (RABV) RNP og belyse, hvorfor en dyb forståelse af denne struktur er afgørende i kampen mod rabies.
Virussets Ydre Form og Dimensioner
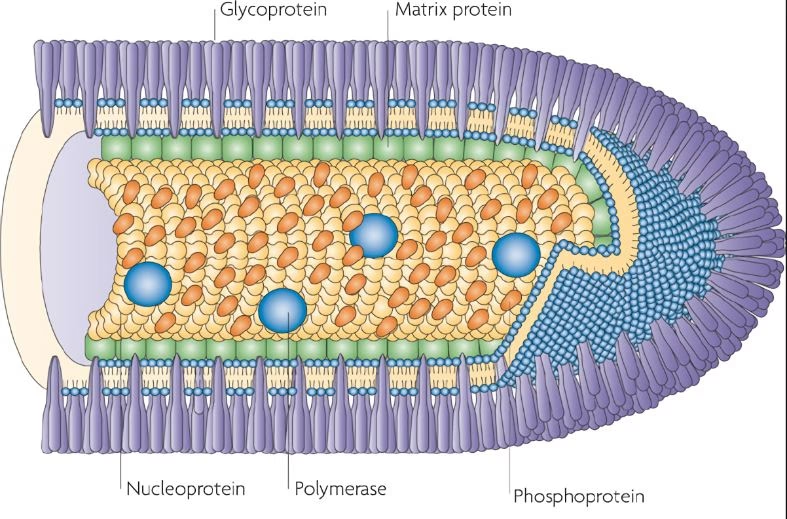
Når man observerer rabiesviruspartikler i et mikroskop, kan man skelne mellem forskellige morfologiske former. Den mest klassiske og velkendte form er den karakteristiske kugleform, der ligner et projektil. Dog findes der også mere afrundede partikler. Begge former er funktionelle og indeholder det virale genom, som er essentielt for infektion. Nyere studier, der anvender tomografisk analyse, har givet os præcise målinger af disse virale partikler.
Rekombinante RABV-partikler har en gennemsnitlig længde på omkring 198 nanometer (nm), med variationer fra 183 til 222 nm. Diameteren ligger i gennemsnit på 86 nm (fra 77 til 95 nm). Disse dimensioner er en smule større end tidligere rapporteret, hvilket understreger vigtigheden af kontinuerlig forskning med forbedrede teknologier. Den cylindriske del af viruspartiklen, 'kroppen', består i gennemsnit af 18 helikale vindinger, mens den koniske ende, 'spidsen', har mellem 1 og 7 vindinger. Denne præcise geometriske opbygning er ikke tilfældig; den er dikteret af den underliggende RNP-struktur.
Ribonukleoproteinets Helikale Arkitektur
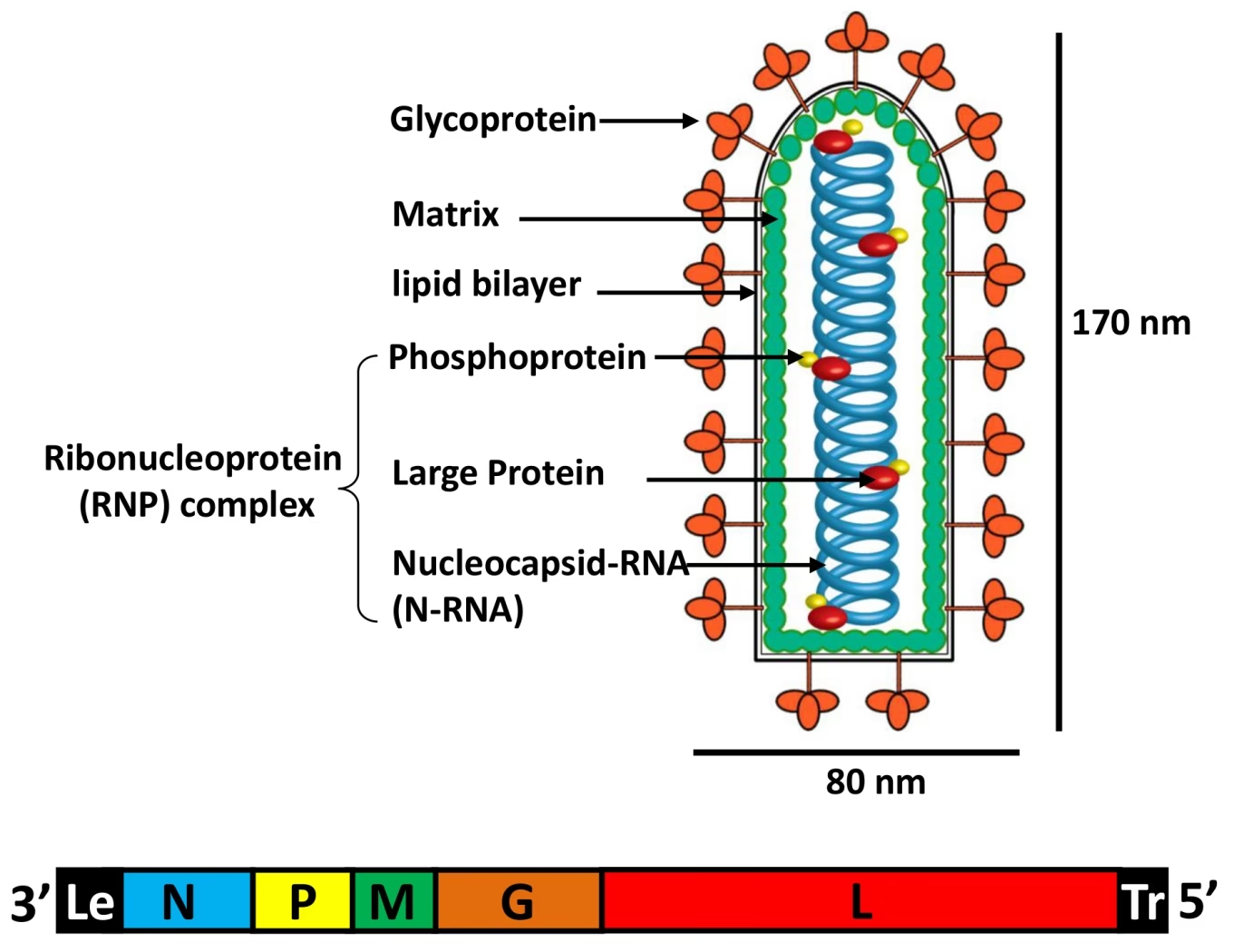
Kernen i rabiesvirus er Ribonukleoproteinet (RNP). Dette er et komplekst maskineri bestående af viralt RNA (arvematerialet) tæt pakket sammen med virale proteiner, primært nukleoproteinet (N-protein). RNP'en er organiseret i en stram, venstrehåndet heliks (spiral), der giver virusset dets form og beskytter det skrøbelige genom. Ved hjælp af en teknik kaldet subtomogram-gennemsnit, har forskere kunnet rekonstruere en 3D-model af RNP-helixen med en opløsning på 15 Ångstrøm (Å), hvilket giver et hidtil uset detaljeringsniveau.
Inden i viruspartiklen fremstår RNP'en med et mønster, der minder om et brystben, hvor hver 'ribbe' repræsenterer en individuel helikal vinding. Disse vindinger har en bemærkelsesværdig præcis organisering:
- De afviger med en vinkel på 44° fra virussets centrale akse.
- Afstanden mellem hver vinding er præcist 71 Å.
- Den ydre diameter af helixen er i gennemsnit 67 nm, mens den indre diameter er 51 nm.
Denne tætpakkede og stabile struktur er afgørende for at beskytte det virale RNA mod nedbrydning, både inde i og uden for værtscellen.
Interaktionen mellem N- og M-Proteiner
Hver helikal vinding kan yderligere opdeles i tre fremtrædende strukturelle zoner: en membran-proksimal (tættest på virusmembranen), en central og en membran-distal (tættest på virussets centrum) del. En af de mest interessante opdagelser er tilstedeværelsen af små 'broer' af tæthed, der forbinder den membran-proksimale del af én vinding med den centrale del af den nærliggende vinding i retning mod virussets koniske spids. Disse broer skaber en stærk og sammenvævet struktur.
Ved at kombinere elektronmikroskopidata med kendte krystalstrukturer har man kunnet 'docke' individuelle N-proteiner ind i 3D-kortet. N-proteinet er det primære protein, der binder til RNA'et og danner rygraden i RNP-helixen. Analysen viser, at RNA-bindingsrillen på hvert N-protein vender mod virussets spids. Dette indebærer, at 3'-enden af det virale RNA (starten af genomet) er placeret i den koniske ende af RNP'en, hvilket er en vigtig information for at forstå, hvordan transkription og replikation initieres.
Den membran-proksimale tæthed menes at huse et andet afgørende protein: matrixproteinet (M-protein). M-proteinet fungerer som et bindeled mellem den indre RNP-kerne og den ydre virusmembran, der indeholder glykoproteinerne, som virusset bruger til at binde sig til værtsceller. Selvom opløsningen endnu ikke er høj nok til utvetydigt at placere M-proteinet, tyder modellerne på en tæt og kompleks interaktion. Et M-protein er sandsynligvis forbundet med mindst ét N-protein på samme vinding, ét N-protein på en nabovinding og to andre M-proteiner. Dette skaber et stærkt, vævet netværk, der stabiliserer hele viruspartiklen.
Strukturelle Parametre for Rabiesvirus
For at give et klart overblik er her en tabel, der opsummerer de vigtigste morfometriske parametre for rabiesviruspartiklen og dens RNP-kompleks, som er blevet bestemt gennem cryoEM-tomografi.
| Parameter | Gennemsnitlig Værdi | Måleområde |
|---|---|---|
| Partikellængde | 198 nm | 183–222 nm |
| Partikeldiameter | 86 nm | 77–95 nm |
| Antal helikale vindinger (krop) | 18 | 14–24 |
| RNP helix ydre diameter | 67 nm | 56–74 nm |
| RNP helix indre diameter | 51 nm | 43–57 nm |
| Afstand mellem vindinger | 71 Å | N/A |
| Vindingers vinkel fra central akse | 44° | N/A |
Betydningen for Fremtidig Behandling
Spørgsmålet 'har rabiesvirus et ribonukleoprotein?' kan besvares med et rungende ja. Det er ikke bare til stede; det er en yderst sofistikeret og velordnet helikale struktur, der er fundamental for virussets overlevelse og funktion. Hvorfor er denne detaljerede viden så vigtig? Fordi RNP-komplekset er et ideelt mål for antivirale lægemidler. Processer som samlingen af RNP, interaktionen mellem N- og M-proteiner, og funktionen af den virale polymerase, der bevæger sig langs RNP-skabelonen, er alle potentielle akilleshæle for virusset.
Ved at forstå den præcise tredimensionelle arkitektur af disse komponenter kan forskere designe små molekyler, der specifikt kan binde sig til kritiske kontaktflader og dermed forstyrre virussets livscyklus. For eksempel kunne et lægemiddel, der forhindrer M-proteinet i at binde korrekt til N-proteinet, destabilisere hele viruspartiklen og forhindre dannelsen af nye, infektiøse vira. Denne strukturbaserede tilgang til lægemiddeludvikling er en af de mest lovende veje fremad i kampen mod virussygdomme som rabies.
Ofte Stillede Spørgsmål (FAQ)
Hvad er et ribonukleoprotein (RNP) helt præcist?
Et ribonukleoprotein er et kompleks, der består af ribonukleinsyre (RNA) og protein. I vira som rabiesvirus er RNP'ens primære funktion at beskytte det sårbare virale genom (RNA) og organisere det på en måde, der muliggør effektiv replikation og transkription inde i en værtscelle.
Hvorfor er rabiesvirus formet som et projektil?
Den karakteristiske kugleform er bestemt af den underliggende RNP-heliks. Den lange, cylindriske krop dannes af de regelmæssige vindinger af helixen, mens den koniske spids dannes, hvor helixen gradvist snævrer ind. Denne form er typisk for vira i Rhabdoviridae-familien.
Er alle rabiesviruspartikler ens?
Nej. Selvom den klassiske kugleform er den mest kendte, observeres også mere afrundede partikler. Variationerne kan skyldes små uregelmæssigheder under samlingsprocessen, men begge former indeholder det essentielle RNP-kompleks og er potentielt infektiøse.
Hvordan kan denne forskning føre til en kur mod rabies?
Selvom vi har effektive vacciner til at forhindre rabies, er behandlingsmulighederne yderst begrænsede, når først symptomerne viser sig. Ved at identificere svage punkter i virussets RNP-struktur kan forskere udvikle antivirale lægemidler, der kan stoppe virusreplikationen hos en allerede smittet person. Dette ville være et gennembrud i behandlingen af aktiv rabiesinfektion.
Hvis du vil læse andre artikler, der ligner Rabiesvirus: En Dybdegående Analyse af RNP, kan du besøge kategorien Sundhed.