20/07/2002
Mange af os kender den alt for godt: den pludselige, skarpe smerte i halsen, feberen der stiger, og den generelle følelse af utilpashed. Ofte er synderen en lille, kugleformet bakterie ved navn Streptococcus pyogenes, også kendt som Gruppe A streptokokker (GAS). Denne mikroorganisme er ansvarlig for op mod 700 millioner infektioner globalt hvert år, spændende fra relativt milde lidelser som halsbetændelse og børnesår til livstruende tilstande som sepsis (blodforgiftning) og nekrotiserende fasciitis, populært kendt som "den kødædende bakterie". Men hvordan kan en enkelt bakterieart forårsage så vidt forskellige sygdomme og være så succesfuld i at inficere mennesker? Svaret ligger i dens bemærkelsesværdige evne til at tilpasse sig og snyde vores immunsystem, en evne der i høj grad er orkestreret af et enkelt, men yderst komplekst, overfladeprotein.
Ny forskning har kastet lys over bakteriens udspekulerede overlevelsesstrategier. Det viser sig, at Streptococcus pyogenes ikke er en statisk fjende; den er en mester i at aflæse sine omgivelser og ændre sin taktik derefter. Afhængigt af om den befinder sig i spyttet i din hals eller er trængt ind i din blodbane, ændrer den, hvilke af kroppens egne proteiner den binder til sig. Denne adfærd kan bedst beskrives som en kamæleonlignende evne til at skifte forklædning for at undgå at blive opdaget og tilintetgjort af kroppens forsvar. Denne artikel dykker ned i den fascinerende verden af vært-patogen interaktioner og afslører, hvordan denne almindelige bakterie bruger sit vigtigste våben, M-proteinet, til at udkæmpe en sofistikeret kamp for overlevelse inde i os.
M-proteinet: Bakteriens Multifunktionelle Værktøj
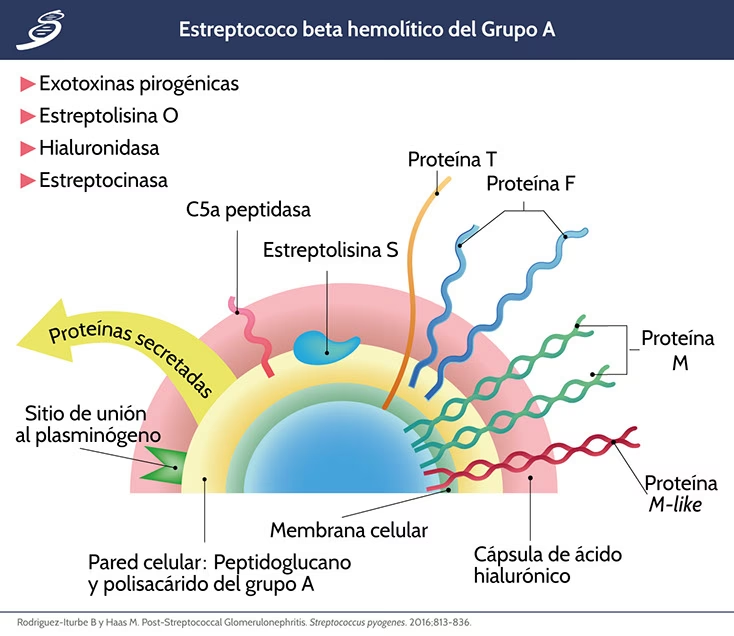
Forestil dig overfladen af Streptococcus pyogenes som et tæt landskab af små, hårlignende strukturer, der stikker ud i omgivelserne. Disse strukturer er primært bygget af et protein kaldet M-protein. Dette protein er ikke bare en del af bakteriens struktur; det er dens primære værktøj til interaktion med den menneskelige vært. Det fungerer som en kombination af et anker, et skjold og en sensor. Der findes over 220 forskellige kendte serotyper af M-proteinet, hvilket er en af hovedårsagerne til, at man kan få halsbetændelse igen og igen – en infektion med én type giver ikke nødvendigvis immunitet mod en anden.
M-proteiner kan groft inddeles i forskellige mønstre eller klasser baseret på deres domænestruktur. De to mest fremtrædende er mønster A-C og mønster E. Tænk på disse mønstre som forskellige modeller af et multifunktionelt værktøj. A-C mønsteret er typisk længere og har flere forskellige "værktøjer" (domæner), mens E-mønsteret er kortere og mere specialiseret. Forskere har observeret, at disse strukturelle forskelle har en direkte indflydelse på, hvor i kroppen de forskellige streptokokstammer foretrækker at opholde sig (vævstropisme). Stammer med A-C mønster M-proteiner er ofte forbundet med halsinfektioner, mens E-mønster stammer er mere alsidige og kan forårsage infektioner i både hals og hud.
Denne specialisering skyldes, at de forskellige domæner på M-proteinet er designet til at binde sig til specifikke humane proteiner. For eksempel er A-C mønsteret kendt for sin evne til at binde fibrinogen, et protein i blodet der er afgørende for blodstørkning. Ved at dække sig med fibrinogen kan bakterien undgå at blive genkendt og "spist" af immunceller (fagocytose). E-mønster proteiner, derimod, har specialiseret sig i at binde andre humane proteiner, såsom immunglobulin A (IgA) og et vigtigt protein fra immunsystemet kaldet C4BP.
En Kamp på To Fronter: Halsen vs. Blodbanen
Den mest banebrydende opdagelse er, hvordan M-proteinet dynamisk ændrer sine interaktioner afhængigt af det mikromiljø, det befinder sig i. Lad os se på et specifikt eksempel med M28, et M-protein af E-mønsteret, for at forstå denne utrolige tilpasningsevne.
Fase 1: Den Lokale Infektion i Halsen
Når Streptococcus pyogenes etablerer sig på slimhinderne i halsen, befinder den sig i et miljø rigt på spyt. Spyttet indeholder en særlig type antistof kaldet sekretorisk IgA (sIgA). sIgA er immunsystemets første forsvarslinje på slimhinderne. Dets opgave er at fange og neutralisere indtrængende patogener. M28-proteinet har imidlertid udviklet en højaffinitetsbindingsplads specifikt for sIgA. Ved at binde sIgA til sig, opnår bakterien to ting: For det første neutraliserer den effektivt antistoffet, så det ikke kan udføre sin funktion. For det andet bruger den potentielt antistoffet som en slags camouflage, hvilket hjælper bakterien med at klæbe sig til slimhindecellerne og undgå andre dele af immunforsvaret.
Fase 2: Den Systemiske Invasion
Hvis infektionen bliver mere alvorlig, kan bakterien forårsage skade på de lokale væv og blodkar. Dette skaber en tilstand af "vaskulær lækage", hvor proteiner fra blodplasma siver ud i det omkringliggende væv. Pludselig ændres bakteriens mikromiljø dramatisk. Koncentrationen af sIgA falder relativt set, mens koncentrationen af plasmaproteiner som monomerisk IgA og især C4b-bindende protein (C4BP) stiger voldsomt.
Her viser M28-proteinet sin geniale tilpasningsevne. Det "skifter partner". Bindingen til sIgA bliver erstattet af en stærk binding til C4BP og monomerisk IgA. Dette skifte er ikke tilfældigt; det er en afgørende overlevelsesmanøvre. C4BP er en potent regulator af komplementsystemet, en kaskade af proteiner i blodet, der er en fundamental del af det medfødte immunforsvar. Komplementsystemet kan direkte dræbe bakterier og "mærke" dem for destruktion af immunceller. Ved at binde C4BP til sin overflade, kaprer Streptococcus pyogenes effektivt denne regulator og bruger den til at deaktivere komplementangreb rettet mod sig selv. Det er som at stjæle fjendens skjold og bruge det til sin egen beskyttelse. Den samtidige binding af monomerisk IgA kan yderligere forhindre fagocytose.
Sammenligning af Interaktioner i Forskellige Miljøer
For at gøre denne komplekse strategi mere overskuelig, kan vi opstille en tabel, der sammenligner bakteriens adfærd i de to miljøer.
| Egenskab | Lokal Infektion (Hals/Slimhinde) | Systemisk Infektion (Blodbane) |
|---|---|---|
| Primært Miljø | Spyt | Blodplasma |
| Dominerende Humane Proteiner | Sekretorisk IgA (sIgA) | Monomerisk IgA, C4BP, Fibrinogen |
| M28-proteinets Primære Binding | Høj affinitet til Sekretorisk IgA (sIgA) | Høj affinitet til C4BP og monomerisk IgA |
| Bakteriens Strategiske Mål | Neutralisere første forsvarslinje, vedhæftning, undgå fagocytose | Deaktivere komplementsystemet, undgå fagocytose, overleve i blodet |
Ofte Stillede Spørgsmål (FAQ)
Hvad er Streptococcus pyogenes helt præcist?
Streptococcus pyogenes er en Gram-positiv bakterie, der er en del af den normale flora hos nogle mennesker, men som oftest er et patogen. Den er årsag til en bred vifte af sygdomme, fra almindelig halsbetændelse og hudinfektioner til alvorlige, invasive sygdomme som skarlagensfeber, gigtfeber og sepsis.
Er M-proteinet det eneste våben, bakterien har?
Nej, M-proteinet er det vigtigste og mest studerede, men S. pyogenes producerer en lang række andre virulensfaktorer, herunder toksiner, der kan ødelægge røde blodlegemer (hæmolysiner) og enzymer, der kan nedbryde væv og hjælpe bakterien med at sprede sig.
Betyder denne tilpasningsevne, at bakterien "tænker"?
Nej, bakterien tænker ikke. Denne sofistikerede adfærd er et resultat af millioner af års evolution. De bakterier, der tilfældigvis udviklede M-proteiner med evnen til at binde de rigtige humane proteiner i de rigtige miljøer, havde en større chance for at overleve og formere sig. Over tid er denne egenskab blevet dominerende. Det er et klassisk eksempel på naturlig selektion i aktion på et mikroskopisk niveau.
Hvordan kan denne viden bruges medicinsk?
En dybere forståelse af, hvordan M-proteinet interagerer med værtens proteiner, åbner op for nye behandlingsmuligheder. I stedet for traditionelle antibiotika kunne man udvikle lægemidler, der specifikt blokerer for M-proteinets evne til at binde f.eks. C4BP eller IgA. Dette ville "afvæbne" bakterien og gøre den sårbar over for kroppens eget immunsystem. Det er også afgørende viden for udviklingen af en effektiv vaccine, som i årtier har været en stor udfordring netop på grund af M-proteinets store variation.
Hvorfor er nogle streptokokinfektioner milde og andre dødelige?
Dette afhænger af en kombination af faktorer: den specifikke stamme af S. pyogenes og dens M-protein type, værtens immunstatus (om personen er svækket i forvejen), og hvor infektionen starter. En bakterie, der hurtigt formår at trænge ind i blodbanen og aktivere sin "systemiske" overlevelsesstrategi ved at binde C4BP, har potentialet til at forårsage en meget mere alvorlig sygdom end en, der forbliver lokaliseret i halsen.
Konklusion: En Lektion i Mikrobiel Overlevelse
Studiet af Streptococcus pyogenes og dets M-protein afslører en verden af utrolig kompleksitet og tilpasning. Denne bakterie er ikke bare en passiv angriber; den er en aktiv deltager, der konstant sonderer og reagerer på sit miljø. Ved at danne miljøafhængige komplekser med værtens egne proteiner, har den udviklet en yderst effektiv strategi for at omgå vores immunforsvar. Den kamæleonlignende evne til at skifte fra at binde sIgA i spyttet til at kapre C4BP i blodet er et vidnesbyrd om den evolutionære kamp mellem patogen og vært. Denne viden understreger ikke kun, hvorfor S. pyogenes fortsat er en betydelig trussel mod menneskers sundhed, men den giver os også et nyt landkort, som vi kan bruge til at designe smartere og mere målrettede terapier mod denne alsidige og farlige mikroorganisme.
Hvis du vil læse andre artikler, der ligner S. pyogenes: Bakteriens Kamæleontrick, kan du besøge kategorien Sundhed.
