16/03/2000
Humant immundefektvirus type 1 (HIV-1) er et retrovirus, en type virus, der udgør en vedvarende global sundhedstrussel. Det unikke ved retrovirusser er deres evne til at omskrive deres genetiske materiale, som består af RNA, til DNA. Dette DNA bliver derefter integreret i værtscellens eget genom, hvilket tvinger cellen til at producere nye viruspartikler. Kernen i hele denne proces er HIV-1's RNA-genom – en kompleks og dynamisk molekylær manual, der styrer hvert eneste trin i virussens livscyklus. At forstå de indviklede roller, som de forskellige RNA-strukturer spiller, er ikke kun afgørende for at forstå virussens biologi, men også for at designe nye og mere effektive terapeutiske strategier til bekæmpelse af AIDS.
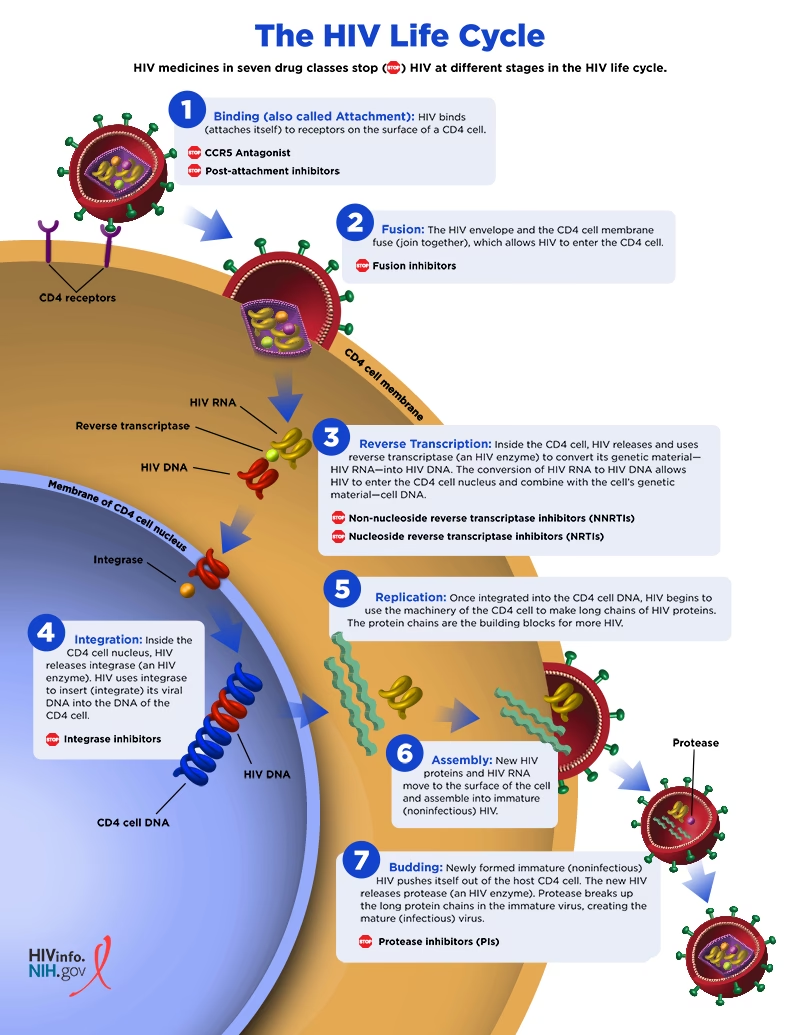
En Oversigt over HIV-1's Livscyklus
HIV-1's livscyklus er en nøje orkestreret proces, der kan opdeles i flere faser, fra det øjeblik virussen møder en værtscelle, til nye, smitsomme viruspartikler frigives. Hver fase er dybt afhængig af specifikke strukturer i virussens RNA.
Processen starter, når HIV-1 binder sig til receptorer på overfladen af en værtscelle, typisk en T-hjælpercelle. Dette fører til en fusion mellem virussens og cellens membraner, hvorefter virussens kerne frigives i cellens cytoplasma. Inde i denne kerne begynder en af de mest afgørende processer: omvendt transkription. Her omdanner enzymet revers transkriptase (RT) de to enkeltstrengede RNA-genomer til en dobbeltstrenget DNA-kopi. Dette virale DNA transporteres derefter ind i cellekernen og integreres i værtscellens kromosomale DNA af enzymet integrase. Fra dette punkt er virus en permanent del af cellen og kaldes et provirus.
Når proviruset er integreret, bruger det cellens eget maskineri til at transkribere sit DNA tilbage til viralt RNA. Disse nye RNA-molekyler har to primære skæbner: Nogle fungerer som messenger-RNA (mRNA) til at producere virale proteiner, mens andre vil blive pakket som genomer i nye viruspartikler. De nydannede virale proteiner og RNA-genomer samles ved cellemembranen, hvorefter en ny, umoden viruspartikel afsnøres. Til sidst gennemgår denne partikel en modningsproces, hvor proteiner spaltes og omarrangeres, hvilket resulterer i en fuldt smitsom virus, klar til at inficere nye celler.
De Specifikke Roller af HIV-1 RNA-Elementer
HIV-1's genom er ikke blot en passiv kode. Det er spækket med højt strukturerede RNA-elementer, der aktivt deltager i og regulerer de forskellige faser af replikationen. Lad os se nærmere på nogle af de vigtigste.
PBS (Primer Binding Site): Startskuddet til Omvendt Transkription
Processen med at omdanne RNA til DNA kræver en primer – et lille startmolekyle. HIV-1 har på smart vis kapret et molekyle fra værtscellen til dette formål: et transfer-RNA kaldet tRNA-Lys3. Dette tRNA binder sig til et specifikt sted på det virale RNA, kendt som Primer Binding Site (PBS). Denne binding danner en kort dobbeltstrenget region, som enzymet revers transkriptase genkender som startpunkt. Uden denne præcise interaktion mellem tRNA og PBS-regionen kan omvendt transkription ikke begynde, og virussens livscyklus stoppes, før den rigtigt er kommet i gang.
TAR (Trans-Activation Response Element): Produktionsforstærkeren
Når det virale DNA er integreret i værtscellens genom, skal det transkriberes effektivt for at producere store mængder nyt viralt RNA. Denne proces er i starten meget ineffektiv, men HIV-1 har en genial mekanisme til at sætte turbo på produktionen. Ved 5'-enden af alle nyligt dannede virale RNA-transkripter findes en hårnåle-lignende struktur kaldet TAR (Trans-Activation Response Element). Denne struktur fungerer som en landingsplads for et viralt protein kaldet Tat (Trans-Activator of Transcription). Når Tat binder sig til TAR, rekrutterer det cellulære faktorer, der dramatisk øger transkriptionshastigheden. Denne interaktion fungerer som en positiv feedback-loop: mere RNA fører til mere Tat-protein, som igen fører til endnu mere RNA. TAR's unikke og fleksible struktur gør det også til et attraktivt mål for lægemiddeludvikling, da stoffer, der kan blokere Tat-bindingen, kan bremse virusproduktionen markant.
RRE (Rev Response Element): Billetten ud af Cellekernen
Værtsceller har normalt strenge regler for, hvilke RNA-molekyler der må forlade kernen og transporteres ud i cytoplasmaet for at blive oversat til protein. Typisk er det kun fuldt splejsede (færdigbehandlede) mRNA'er, der får lov at passere. Dette udgør et problem for HIV-1, da virussen har brug for både usplejsede og delvist splejsede RNA'er i cytoplasmaet – de usplejsede skal fungere som genomer for nye vira. Løsningen er et andet komplekst RNA-element kaldet RRE (Rev Response Element), som findes i alle usplejsede og delvist splejsede RNA'er. Et andet viralt protein, Rev, binder sig til RRE inde i kernen. Rev/RRE-komplekset fungerer som en nøgle, der interagerer med cellens eksportmaskineri og sikrer, at de usplejsede virale RNA'er kan smugles ud af kernen. Uden denne mekanisme ville de genomiske RNA'er forblive fanget, og ingen nye viruspartikler kunne samles.
Pakning af Genomet: Hvordan HIV-1 Vælger og Samler sit RNA
En af de mest fascinerende processer er, hvordan HIV-1 specifikt udvælger og pakker to kopier af sit genomiske RNA ind i hver ny viruspartikel blandt tusindvis af cellulære RNA-molekyler. Denne proces er afgørende for virussens overlevelse og involverer en række nøje afstemte interaktioner.

Psi (Ψ) Signalet: Det Genomiske Postnummer
Nøglen til den selektive pakning er en meget struktureret region i 5'-enden af det genomiske RNA, kendt som Psi (Ψ) signalet. Denne region fungerer som et unikt "postnummer" eller en genkendelsessignatur, der fortæller det virale samlemaskineri: "Dette er et genom, der skal pakkes". Psi-regionen består af flere hårnåle-strukturer (stem-loops), herunder SL1, SL2, SL3 og SL4.
Dimerisering: To er Bedre end Én
HIV-1 pakker altid to identiske RNA-genomer, som holdes sammen i en dimer. Denne dimerisering er en forudsætning for pakning og menes at give virussen en evolutionær fordel, f.eks. ved at tillade genetisk rekombination. Dimeriseringen initieres af en specifik sekvens i SL1-hårnålen, kaldet DIS (Dimerization Initiation Site). DIS-sekvenserne fra to forskellige RNA-genomer er selvkomplementære, hvilket betyder, at de kan baseparre med hinanden. Dette skaber en indledende forbindelse mellem de to genomer, ofte beskrevet som et "kissing-loop" kompleks. Denne løse forbindelse omdannes efterfølgende til en mere stabil, udvidet dobbeltspiral (extended duplex), som låser de to genomer sammen.
Gag-polyproteinets Hovedrolle
Den centrale aktør i både genkendelse og pakning er det virale Gag-polyprotein. Gag er et stort protein, der senere spaltes til flere mindre strukturproteiner. En specifik del af Gag, nukleokapsid-domænet (NC), har en stærk affinitet for Psi-signalets struktur. Gag-proteiner binder sig til Psi-regionen på det dimeriserede RNA-genom og fungerer som en bro mellem genomet og cellemembranen, hvor samlingen af den nye viruspartikel finder sted. Gag medierer ikke kun pakningen af RNA'et, men driver også selve samlingen og afsnøringen af den nye virus. Forskning tyder på, at Gag-koncentrationen i cellen er afgørende; først når der er produceret en tilstrækkelig mængde Gag, skifter RNA'et til en konformation, der er klar til dimerisering og pakning.
Præcis hvor i cellen dimeriseringen sker, er stadig genstand for debat. Nogle studier tyder på, at det sker i cytoplasmaet, hvorefter dimeren transporteres til cellemembranen, mens andre peger på, at dimeriseringen først sker ved selve cellemembranen, medieret af Gag-proteiner, der allerede er bundet der.
Tabel: Nøgle RNA-Elementer i HIV-1
| RNA-Element | Primær Funktion | Interagerer med |
|---|---|---|
| PBS (Primer Binding Site) | Initierer omvendt transkription. | tRNA-Lys3, Revers Transkriptase (RT) |
| TAR (Trans-Activation Response) | Forstærker transkription af viralt genom. | Tat-protein, cellulære faktorer |
| RRE (Rev Response Element) | Medierer eksport af usplejset RNA fra kernen. | Rev-protein, cellulært eksportmaskineri |
| Psi (Ψ) / DIS | Signal for genom-pakning og initiering af dimerisering. | Gag-polyprotein, et andet RNA-genom |
Ofte Stillede Spørgsmål
Hvad er et retrovirus?
Et retrovirus er en type virus, der har RNA som sit genetiske materiale. Når det inficerer en celle, bruger det et specielt enzym kaldet revers transkriptase til at lave en DNA-kopi af sit RNA-genom. Dette DNA integreres derefter i værtscellens DNA, hvilket gør infektionen permanent.
Hvorfor pakker HIV-1 to kopier af sit RNA-genom?
At have to kopier (at være diploid) giver virussen flere fordele. Det øger sandsynligheden for en vellykket infektion og giver mulighed for genetisk rekombination. Hvis der opstår skader på den ene RNA-streng under omvendt transkription, kan enzymet skifte over og bruge den anden streng som skabelon, hvilket fungerer som en form for reparation og skaber genetisk variation.
Hvad er Gag-polyproteinets vigtigste funktioner?
Gag er det primære strukturelle protein i HIV-1. Det har flere afgørende roller: Det genkender og binder det virale RNA-genom via Psi-signalet, det medierer transporten af genomet til cellemembranen, det driver samlingen af den nye viruspartikel, og det er ansvarligt for afsnøringen fra værtscellen.
Kan man udvikle medicin, der specifikt rammer HIV's RNA-strukturer?
Ja, det er et aktivt forskningsområde. Fordi mange af RNA-strukturerne som TAR og RRE er unikke for virussen og essentielle for dens overlevelse, udgør de lovende mål for nye antivirale lægemidler. Udfordringen ligger i at designe små molekyler, der kan binde sig til disse RNA-strukturer med høj specificitet og affinitet og dermed blokere deres funktion uden at påvirke cellens egne processer.
Hvis du vil læse andre artikler, der ligner HIV-1 RNA: Virussens Kritiske Byggeplan, kan du besøge kategorien Sundhed.
