26/09/2018
I århundreder har man haft en mistanke om en sammenhæng mellem tændernes sundhed og generel kropslig velvære. Allerede Hippokrates bemærkede, at tandudtrækning kunne lindre ledsmerter. I dag er denne observation ikke længere blot en anekdote, men et intenst forskningsområde. Nyere videnskabelige opdagelser har afsløret en direkte og foruroligende forbindelse mellem en specifik bakterie i vores mund og den invaliderende autoimmune sygdom, leddegigt. Denne artikel dykker ned i den patogene rolle, som bakterien Porphyromonas gingivalis spiller, og hvordan en infektion i tandkødet potentielt kan udløse eller forværre leddegigt.
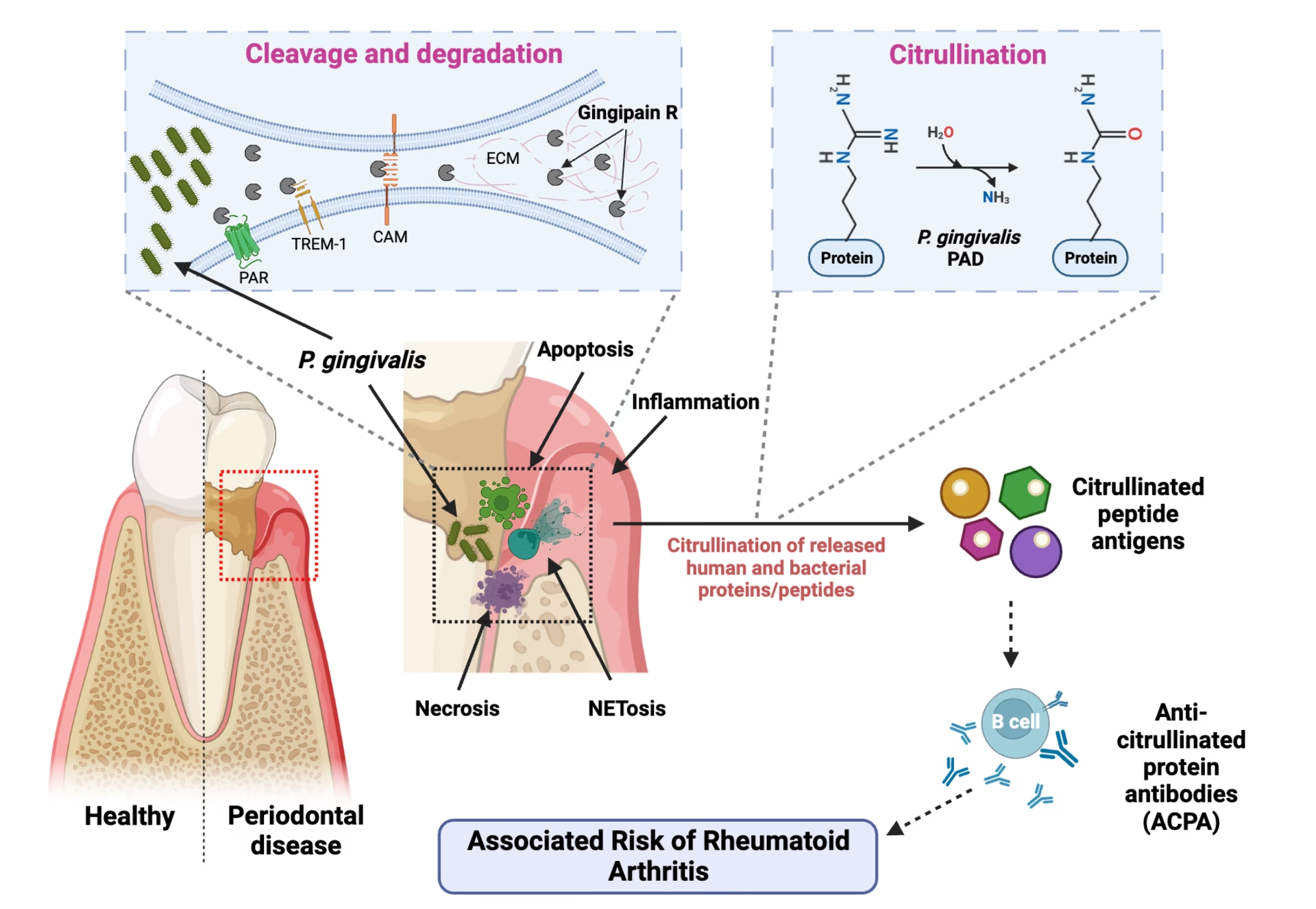
Hvad er Leddegigt og Paradentose?
For at forstå forbindelsen er det vigtigt først at kende de to sygdomme hver for sig. Leddegigt (reumatoid artritis) er en kronisk autoimmun sygdom, hvor kroppens immunforsvar fejlagtigt angriber sine egne led. Dette fører til inflammation, smerte, stivhed og over tid, ødelæggelse af brusk og knogler i leddene. Det er en systemisk sygdom, der kan påvirke hele kroppen.
Paradentose (parodontitis) er en alvorlig tandkødsinfektion, der ødelægger det bløde væv og knoglen, som støtter tænderne. Den starter ofte som tandkødsbetændelse (gingivitis) og udvikler sig, hvis den ikke behandles. I de dybe tandkødslommer, der dannes, trives anaerobe bakterier – bakterier, der lever uden ilt. En af de mest berygtede af disse er Porphyromonas gingivalis.
Porphyromonas gingivalis: En Nøgleaktør i Munden
P. gingivalis er en af hovedårsagerne til kronisk paradentose. Denne bakterie er særligt dygtig til at manipulere værtens immunforsvar for at skabe et miljø, hvor den kan trives. Den producerer en række enzymer og toksiner, der nedbryder væv og fremmer en vedvarende, lavgradig inflammation. Men dens indflydelse stopper ikke ved mundhulen. Forskning viser, at denne bakterie og de inflammatoriske signaler, den skaber, kan trænge ind i blodbanen og påvirke andre dele af kroppen, herunder leddene.
Den Biokemiske Forbindelse: Citrullinering
Den mest afgørende opdagelse, der forbinder P. gingivalis med leddegigt, er en proces kaldet citrullinering. Dette er en post-translationel modifikation, hvor aminosyren arginin i et protein omdannes til aminosyren citrullin. I menneskekroppen udføres denne proces af vores egne enzymer kaldet Peptidyl-arginin deiminaser (PAD'er) og er vigtig for mange normale fysiologiske processer.
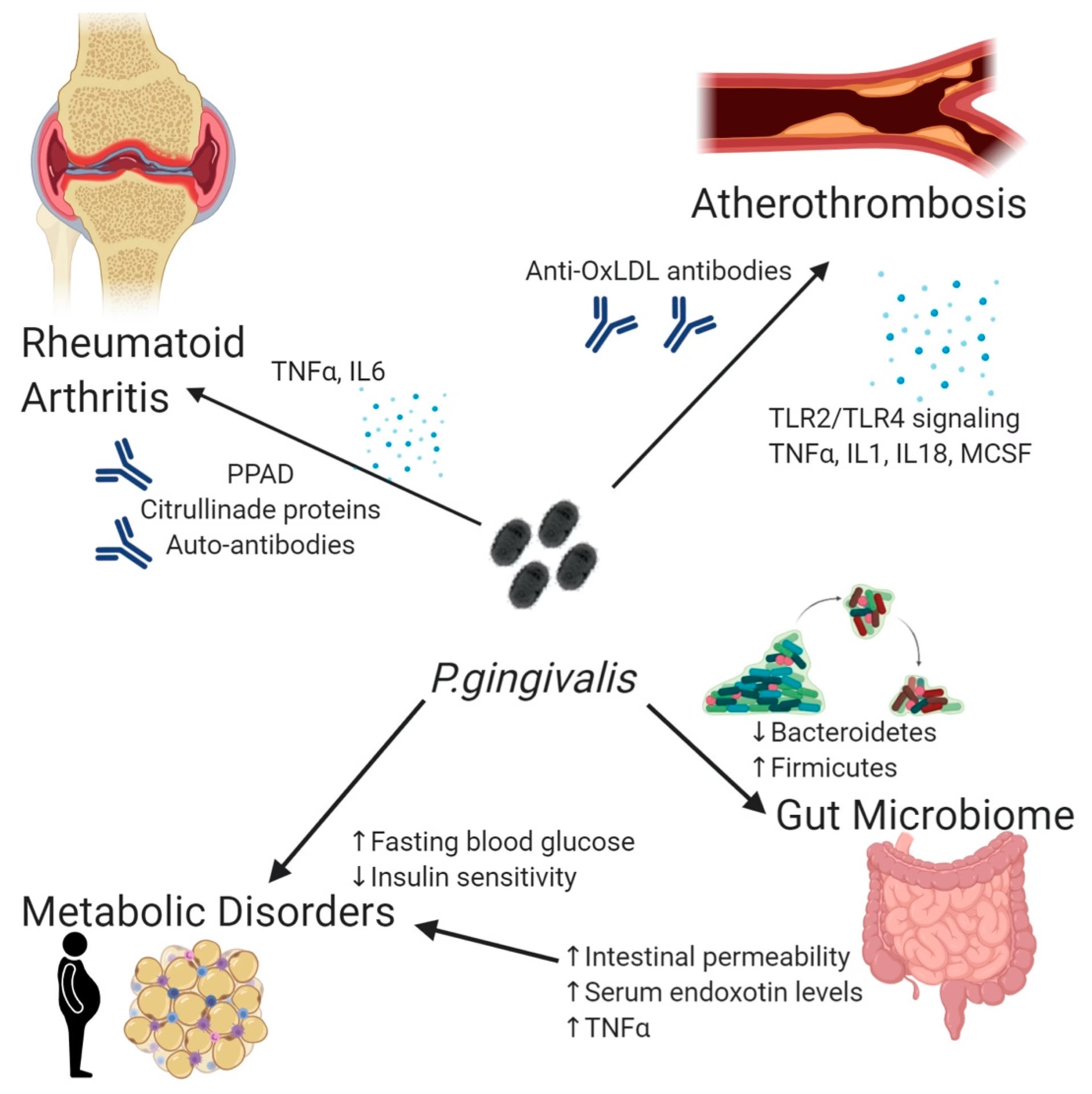
Problemet opstår, når denne proces løber løbsk. Ved leddegigt reagerer immunforsvaret på disse citrullinerede proteiner, som om de var fremmede. Kroppen begynder at producere antistoffer mod dem, kendt som anti-citrullinerede protein-antistoffer (ACPA). Disse antistoffer er en meget specifik markør for leddegigt og kan ofte påvises i blodet flere år før, symptomerne på sygdommen viser sig.
Her kommer P. gingivalis ind i billedet på en helt unik måde. Som den eneste kendte prokaryot (bakterie) producerer P. gingivalis sit eget PAD-enzym, kaldet PPAD (Porphyromonas gingivalis Peptidyl-arginin deiminase). Dette bakterielle enzym er i stand til at citrullinere både bakteriens egne proteiner og værtens (menneskets) proteiner. Denne handling kan være den tændsats, der starter den autoimmune reaktion. Ved at skabe en overflod af citrullinerede proteiner i tandkødet, kan P. gingivalis potentielt "træne" immunforsvaret til at angribe disse proteiner. Når immunforsvaret senere støder på lignende, naturligt forekommende citrullinerede proteiner i leddene, kan det udløse det ødelæggende angreb, der kendetegner leddegigt.
Beviser fra Dyremodeller
For at bevise denne hypotese har forskere udført studier på mus, der er genetisk disponerede for at udvikle en form for leddegigt (kollagen-induceret artritis, CIA). Resultaterne er slående:
- Mus inficeret med en levende, normal stamme af P. gingivalis udviklede leddegigt tidligere, med hurtigere progression og med en markant højere sværhedsgrad end ikke-inficerede mus.
- De inficerede mus viste signifikant mere knogle- og bruskødelæggelse i deres led.
- Mest afgørende var, at da forskerne inficerede mus med en genetisk modificeret P. gingivalis-stamme, der manglede PPAD-enzymet, så man ingen forværring af leddegigten. Sygdommen udviklede sig på samme måde som hos de ikke-inficerede kontrolmus.
Disse resultater peger direkte på, at det er bakteriens evne til at citrullinere proteiner via sit PPAD-enzym, der er den mekanistiske forbindelse til forværringen af leddegigt. Studierne viste også, at kun mus inficeret med den normale P. gingivalis-stamme udviklede høje niveauer af de leddegigt-specifikke ACPA-antistoffer.
Sammenligning af Infektionseffekter i Musestudier
| Karakteristikum | Infektion med Normal P. gingivalis (med PPAD) | Infektion med P. gingivalis (uden PPAD) |
|---|---|---|
| Start på Leddegigt | Tidligere | Ingen ændring |
| Sværhedsgrad af Leddegigt | Signifikant forværret | Ingen ændring |
| Knogleskade | Øget | Ingen ændring |
| Niveau af ACPA-antistoffer | Signifikant forhøjet | Ingen ændring |
Andre Sygdomsfremkaldende Mekanismer
Citrullinering er ikke den eneste måde, P. gingivalis bidrager til systemisk inflammation og leddestruktion. Bakterien har flere andre skadelige virkninger:
- Induktion af NETose: P. gingivalis kan få neutrofiler (en type hvide blodlegemer) til at gennemgå en proces kaldet NETose, hvor de udslynger deres DNA i et net-lignende struktur for at fange patogener. Disse net indeholder dog også pro-inflammatoriske proteiner, som kan forværre inflammationen.
- Fremme af Osteoklastogenese: Bakterien kan stimulere dannelsen af osteoklaster, de celler, der er ansvarlige for at nedbryde knoglevæv. Dette bidrager direkte til knogleerosionen, der ses både ved paradentose og leddegigt.
- Stimulering af Th17-respons: P. gingivalis fremmer en pro-inflammatorisk immunrespons (Th17), som er stærkt involveret i den autoimmune ødelæggelse ved leddegigt.
Ofte Stillede Spørgsmål (OSS)
Betyder det, at dårlig mundhygiejne direkte forårsager leddegigt?
Nej, ikke direkte. Leddegigt er en kompleks sygdom med mange medvirkende faktorer, herunder genetik og andre miljøpåvirkninger. Man skal sandsynligvis være genetisk disponeret for at udvikle sygdommen. P. gingivalis-infektion (altså alvorlig paradentose) ser dog ud til at fungere som en kraftig udløsende eller forværrende faktor hos disse disponerede individer. God mundhygiejne minimerer risikoen for paradentose og dermed eksponeringen for denne bakterie.
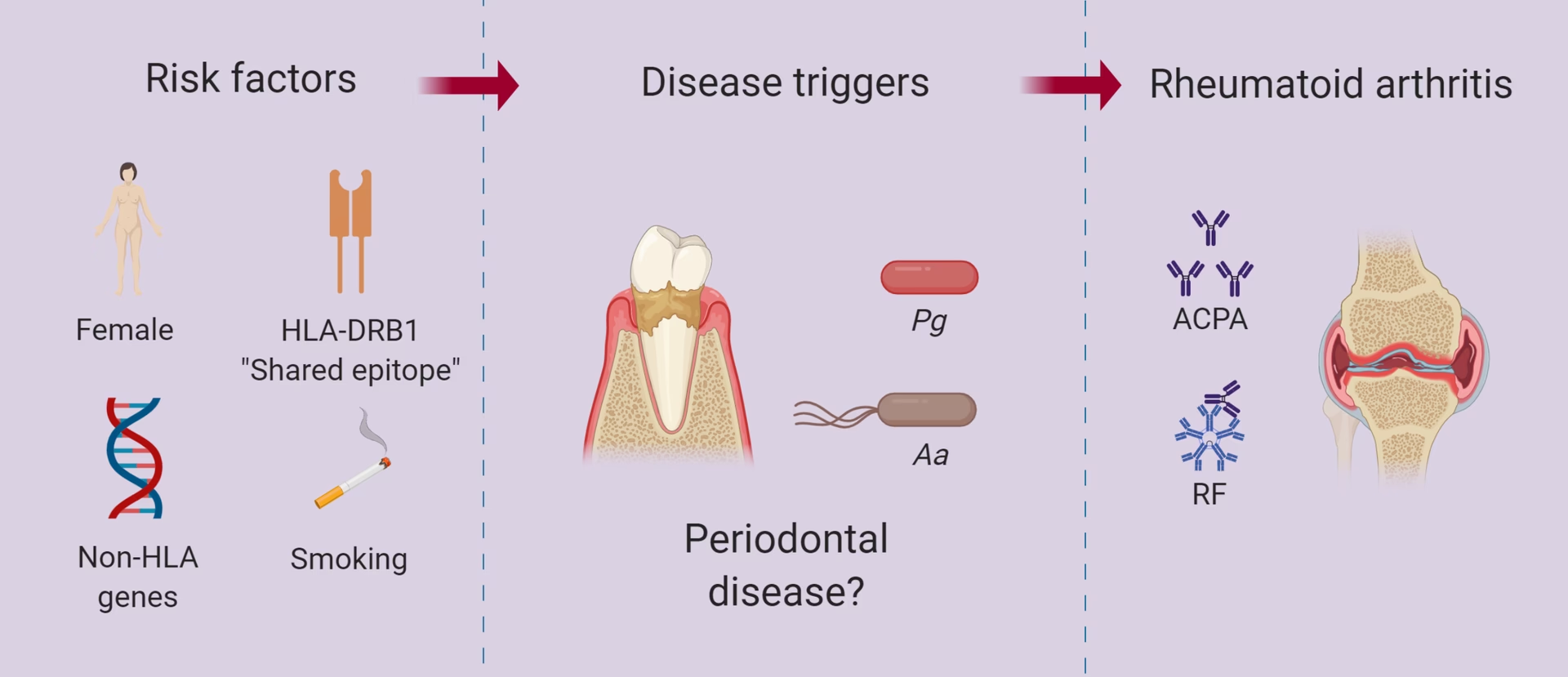
Kan behandling af min paradentose hjælpe på mine leddegigtsymptomer?
Flere kliniske studier peger i den retning. Behandling af paradentose reducerer den samlede inflammatoriske byrde i kroppen og fjerner en kilde til P. gingivalis. Mange patienter med leddegigt oplever en forbedring i deres ledsymptomer efter vellykket paradentosebehandling. Det er derfor afgørende for personer med leddegigt at få deres tandsundhed tjekket og behandlet regelmæssigt.
Er P. gingivalis den eneste kilde til citrullinering i kroppen?
Nej. Som nævnt har mennesker deres egne PAD-enzymer, som er nødvendige for normal funktion. Rygning er en anden kendt risikofaktor for leddegigt, og det menes, at det virker ved at øge aktiviteten af PAD-enzymer i lungerne, hvilket fører til citrullinering dér. Det unikke ved P. gingivalis er, at den introducerer en ekstern, bakteriel kilde til PAD-enzymer direkte i et kronisk betændt væv, hvilket skaber en vedvarende kilde til de antigener, der kan udløse autoimmunitet.
Konklusion: Mundsundhed er Generel Sundhed
Videnskaben har endegyldigt fastslået, at munden ikke er en isoleret del af kroppen. Den gamle mistanke om en forbindelse mellem tænder og led er nu underbygget af stærke biokemiske og immunologiske beviser. Porphyromonas gingivalis fremstår som en central aktør, der via sit unikke PPAD-enzym bygger en molekylær bro mellem infektion i tandkødet og autoimmun ødelæggelse i leddene. Denne viden understreger vigtigheden af grundig mundhygiejne og regelmæssig tandpleje, ikke kun for at bevare tænderne, men som en fundamental del af at forebygge og håndtere alvorlige systemiske sygdomme som leddegigt.
Hvis du vil læse andre artikler, der ligner Mundbakterie og Leddegigt: Den Skjulte Forbindelse, kan du besøge kategorien Sundhed.
