08/07/2025
Fremstillingen af medicinsk udstyr er en kompleks proces, hvor patientens sikkerhed og udstyrets pålidelighed er af allerhøjeste prioritet. Selv for de mest erfarne producenter kan det være en udfordring at udvikle og fremstille et stabilt og sikkert produkt gang på gang. Hvordan kan man sikre, at hvert enkelt apparat, der forlader produktionslinjen, yder præcist som forventet med minimal variation? Svaret ligger i en streng og systematisk tilgang kendt som procesvalidering. Dette er rammeværket, der sikrer, at hele fremstillingsprocessen er under kontrol og leverer forudsigelige resultater.
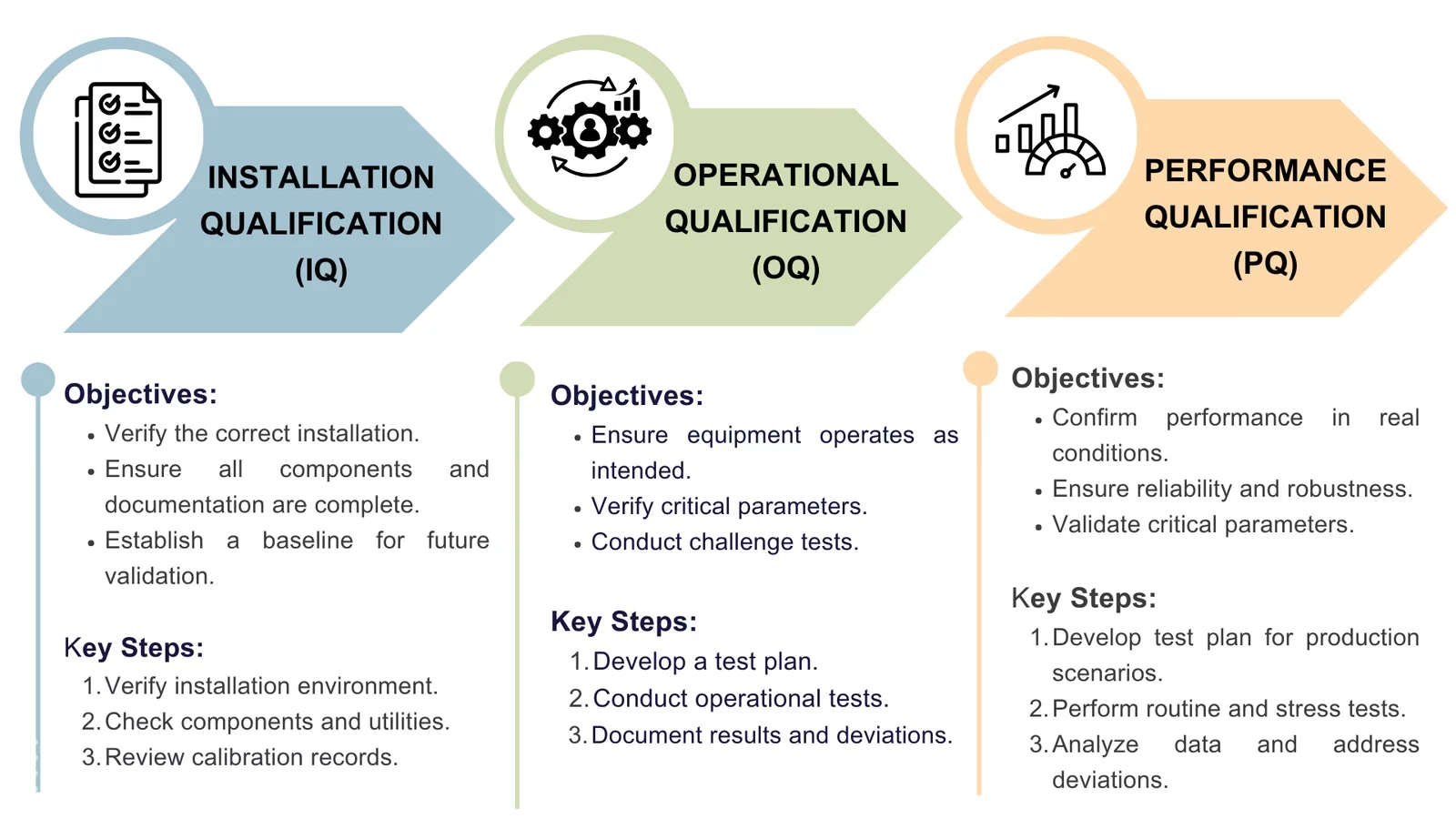
Procesvalidering er ikke en enkeltstående begivenhed, men en række faser, der beviser, at en produktionsproces konsekvent vil producere et produkt, der opfylder sine forudbestemte specifikationer og kvalitetsattributter. En af de mest kritiske faser i denne validering er Operationel Kvalificering, ofte forkortet OQ. Denne fase følger efter Installationskvalificering (IQ), hvor man bekræfter, at udstyret er installeret korrekt. OQ tager skridtet videre og tester, om udstyret rent faktisk fungerer korrekt under specificerede driftsbetingelser.
Hvad er Operationel Kvalificering (OQ)?
Operationel Kvalificering (OQ) er den dokumenterede verifikation af, at udstyret og dets delsystemer fungerer som forventet inden for de fastsatte operationelle grænser. Efter at have bekræftet, at alt er korrekt installeret (IQ-fasen), stiller OQ-fasen de afgørende spørgsmål: "Fungerer mit udstyr korrekt?" og "Hvad er udstyrets operationelle grænser?".
Ifølge den amerikanske fødevare- og lægemiddelmyndighed (FDA) defineres OQ som processen, der "...etablerer tillid til, at procesudstyr og delsystemer er i stand til konsekvent at fungere inden for angivne grænser og tolerancer." OQ bør udføres, hver gang nyt udstyr installeres, men også efter væsentlig vedligeholdelse eller modifikationer. Det kan også være en fast del af den planlagte kvalitetssikring.
Formålet med OQ er todelt:
- Identificere kritiske parametre og etablere et driftsvindue: Ved at forstå udstyrets præcise grænser kan producenten definere et sikkert 'vindue' af indstillinger (f.eks. temperatur, tryk, hastighed), hvor man med sikkerhed ved, at der kan produceres et konformt produkt hver eneste gang.
- Udfordre 'worst-case' betingelser: Processen testes under de mest ugunstige operationelle forhold. Dette inkluderer at køre udstyret ved de yderste grænser af det definerede driftsvindue. Ved at gøre dette demonstrerer man, at selv under de værst tænkelige, men stadig acceptable, forhold, vil resultatet stadig være et sikkert og effektivt medicinsk udstyr. Dette beviser processens robusthed.
Hvorfor er OQ afgørende for producenter?
At udføre en grundig OQ er ikke blot en formalitet; det er en fundamental del af kvalitetssikringen med flere betydelige fordele. For det første er det et lovkrav fra regulerende myndigheder som FDA. Manglende eller utilstrækkelig procesvalidering kan føre til alvorlige konsekvenser, herunder afvisning af produkter og juridiske sanktioner.
Ud over det regulatoriske aspekt er der flere praktiske fordele:
- Reduceret risiko for patienter og brugere: Den vigtigste fordel er risikoreduktion. Når et stykke medicinsk udstyr fungerer fejlfrit inden for sine specificerede grænser, minimeres risikoen for fejl, der kan skade patienter eller sundhedspersonale.
- Opdagelse af skjulte fejl: Uden OQ kan potentielle problemer med udstyret blive overset. En maskine kan umiddelbart synes at fungere, men små afvigelser i software, beskadigede komponenter eller workflow-problemer kan føre til alvorlige fejl på et senere tidspunkt. OQ er designet til at fange disse problemer, før produktet når markedet.
- Etablering af et pålideligt driftsvindue: OQ giver producenten en dyb forståelse for processens øvre og nedre grænser. Dette driftsvindue sikrer, at alle enheder, der fremstilles inden for disse rammer, vil fungere som tilsigtet, selv når de udsættes for varierende miljømæssige forhold.
- Forbedret sporbarhed og fejlfinding: Hvis der opstår et problem med et produkt ude hos brugeren, er den komplette valideringsdokumentation (inklusive IQ, OQ og PQ) et uvurderligt værktøj. Den giver myndigheder og producenten mulighed for at spore processen tilbage, identificere den grundlæggende årsag til fejlen og implementere korrigerende handlinger.
Processen for Operationel Kvalificering
En vellykket OQ-proces kræver en omhyggelig og systematisk plan. Generelt indeholder en OQ-protokol følgende aktiviteter:
- Identifikation af kritiske driftsparametre: Hvilke variable har en direkte indflydelse på produktkvaliteten? (f.eks. temperatur, tid, tryk, flowhastighed).
- Beskrivelse af eksperimenter: En detaljeret plan for, hvordan hver kritisk variabel vil blive testet.
- Fastlæggelse af testsekvens: Rækkefølgen af eksperimenterne skal være logisk og designet til at teste interaktioner mellem parametre.
- Specifikation af måleudstyr: Alt udstyr, der bruges til at måle og overvåge processen, skal være kalibreret og specificeret.
- Definition af acceptkriterier: Klare, målbare og forudbestemte kriterier for, hvornår en test er bestået.
Et praktisk eksempel: Varmeforsegling af steril emballage
Forestil dig en proces, hvor en steril pose til et medicinsk instrument skal forsegles. En svag forsegling kan kompromittere steriliteten, mens en for stærk forsegling kan gøre posen svær at åbne. Her er OQ afgørende.
- Inputfaktorer (kritiske parametre): Temperatur, tid og tryk på forseglingsmaskinen.
- Outputfaktor (resultat): Forseglingens styrke, målt i f.eks. Newton.
OQ-processen vil involvere testning ved de yderste grænser af disse parametre. For eksempel kan de øvre grænser være 160°C, 2,5 sekunder og 3,5 PSI. De nedre grænser kunne være 140°C, 1,5 sekunder og 2,5 PSI. Ved at teste kombinationer af disse 'worst-case' indstillinger og bekræfte, at forseglingens styrke stadig ligger inden for de acceptable grænser, beviser man, at processen er robust og pålidelig inden for hele dette driftsvindue.

Sammenligning af Valideringsfaser: IQ vs. OQ
For at skabe et klart overblik er det nyttigt at sammenligne Installationskvalificering (IQ) med Operationel Kvalificering (OQ), da de er tæt forbundne, men tjener forskellige formål.
| Aspekt | Installationskvalificering (IQ) | Operationel Kvalificering (OQ) |
|---|---|---|
| Formål | At verificere, at udstyret er installeret korrekt i henhold til producentens specifikationer. | At verificere, at udstyret fungerer korrekt og konsekvent inden for de definerede grænser. |
| Spørgsmål | "Er alt installeret som det skal?" | "Fungerer alt som det skal?" |
| Fokus | Statisk verifikation: korrekte kabler, softwareversion, placering, dokumentation. | Dynamisk testning: alarmer, knapper, procesparametre, 'worst-case' scenarier. |
| Timing | Udføres én gang ved installation eller flytning af udstyr. | Udføres efter IQ og gentages efter større vedligeholdelse eller modifikationer. |
Ofte Stillede Spørgsmål (FAQ)
Hvad er forskellen på IQ, OQ og PQ?
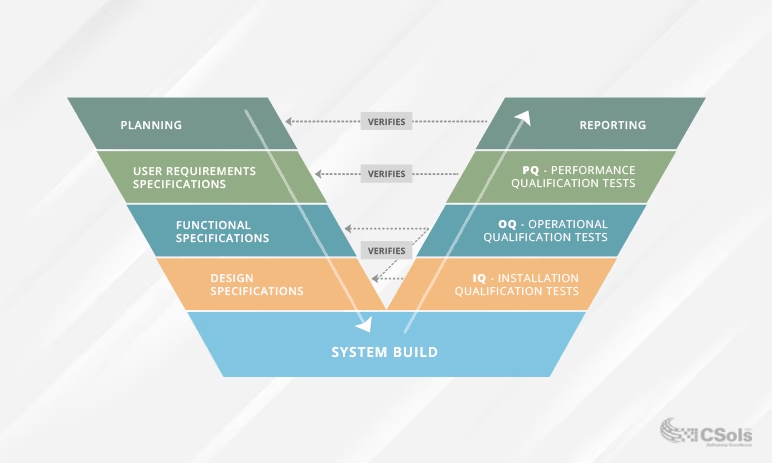
IQ (Installationskvalificering), OQ (Operationel Kvalificering) og PQ (Performance Kvalificering) er de tre hovedfaser i procesvalidering. IQ bekræfter korrekt installation. OQ bekræfter, at udstyret fungerer korrekt inden for sine grænser. PQ (Performance Kvalificering) er den sidste fase, som bekræfter, at processen konsekvent producerer et acceptabelt produkt under normale, reelle produktionsbetingelser over en længere periode. PQ tester processens langsigtede stabilitet.
Hvad sker der, hvis en OQ-test fejler?
Hvis en test fejler under OQ, skal processen stoppes. En grundig undersøgelse skal iværksættes for at finde årsagen til fejlen. Dette kan indebære justering af udstyret, ændring af procesparametre eller endda reparation. Når problemet er identificeret og løst, skal den relevante del af OQ-protokollen (eller hele protokollen) gentages for at dokumentere, at fejlen er rettet, og at udstyret nu opfylder acceptkriterierne.
Er OQ kun for nyt udstyr?
Nej. OQ er essentielt for alt nyt udstyr, men det er lige så vigtigt at gen-kvalificere udstyr efter væsentlige ændringer. Dette inkluderer softwareopdateringer, udskiftning af kritiske komponenter, flytning af udstyr eller ændringer i selve fremstillingsprocessen. Formålet er at sikre, at ændringerne ikke har påvirket udstyrets evne til at fungere korrekt og sikkert.
Afslutningsvis er Operationel Kvalificering en uundværlig søjle i fremstillingen af medicinsk udstyr. Det er den metodiske proces, der bygger bro mellem en korrekt installation og en pålidelig, konsekvent produktion. Ved at investere tid og ressourcer i en grundig OQ sikrer producenter ikke kun overholdelse af lovgivningen, men også, og vigtigst af alt, at de leverer sikre og effektive produkter, der forbedrer og redder liv.
Hvis du vil læse andre artikler, der ligner Operationel Kvalificering af Medicinsk Udstyr, kan du besøge kategorien Sundhed.