30/10/2006
Inden for fremstilling af medicinsk udstyr er præcision og pålidelighed ikke bare mål – de er absolutte krav. Et enkelt svigt i en produktionsproces kan have alvorlige konsekvenser for patienterne. For at garantere den højeste grad af sikkerhed og kvalitet anvender industrien en streng, tredelt valideringsproces kendt som IQ, OQ og PQ. Disse forkortelser står for Installation Qualification (Installationskvalificering), Operational Qualification (Operationel Kvalificering) og Performance Qualification (Performancekvalificering). Tilsammen udgør de rygraden i procesvalidering og sikrer, at alt udstyr, der anvendes til fremstilling, fungerer præcist som forventet – hver eneste gang.
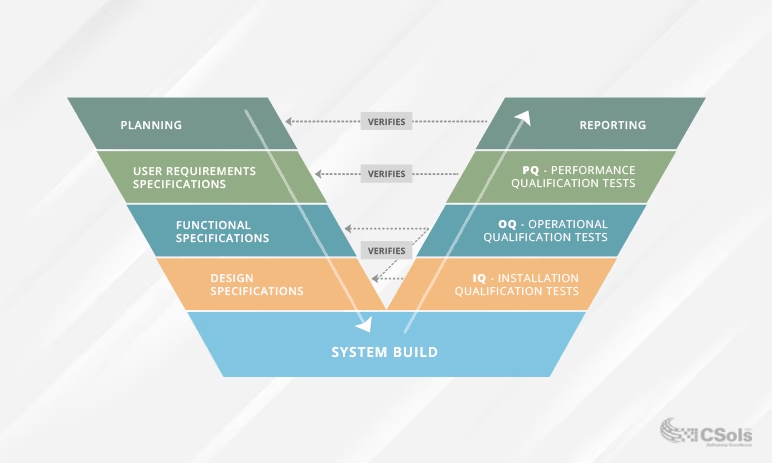
Denne artikel vil dykke ned i hver af disse faser, forklare deres formål, og hvordan de tilsammen skaber en robust ramme, der garanterer, at det endelige medicinske udstyr er både sikkert og effektivt for patienten.
- Hvad Betyder IQ, OQ, PQ og Procesvalidering?
- Installation Kvalificering (IQ): Fundamentet for Succes
- Operationel Kvalificering (OQ): Test af Grænserne
- Performance Kvalificering (PQ): Bevis for Konsistent Kvalitet
- Sammenligning af IQ, OQ og PQ
- Hvornår er Procesvalidering Nødvendig?
- Ofte Stillede Spørgsmål (FAQ)
Hvad Betyder IQ, OQ, PQ og Procesvalidering?
Ifølge FDA's vejledning er procesvalidering defineret som "indsamling og evaluering af data, fra procesdesignfasen til kommerciel produktion, som etablerer videnskabeligt bevis for, at en proces er i stand til konsekvent at levere et kvalitetsprodukt." For at opnå dette skal producenterne omhyggeligt udføre og dokumentere de tre kvalificeringsfaser på det udstyr, der anvendes i produktionen.
Det er afgørende at forstå, at disse faser skal udføres i en bestemt rækkefølge: Først IQ, derefter OQ, og til sidst PQ. Logikken er klar: Man kan ikke kvalificere driften af udstyret (OQ), før man har bekræftet, at det er korrekt installeret (IQ). Ligeledes kan man ikke kvalificere processens ydeevne under reelle forhold (PQ), før man har fastslået, at udstyret fungerer korrekt inden for sine operationelle grænser (OQ).
Installation Kvalificering (IQ): Fundamentet for Succes
Installationskvalificering (IQ) er den første og grundlæggende fase. Den besvarer det simple, men kritiske spørgsmål: "Er alt installeret korrekt?" Før man overhovedet kan begynde at teste udstyrets funktion, skal man have dokumenteret bevis for, at det er blevet leveret, installeret og konfigureret i fuld overensstemmelse med producentens specifikationer og virksomhedens egne krav.
En typisk IQ-protokol omfatter en detaljeret tjekliste, der verificerer en række punkter, herunder:
- Verifikation af leverance: Kontrol af, at alt indhold i pakken stemmer overens med pakkelisten.
- Inspektion for skader: Grundig gennemgang af udstyret for eventuelle transportskader.
- Korrekt placering: Sikring af, at hver enkelt del af udstyret er installeret på den korrekte fysiske placering.
- Tilslutninger: Kontrol af alle kabler, rør og andre forbindelser til andet udstyr for korrekt og sikker montering.
- Strømforsyning: Verifikation af, at udstyret er tilsluttet den korrekte strømkilde med den rette spænding.
- Miljømæssige forhold: Bekræftelse af, at driftsmiljøet (f.eks. temperatur, fugtighed) overholder producentens specifikationer.
- Dokumentation: Indsamling og organisering af alle manualer, certifikater, kalibreringsrapporter og anden nødvendig dokumentation.
- Softwareinstallation: Bekræftelse af, at al nødvendig software er installeret korrekt og er den rigtige version.
Når IQ-fasen er afsluttet med succes, har man en solid, dokumenteret base, der bekræfter, at udstyret er klar til den næste fase: den operationelle kvalificering.
Operationel Kvalificering (OQ): Test af Grænserne
Når udstyret er korrekt installeret, går man videre til Operationel Kvalificering (OQ). Denne fase besvarer spørgsmålene: "Fungerer alt korrekt?" og "Hvad er de operationelle grænser for dette udstyr?" Formålet med OQ er at udfordre udstyret og processen ved at teste det under dets yderste operationelle grænser, ofte omtalt som worst-case scenarier. Dette gøres for at fastslå, at processen kan levere et acceptabelt produkt, selv når parametrene er sat til deres minimums- og maksimumsværdier.
Det er vigtigt at bemærke, at OQ er en formel testfase, ikke en udviklingsfase. Procesparametrene og deres grænser bør være defineret under procesudviklingen, som finder sted *før* den formelle kvalificering starter. Desværre ses det ofte, at virksomheder forsøger at udvikle processen under OQ, hvilket er en forkert praksis.
OQ involverer test af alle udstyrets funktioner, som kan omfatte:
- Alarmer og displays (f.eks. LED-indikatorer, lydsignaler).
- Styring af temperatur og tryk.
- Kontrolsystemer for fugtighed.
- Motorhastigheder og servomotorer.
- Timere og aktivitetsudløsere.
Proces OQ vs. Udstyr OQ
Man skelner sommetider mellem en 'Proces OQ' og en 'Udstyr OQ'. Forskellen er ligetil: Mens en Proces OQ udfordrer selve *processen* ved at indstille procesparametrene til deres yderpunkter, udfordrer en Udstyr OQ selve *udstyret* ved at teste det ved dets tekniske grænser som specificeret af producenten. Udstyr OQ kan ses som en udvidet del af IQ, hvor man bekræfter, at udstyret fungerer som lovet.

Performance Kvalificering (PQ): Bevis for Konsistent Kvalitet
Performance Kvalificering (PQ) er den sidste og afgørende fase i valideringsprocessen. Den besvarer spørgsmålene: "Producerer denne proces konsekvent det korrekte resultat?" og "Er denne proces sikker og stabil under normale driftsforhold?"
Mens OQ tester processen under ekstreme forhold, verificerer PQ, at processen leverer et produkt af høj konsistens under reelle, normale produktionsbetingelser. Dette betyder, at PQ skal udføres på den faktiske produktionsfacilitet, med trænet personale, og ved brug af de procedurer, materialer og det udstyr, der vil blive brugt til kommerciel produktion.
FDA anbefaler, at der udarbejdes en skriftlig PQ-protokol, som bør indeholde:
- En detaljeret beskrivelse af produktionsbetingelser, driftsparametre og anvendte råmaterialer.
- En plan for dataindsamling og evaluering.
- De specifikke tests, der skal udføres, og de tilhørende acceptkriterier.
- En omfattende stikprøveplan for at sikre kvalitet både inden for og mellem batches.
- Kriterier for videnskabs- og risikobaserede beslutninger om processens effektivitet.
- Valideringsstatus for de analysemetoder, der anvendes til at måle proces, materialer og slutprodukt.
- Gennemgang og godkendelse af protokollen af alle relevante afdelinger, herunder kvalitetsafdelingen.
Efter en vellykket PQ er processen officielt valideret, og man har stærk dokumentation for, at den er i stand til konsekvent at fremstille produkter, der lever op til alle forudbestemte specifikationer.
Sammenligning af IQ, OQ og PQ
For at give et klart overblik er her en tabel, der sammenligner de tre faser:
| Fase | Hovedspørgsmål | Formål | Eksempler |
|---|---|---|---|
| IQ (Installation) | Er alt installeret korrekt? | At verificere og dokumentere, at udstyret er installeret i henhold til producentens specifikationer. | Kontrol af strømforsyning, softwareversion, fysisk placering, dokumentation. |
| OQ (Operationel) | Fungerer alt korrekt ved sine grænser? | At udfordre processen ved dens operationelle yderpunkter (worst-case) for at definere et robust procesvindue. | Test af alarmer, motorhastigheder, temperaturkontrol ved min/max værdier. |
| PQ (Performance) | Leverer processen konsekvent et kvalitetsprodukt? | At demonstrere, at processen konsekvent producerer acceptable resultater under normale, reelle produktionsforhold. | Kørsel af flere produktionsbatches, stikprøvetagning, test af produktets holdbarhed. |
Hvornår er Procesvalidering Nødvendig?
Ifølge lovgivningen (f.eks. 21 CFR 820) skal procesvalidering udføres, "hvor resultaterne af en proces ikke fuldt ud kan verificeres ved efterfølgende inspektion og test." Dette gælder for mange kritiske processer i fremstillingen af medicinsk udstyr.
Eksempler på sådanne processer inkluderer:
- Steril forsegling af emballage: Man kan ikke teste styrken af hver forsegling uden at ødelægge den sterile barriere. Derfor validerer man selve forseglingsprocessen for at have tillid til, at hver eneste forsegling er intakt.
- Svejsning og lodning: Det er ofte umuligt at inspicere den indre kvalitet af en svejsning uden destruktiv test.
- Sprøjtestøbning: Selvom man kan måle det færdige produkt, kan interne spændinger eller mikroskopiske fejl, der stammer fra processen, ikke altid detekteres.
I disse tilfælde er en robust procesvalidering (IQ, OQ, PQ) den eneste måde at sikre, at slutproduktet konsekvent lever op til kvalitetskravene.
Ofte Stillede Spørgsmål (FAQ)
Hvad sker der, hvis man springer en af faserne over?
At springe en fase over, eller udføre dem i den forkerte rækkefølge, underminerer hele valideringsprocessen. Det er et alvorligt brud på regulatoriske krav og kan føre til usikre produkter. Uden en korrekt IQ har man intet grundlag for at stole på OQ-resultaterne, og uden en vellykket OQ kan man ikke garantere, at processen er robust nok til PQ. Rækkefølgen IQ -> OQ -> PQ er obligatorisk.
Hvem er ansvarlig for at udføre IQ, OQ og PQ?
Ansvaret ligger typisk hos et tværfunktionelt team. Dette team kan bestå af ingeniører fra produktion og udvikling, specialister fra kvalitetsafdelingen (QA), og operatører, der skal arbejde med udstyret. Samarbejde er nøglen til en vellykket validering.
Skal man validere igen, hvis man flytter udstyret?
Ja. Hvis et stykke valideret udstyr flyttes, skal der som minimum udføres en ny IQ for at bekræfte, at det er blevet geninstalleret korrekt. Afhængigt af risikoen og kompleksiteten af udstyret og processen kan det også være nødvendigt at udføre dele af eller en fuld OQ og PQ for at sikre, at flytningen ikke har påvirket udstyrets funktion og ydeevne.
Er OQ kun en test af 'worst-case' scenarier?
Ja, det er dens primære formål. Ved at teste processen ved dens yderste grænser (f.eks. højeste temperatur og korteste tid vs. laveste temperatur og længste tid) fastlægger man et "procesvindue", inden for hvilket man med sikkerhed ved, at processen fungerer. Dette giver en robusthed og en tillid til, at små, normale variationer i produktionen ikke vil føre til et defekt produkt.
Hvis du vil læse andre artikler, der ligner IQ, OQ, PQ: Validering af medicinsk udstyr, kan du besøge kategorien Sundhed.

