18/03/2014
I den komplekse verden af medicin og farmakologi er det afgørende at forstå præcist, hvordan et lægemiddel interagerer med kroppen for at frembringe en ønsket effekt. En af de mest fundamentale interaktioner sker, når et molekyle, kendt som en agonist, binder sig til en receptor på en celle og aktiverer den. Tænk på det som en nøgle (agonisten), der passer ind i en lås (receptoren) og drejer den for at åbne en dør (udløse en biologisk respons). Men ikke alle nøgler drejer låsen lige effektivt. For at kvantificere og forudsige denne proces bruger forskere matematiske rammer, og en af de mest centrale er den operationelle model for agonisme. Denne model er et kraftfuldt værktøj, der hjælper os med at dissekere og forstå de finere detaljer i, hvordan medicin virker på et molekylært niveau.
Hvad er den Operationelle Model for Agonisme?
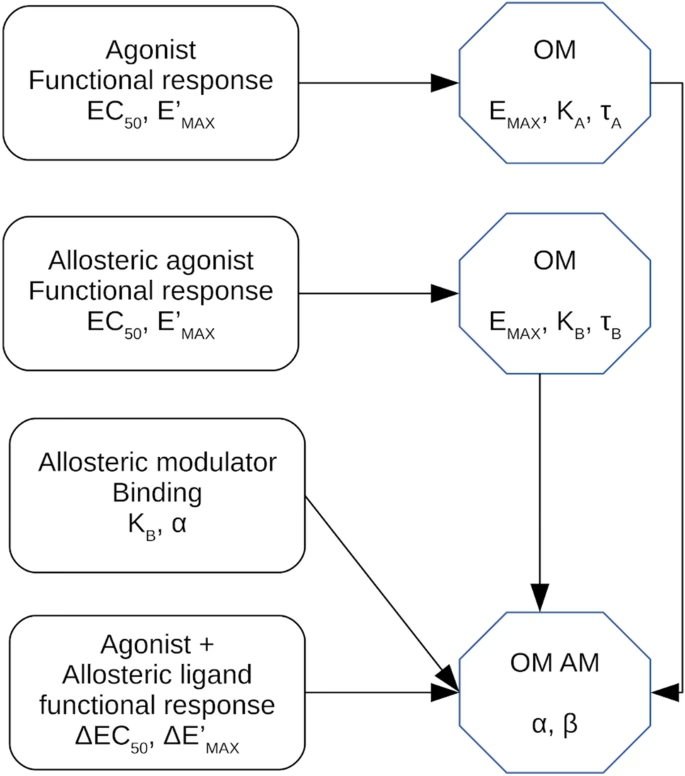
Den operationelle model for agonisme (OM) er en matematisk formel, der beskriver forholdet mellem koncentrationen af et lægemiddel og den biologiske respons, det fremkalder. Modellen tager højde for tre kritiske parametre, der tilsammen definerer en agonists unikke profil:
- Affinitet (KA): Dette er et mål for, hvor stærkt en agonist binder sig til sin receptor. En høj affinitet (lav KA-værdi) betyder, at lægemidlet er meget "klæbrigt" og binder sig effektivt til receptoren, selv ved lave koncentrationer. Det svarer til, hvor godt nøglen passer ind i låsen.
- Maksimal Systemrespons (EMAX): Dette repræsenterer den absolut maksimale effekt, som det biologiske system (f.eks. en celle eller et væv) kan producere, uanset hvor kraftig agonisten er. Det er den øvre grænse for systemets kapacitet.
- Operationel Effektivitet (τ, tau): Dette er måske den mest interessante parameter. Effektivitet beskriver agonistens evne til at aktivere receptoren, efter den har bundet sig. Det er et mål for agonistens iboende "power". En agonist med høj effektivitet kan fremkalde en stærk respons, selv når kun en lille brøkdel af receptorerne er optaget. Det svarer til, hvor let nøglen drejer låsen, når den først er sat i.
Kombinationen af disse tre faktorer giver et detaljeret billede af, hvordan et lægemiddel vil opføre sig. Modellen giver forskere mulighed for at sammenligne forskellige lægemiddelkandidater objektivt og forudsige deres potentiale som terapeutiske midler.
Udfordringen: Parametrenes Komplekse Samspil
Selvom den operationelle model er utroligt nyttig, har den en indbygget matematisk udfordring: de tre kerneparametre (KA, EMAX og τ) er indbyrdes afhængige. Det betyder, at når man forsøger at bestemme dem alle på én gang ud fra et enkelt eksperiment, kan de "forvirre" hinanden. En lille fejl i estimeringen af én parameter kan føre til store fejl i de andre.
Forestil dig, at du ser en bil accelerere og ud fra den ene observation skal bestemme bilens vægt, motorens hestekræfter og dækkenes vejgreb. Det er svært at adskille, hvilken faktor der bidrager mest til accelerationen. På samme måde kan det i et farmakologisk eksperiment være svært at skelne mellem, om en stærk respons skyldes, at lægemidlet binder meget stærkt (høj affinitet), eller om det er ekstremt godt til at aktivere receptoren (høj effektivitet). Denne usikkerhed gør det vanskeligt at opnå pålidelige og reproducerbare resultater, især når man analyserer data fra et enkelt koncentrations-respons-eksperiment.
En Mere Robust Løsning: Den Trinvise Analysemetode
For at overvinde denne udfordring har forskere udviklet en mere sofistikeret og robust analyseprocedure. I stedet for at forsøge at finde alle parametre på én gang, nedbrydes problemet i flere håndterbare trin. Denne metode giver langt mere præcise og pålidelige estimater.
Metoden fungerer typisk således:
- Indsamling af omfangsrige data: Først udføres en række eksperimenter. Dette kan involvere test af den samme agonist på forskellige cellelinjer, der udtrykker varierende antal receptorer, eller test af flere forskellige agonister på det samme system.
- Bestemmelse af tilsyneladende værdier: For hver enkelt koncentrations-respons-kurve bestemmes to "tilsyneladende" værdier: den maksimale observerede respons (E'MAX) og den koncentration, der giver halvdelen af denne respons (EC50). Disse værdier kan bestemmes med høj præcision.
- Afsløring af de sande systemparametre: Nu kommer det smarte trick. Ved at plotte de tilsyneladende maksimale responser (E'MAX) mod de tilsvarende EC50-værdier fra alle eksperimenterne, opstår et nyt mønster. En specifik matematisk ligning kan tilpasses dette nye plot, og ud fra denne analyse kan man med stor nøjagtighed bestemme de to sande, underliggende parametre: systemets reelle maksimale respons (EMAX) og agonistens sande affinitet (KA).
- Præcis beregning af effektivitet: Med EMAX og KA nu fastlagt og "låst", går man tilbage til de oprindelige data. Den operationelle model anvendes igen, men denne gang er det kun den operationelle effektivitet (τ), der er ukendt. Da de andre parametre er kendte, kan τ nu beregnes med en hidtil uset præcision.
Denne trinvise tilgang fjerner den usikkerhed, der plagede den direkte metode, og giver forskerne et solidt fundament for at karakterisere og sammenligne lægemidler.
Validering i Laboratoriet med Muskarinreceptorer
For at bevise værdien af denne nye metode blev den testet i praksis. Forskere brugte cellelinjer, der var genetisk modificeret til at udtrykke muskarinreceptorer (specifikt M2 og M4-typerne), som er vigtige mål for lægemidler i centralnervesystemet. Ved at skabe flere versioner af disse cellelinjer med forskellige mængder af receptorer, kunne de skabe det ideelle system til at teste modellen.

De testede en række kendte muskarinagonister, herunder lægemidler som carbachol, oxotremorin og pilocarpin. De målte den funktionelle respons på tre forskellige måder: ved at måle G-protein-aktivering ([35S]GTPγS-binding), produktion af inositolfosfater (IPX) og ændringer i intracellulært calcium. Resultaterne var entydige: den trinvise analysemetode gav konsekvent mere stabile og pålidelige værdier for lægemidlernes effektivitet (τ) sammenlignet med traditionelle metoder. Dette bekræftede, at metoden ikke kun er teoretisk elegant, men også praktisk overlegen til at analysere komplekse farmakologiske data.
Sammenligning af Analysemetoder
| Egenskab | Traditionel Direkte Tilpasning | Ny Trinvis Metode |
|---|---|---|
| Nøjagtighed af Parametre | Lav til variabel; stor fejlmargin | Høj; signifikant reduceret fejlmargin |
| Pålidelighed | Afhængig af startestimater; kan give forkerte resultater | Robust og uafhængig af startestimater |
| Krav til Data | Kan give upålidelige resultater fra enkelte kurver | Kræver flere datasæt (f.eks. forskellige receptor-niveauer) for optimal præcision |
Ofte Stillede Spørgsmål
Hvorfor er denne model vigtig for lægemiddeludvikling?
Denne model er fundamental for moderne lægemiddeludvikling. Den giver forskere mulighed for præcist at kvantificere og sammenligne potentielle lægemiddelkandidater. Ved at bestemme affinitet og effektivitet kan de udvælge de stoffer, der har den mest ønskværdige profil for et givent sygdomsmål. Det hjælper med at forudsige, hvordan et lægemiddel vil opføre sig in vivo, og reducerer risikoen for at investere tid og ressourcer i ineffektive kandidater. Præcision i disse tidlige faser er nøglen til at udvikle sikrere og mere effektive lægemidler.
Hvad er forskellen på affinitet (KA) og effektivitet (τ)?
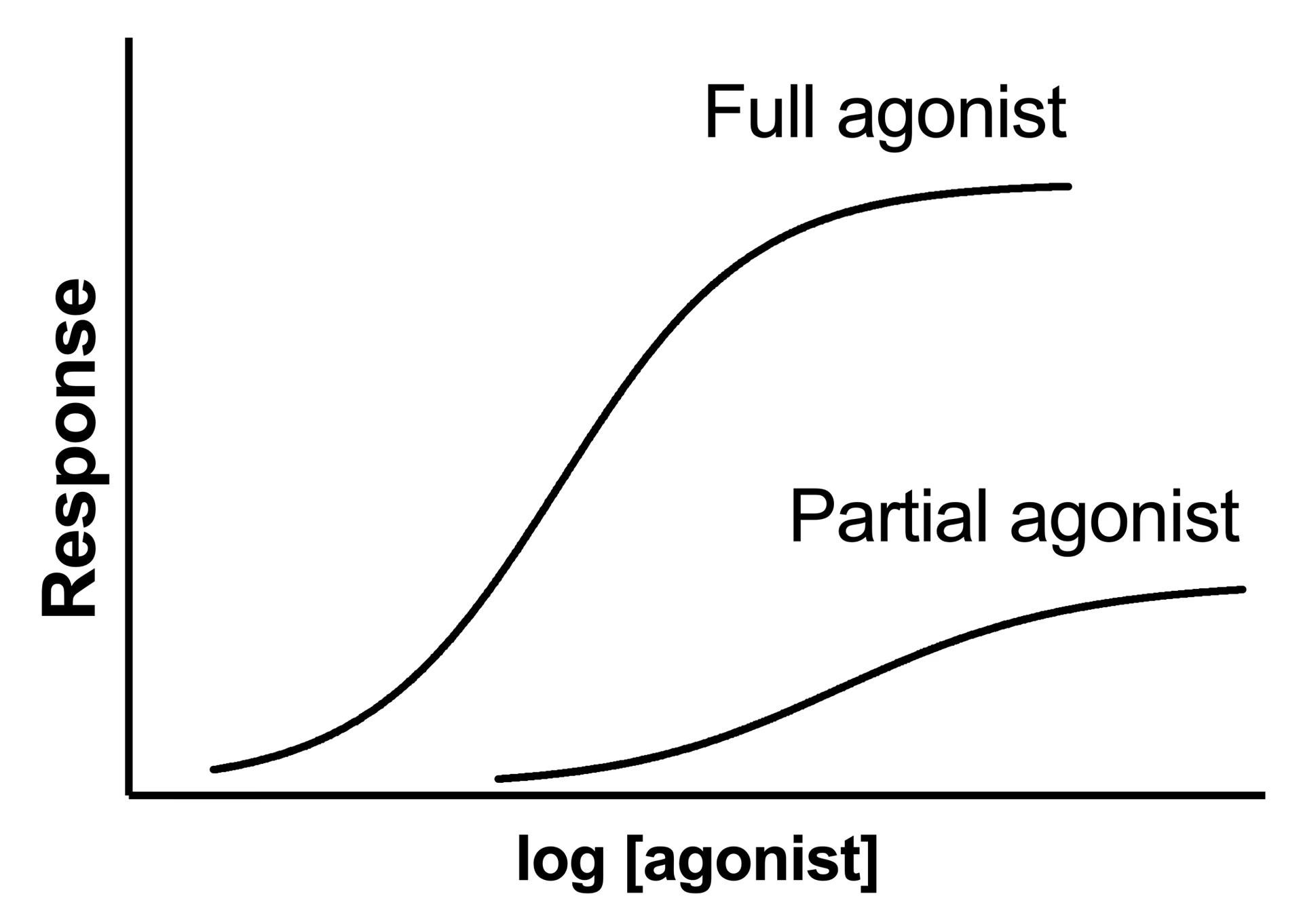
Det er en kritisk skelnen. Lad os vende tilbage til nøgle-og-lås-analogien. Affinitet (KA) beskriver, hvor perfekt nøglen passer i låsen. En nøgle med høj affinitet glider let ind og sidder fast. Effektivitet (τ) beskriver, hvor godt nøglen er i stand til at dreje om og åbne døren, når den først er inde i låsen. Et lægemiddel kan have meget høj affinitet (passer perfekt) men lav effektivitet (drejer kun låsen en smule). Sådanne stoffer kaldes "partielle agonister". Et andet lægemiddel kan have lavere affinitet men ekstremt høj effektivitet, hvilket gør det til en "fuld agonist". Modellen hjælper med at adskille disse to afgørende egenskaber.
Gælder denne model for alle typer medicin?
Den operationelle model er specifikt designet til at beskrive agonister – stoffer, der aktiverer en receptor. Dette dækker en enorm klasse af lægemidler, herunder mange medikamenter til behandling af astma, hjertesygdomme, psykiske lidelser og smerter. Modellen gælder dog ikke for alle lægemiddelmekanismer. For eksempel virker antagonister ved at blokere en receptor (som en nøgle, der passer i låsen, men ikke kan dreje), og enzymerhæmmere virker ved at blokere et enzyms funktion. For disse mekanismer anvendes andre, specialiserede matematiske modeller.
I sidste ende repræsenterer den operationelle model og de forfinede metoder til dens anvendelse et stort fremskridt inden for farmakologien. Evnen til præcist at måle og forstå de fundamentale interaktioner mellem et lægemiddel og dets mål i kroppen er hjørnestenen i rationel lægemiddeldesign. Hver forbedring i vores modelleringsværktøjer bringer os et skridt tættere på at udvikle den næste generation af medicin, der er mere målrettet, mere effektiv og mere sikker for patienterne.
Hvis du vil læse andre artikler, der ligner Den Operationelle Model for Agonisme Forklaret, kan du besøge kategorien Sundhed.