09/12/2015
Når du står på apoteket for at hente en receptpligtig medicin eller køber en pille i håndkøb, tænker du sjældent over den utrolige rejse, det pågældende lægemiddel har været på. Det er en rejse, der strækker sig over år, koster milliarder af kroner og involverer tusindvis af forskere, læger og patienter. Denne komplekse proces kaldes Forskning og Udvikling (F&U), og den er hjørnestenen i moderne medicin. Uden den ville vi ikke have de behandlinger, vi i dag tager for givet, fra antibiotika og vacciner til avanceret kræftmedicin. Men hvad indebærer denne proces egentlig, og hvordan måler man succesen af en så enorm investering?
Hvad er Forskning og Udvikling (F&U) i Lægemiddelindustrien?
Forskning og Udvikling inden for sundhedssektoren er den systematiske proces, hvor nye lægemidler, behandlinger og medicinsk udstyr opdages, testes og godkendes til brug for patienter. Det er en yderst reguleret og omkostningstung proces, der kan opdeles i flere afgørende faser, som hver især bærer en betydelig risiko for fiasko.
Fase 1: Grundforskning og Opdagelse
Alt starter med en idé. Forskere på universiteter, hospitaler og i medicinalvirksomheder arbejder på at forstå sygdomme på et molekylært niveau. De identificerer et 'mål' – for eksempel et specifikt protein eller gen, der spiller en central rolle i en sygdom. Herefter begynder jagten på et molekyle eller en kemisk forbindelse, der kan påvirke dette mål på en positiv måde. Tusindvis, nogle gange millioner, af forbindelser screenes, før man finder nogle få lovende kandidater.
Fase 2: Prækliniske Studier
Før et potentielt lægemiddel kan testes på mennesker, skal det gennemgå omfattende prækliniske tests. Dette sker typisk i laboratoriet (in vitro) og i dyremodeller (in vivo). Formålet er at fastslå, om stoffet er sikkert, og om det har den ønskede effekt. Forskere undersøger toksicitet, hvordan stoffet optages, fordeles og udskilles af kroppen, og hvilken dosis der er mest effektiv. Kun en brøkdel af de stoffer, der når denne fase, viser sig at være sikre og effektive nok til at gå videre til test i mennesker.
Fase 3: Kliniske Forsøg
Dette er den længste og dyreste del af processen. Kliniske forsøg udføres på mennesker og er opdelt i tre (nogle gange fire) faser:
- Fase I: Lægemidlet testes på en lille gruppe raske, frivillige personer (typisk 20-80). Hovedformålet er at vurdere sikkerheden, identificere bivirkninger og bestemme den korrekte dosering.
- Fase II: Her testes lægemidlet på en større gruppe patienter (typisk 100-300), der lider af den sygdom, behandlingen er rettet imod. Målet er at vurdere lægemidlets effektivitet og fortsat overvåge dets sikkerhed.
- Fase III: Dette er store, afgørende studier, der involverer tusindvis af patienter på tværs af mange hospitaler og lande. Lægemidlet sammenlignes ofte med en eksisterende standardbehandling eller placebo (en pille uden aktivt stof) for endegyldigt at bevise dets effekt og sikkerhed. Resultaterne fra Fase III-studier er afgørende for, om myndighederne vil godkende medicinen.
Fase 4: Godkendelse og Overvågning
Hvis et lægemiddel succesfuldt gennemgår alle tre faser af kliniske forsøg, kan medicinalfirmaet indsende en ansøgning om markedsføringstilladelse til de relevante sundhedsmyndigheder, såsom Lægemiddelstyrelsen i Danmark eller Det Europæiske Lægemiddelagentur (EMA). Myndighederne gennemgår omhyggeligt alle data fra forskningen for at sikre, at fordelene ved medicinen opvejer risiciene. Selv efter godkendelse fortsætter overvågningen (Fase IV) for at fange sjældne eller langsigtede bivirkninger, når medicinen bruges af en meget større population.
Måling af Succes: En Balance mellem Sundhed og Økonomi
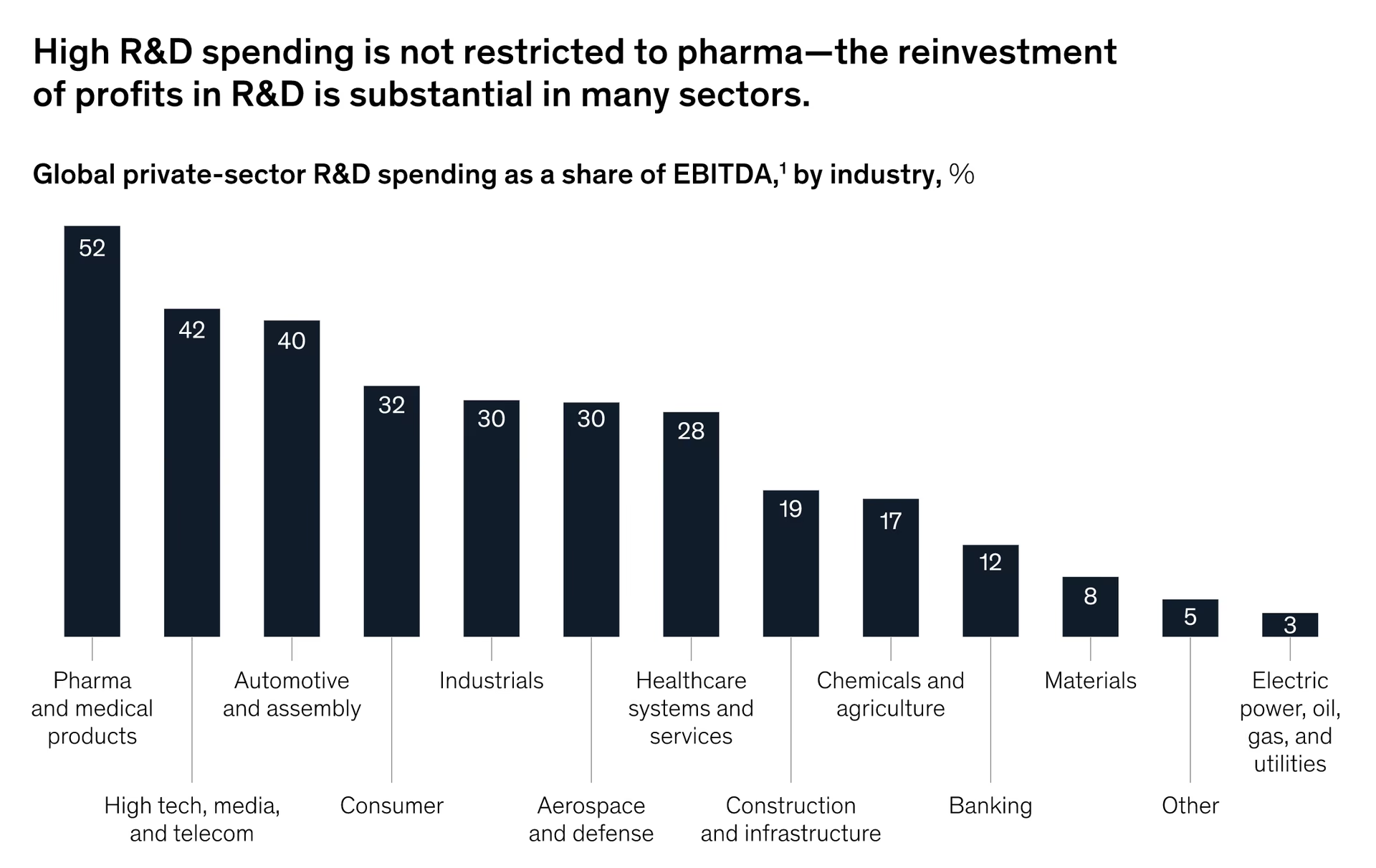
Med en udviklingsproces, der kan tage 10-15 år og koste over 15 milliarder kroner, er det klart, at F&U er en enorm økonomisk satsning for medicinalvirksomheder. Hvordan måler man så, om en så stor investering betaler sig? Her kan man skele til et finansielt nøgletal kendt som 'Return on Research Capital' (RORC), eller afkast af forskningskapital.

RORC giver et billede af, hvor meget profit der genereres for hver krone, der er brugt på F&U i en tidligere periode. Udregningen er simpel:
Indeværende års bruttofortjeneste / Forrige års F&U-udgifter
Selvom dette er et forretningsværktøj, illustrerer det den økonomiske virkelighed, der driver innovationen. Et firma, der udvikler et 'blockbuster'-lægemiddel mod en udbredt sygdom som forhøjet kolesterol eller diabetes, vil have en meget høj RORC. Dette overskud er ikke kun til gavn for aktionærerne; det er også afgørende for at kunne finansiere forskning i nye, måske mere sjældne, sygdomme, hvor den kommercielle rentabilitet er lavere. Omvendt vil et firma, hvis lovende kræftmiddel fejler i et sent Fase III-studie, lide et enormt økonomisk tab, hvilket understreger den høje risiko i branchen.
En Tidslinje for Udvikling af Lægemidler
For at give et bedre overblik over den lange rejse er her en typisk tidslinje for udviklingen af et nyt lægemiddel.
| Fase | Estimeret Tidsramme | Primært Formål |
|---|---|---|
| Grundforskning | 2-5 år | Forstå sygdommen og identificere potentielle lægemiddelkandidater. |
| Prækliniske Studier | 1-2 år | Teste sikkerhed og effekt i laboratorie- og dyreforsøg. |
| Kliniske Forsøg: Fase I | ~1 år | Vurdere sikkerhed og dosering på en lille gruppe raske frivillige. |
| Kliniske Forsøg: Fase II | 2-3 år | Teste effekt og bivirkninger på en mindre gruppe patienter. |
| Kliniske Forsøg: Fase III | 3-5 år | Bekræfte effekt og sikkerhed i en stor, international patientgruppe. |
| Godkendelsesproces | 1-2 år | Myndighedernes grundige gennemgang af al dokumentation. |
| Overvågning (Fase IV) | Løbende | Indsamle data om langsigtede effekter og sjældne bivirkninger. |
Hvorfor er F&U Vigtigt for Dig som Patient?
I sidste ende handler alt dette om én ting: at forbedre livet for patienten. Uden den vedholdende og dyre F&U-proces ville vi ikke have de behandlinger, der har udryddet sygdomme som kopper, gjort HIV til en kronisk i stedet for en dødelig sygdom, og markant forbedret overlevelsesraten for mange kræftformer. Hver gang en læge udskriver en recept, og hver gang du henter medicin på dit lokale apotek, er det kulminationen på årtiers videnskabeligt arbejde. Hospitaler spiller en central rolle, ikke kun i behandlingen, men også som vitale centre for kliniske forsøg, hvor nye, lovende behandlinger testes i samarbejde med patienter.
Ofte Stillede Spørgsmål
Hvorfor er ny medicin så dyr?
Prisen på ny medicin afspejler de enorme omkostninger ved F&U-processen. For hvert lægemiddel, der kommer på markedet, er der ni andre, der er fejlet undervejs. Indtægterne fra det succesfulde lægemiddel skal dække omkostningerne til alle de mislykkede projekter samt finansiere forskningen i den næste generation af medicin.

Kan man stole på forskningen fra medicinalfirmaer?
Ja, processen er underlagt ekstremt streng kontrol fra uafhængige, statslige myndigheder. Intet lægemiddel kan blive godkendt, medmindre der foreligger solid, videnskabelig dokumentation for, at det er både sikkert og effektivt. Læger og forskere, der udfører de kliniske forsøg, er også underlagt strenge etiske retningslinjer.
Hvad er forskellen på original medicin og kopimedicin (generika)?
Original medicin er udviklet af det firma, der opfandt det. De har patent på lægemidlet i en årrække for at kunne tjene deres F&U-investering hjem. Når patentet udløber, må andre firmaer producere kopier, såkaldt generisk medicin. Generika indeholder det samme aktive stof og har samme virkning, men er meget billigere, fordi producenterne ikke har haft de samme udviklingsomkostninger.
Rejsen fra et molekyle i et reagensglas til en pille i din hånd er lang, kompliceret og fyldt med usikkerhed. Det er en proces, der kræver tålmodighed, massive investeringer og et tæt samarbejde mellem forskere, læger, hospitaler, myndigheder og ikke mindst de patienter, der deltager i kliniske forsøg. Det er denne indsats, der driver den medicinske udvikling fremad og sikrer, at vi i fremtiden har endnu bedre behandlinger til at bekæmpe sygdomme.
Hvis du vil læse andre artikler, der ligner Fra Laboratorium til Apotek: Medicinens Rejse, kan du besøge kategorien Sundhed.