31/10/2017
Vejen fra en lovende idé i et laboratorium til et færdigt produkt på apotekets hylde eller i en operationsstue er utroligt lang, kompleks og fyldt med udfordringer. For hvert nyt lægemiddel eller medicinsk udstyr, der succesfuldt når patienterne, er der utallige andre, der fejler undervejs. Denne komplekse rejse kræver en ekstremt disciplineret og struktureret tilgang. Det er her, Ny Produktudvikling, eller New Product Development (NPD), kommer ind i billedet. NPD er ikke blot en proces; det er en strategisk ramme, der kombinerer videnskabelig forskning, ingeniørkunst, regulatorisk viden og projektledelse for at sikre, at nye sundhedsløsninger er sikre, effektive og opfylder et reelt klinisk behov.
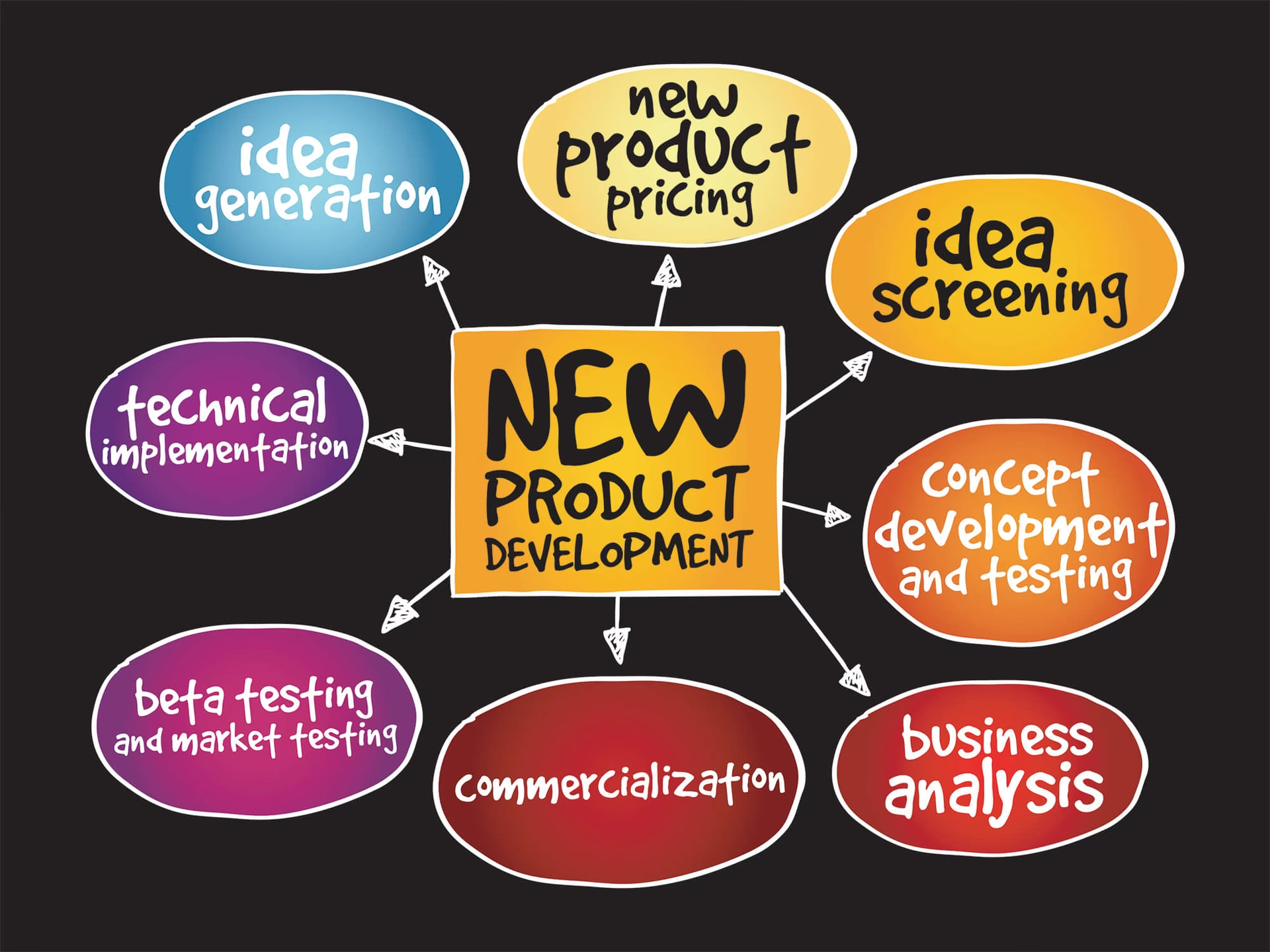
Hvad er Ny Produktudvikling (NPD) i Sundhedssektoren?
Ny Produktudvikling (NPD) er den systematiske proces, der tager et nyt produkt fra det indledende koncept til fuld kommercialisering og lancering på markedet. I sundhedssektoren er denne proces særligt krævende på grund af strenge regulatoriske krav, høje udviklingsomkostninger og den direkte indvirkning på menneskers liv og velvære. Projekterne involverer typisk store, tværfaglige teams bestående af forskere, klinikere, ingeniører, regulatoriske specialister, marketingfolk og mange andre, der skal arbejde tæt sammen.
En succesfuld NPD-proces kræver præcis planlægning, konstant overvågning og effektiv kontrol for at navigere i de mange risici, holde sig inden for budgettet og i sidste ende levere et produkt, der forbedrer patientbehandlingen og stemmer overens med virksomhedens strategiske mål.
Hvorfor er Effektiv NPD-Styring altafgørende?
Statistikkerne taler deres tydelige sprog. Ifølge Harvard Business Review er det kun omkring 40% af alle nye produkter, der rent faktisk når markedet. Inden for medicinal- og medicoindustrien kan dette tal være endnu lavere. Korrekt planlægning, styring og kontrol er derfor ikke bare en fordel – det er en absolut nødvendighed for overlevelse og succes.
- Højere succesrate: Virksomheder med stærk projektledelse i deres NPD-processer er ifølge Project Management Institute 28% mere succesfulde med at overholde deres lanceringsfrister.
- Omkostningseffektivitet: En velstyret proces kan ifølge McKinsey reducere projektomkostningerne med op til 20%. I en branche, hvor udviklingen af et enkelt lægemiddel kan koste milliarder, er dette en markant besparelse.
- Risikominimering: Sundhedssektoren er fyldt med risici – fra kliniske forsøg, der slår fejl, til uventede regulatoriske forhindringer. En struktureret NPD-proces hjælper med at identificere og planlægge for disse risici tidligt.
Ved at fokusere på en velstruktureret planlægning og kontrol kan organisationer dramatisk øge deres chancer for succes og opnå en afgørende konkurrencefordel, samtidig med at de sikrer, at kun de bedste og sikreste produkter når patienterne.
NPD-processen: En Trin-for-Trin Guide fra Laboratorium til Patient
At styre et NPD-projekt inden for sundhed kræver en systematisk tilgang for at sikre overensstemmelse, effektivitet og tilpasningsevne gennem hele projektets livscyklus. Processen kan opdeles i flere afgørende faser:
- Definer Mål og Omfang: Alt starter med et klart defineret mål. Hvilket klinisk problem forsøger vi at løse? Hvem er målgruppen af patienter? Hvad er de ønskede resultater? En klar afgrænsning af projektets omfang fra starten forhindrer "scope creep" senere i processen.
- Gennemfør Markeds- og Klinisk Forskning: Indsaml data om patientbehov, markedstendenser og konkurrerende behandlinger. Denne fase er afgørende for at guide produktspecifikationerne og sikre, at der er et reelt marked for produktet.
- Udvikl en Detaljeret Projektplan: Udarbejd en omfattende plan, der inkluderer tidslinjer, milepæle, budgetter og ressourceallokering. For et lægemiddel vil dette inkludere tidsplaner for prækliniske studier, de forskellige faser af kliniske forsøg og forventet tid til regulatorisk godkendelse.
- Udarbejd en Risikostyringsplan: Identificer potentielle risici tidligt – hvad enten de er videnskabelige, tekniske, regulatoriske eller kommercielle. Udvikl nødplaner for at imødegå disse risici, hvis de skulle opstå. Dette er en central del af risikominimering.
- Design Produktspecifikationer: I tæt samarbejde med ingeniør- og forskerhold defineres de tekniske specifikationer. For et lægemiddel kan det være den kemiske sammensætning og doseringsform; for et medicinsk udstyr kan det være design, materialer og software.
- Prototype og Test (Kliniske Studier): Dette er en af de længste og mest kritiske faser. For udstyr bygges og testes prototyper for at validere funktion og brugervenlighed. For lægemidler udføres omfattende kliniske forsøg i flere faser for at bevise produktets sikkerhed og effektivitet.
- Overvåg Fremskridt: Anvend projektledelsesværktøjer til løbende at spore fremskridt i forhold til tidsplaner og budgetter. Regelmæssige statusmøder og rapportering er nødvendige for at foretage justeringer undervejs.
- Implementer Kvalitetskontrol: Sæt høje kvalitetsstandarder og udfør regelmæssige kontroller for at sikre, at produktet overholder alle regulatoriske og industrielle krav, såsom ISO 13485 for medicinsk udstyr eller Good Manufacturing Practice (GMP) for lægemidler. Effektiv kvalitetskontrol er ikke til forhandling.
- Engager Tværfaglige Teams: Koordiner indsatsen tæt mellem marketing, forskning, produktion og salg for at sikre, at alle arbejder mod det samme mål og at overgangen mellem faserne er så gnidningsfri som mulig.
- Forbered Lancering: Udvikl en "go-to-market"-strategi, der omfatter markedsføring til sundhedspersonale, distributionsplaner og salgstræning. Dette inkluderer også den endelige ansøgning om markedsføringstilladelse fra myndigheder som Det Europæiske Lægemiddelagentur (EMA).
- Gennemfør Post-Lancering Evaluering: Efter lanceringen er arbejdet ikke slut. Overvåg produktets ydeevne på markedet, indsaml feedback fra brugere (læger og patienter) og indsaml real-world data for at identificere områder til forbedring og for at overvåge for uventede bivirkninger (farmakovigilans).
Sammenligning af NPD-faser
For at give et bedre overblik kan processens hovedfaser sammenlignes i en tabel:
| Fase | Primært Fokus | Nøgleaktiviteter |
|---|---|---|
| Idé & Koncept | Identifikation af klinisk behov | Brainstorming, markedsanalyse, feasibility-studier |
| Udvikling & Test | Bevis for sikkerhed & effektivitet | Prækliniske studier, kliniske forsøg, prototyping, regulatorisk dokumentation |
| Lancering | Markedsadgang & accept | Regulatorisk godkendelse, marketingstrategi, produktion, distribution |
| Post-Lancering | Løbende overvågning & optimering | Indsamling af real-world data, patientfeedback, farmakovigilans |
Ofte Stillede Spørgsmål (FAQ)
Hvad er den største udfordring i NPD for medicinalprodukter?
Den absolut største udfordring er den lange, ekstremt dyre og høj-risiko proces forbundet med kliniske forsøg og den efterfølgende regulatoriske godkendelsesproces. Mange lovende lægemiddelkandidater fejler i de sene faser af kliniske forsøg, hvilket resulterer i enorme økonomiske tab.
Hvor lang tid tager en typisk NPD-proces i sundhedssektoren?
Det varierer meget. For et nyt lægemiddel kan processen fra opdagelse til markedsgodkendelse nemt tage 10-15 år. For medicinsk udstyr kan cyklussen være kortere, typisk mellem 3 og 7 år, afhængigt af enhedens kompleksitet og risikoklasse.
Hvilken rolle spiller patienterne i NPD-processen?
Patienternes rolle er blevet stadig vigtigere. Tidligere var de primært deltagere i kliniske forsøg, men i dag inddrages de ofte tidligere i processen for at give input til design af produkter og forsøg. Patientcentreret innovation er en voksende trend, der sikrer, at de endelige produkter reelt imødekommer patienternes behov og præferencer.
Hvad er forskellen på NPD for et medicinsk udstyr og en ny medicin?
Selvom de overordnede principper er de samme, er der store forskelle. Lægemidler gennemgår en streng, faseopdelt klinisk afprøvning for at bevise sikkerhed og effekt. Medicinsk udstyr har forskellige regulatoriske veje baseret på risikoklassificering, og fokus er ofte mere på teknisk ydeevne, brugervenlighed og klinisk evidens frem for farmakologiske effekter.
Konklusion: En Nødvendig Disciplin for Fremtidens Sundhed
Effektiv planlægning, styring og kontrol i Ny Produktudvikling er ikke blot en administrativ øvelse. Det er den afgørende disciplin, der sikrer, at videnskabelige gennembrud kan omsættes til pålidelige, sikre og effektive behandlinger, der når ud til de patienter, som har brug for dem. Ved at anvende en struktureret NPD-tilgang kan virksomheder i sundhedssektoren bedre navigere i det komplekse landskab, minimere risici og i sidste ende opfylde deres vigtigste mission: at forbedre menneskers sundhed og livskvalitet.
Hvis du vil læse andre artikler, der ligner Fra Idé til Patient: Styring af NPD-projekter, kan du besøge kategorien Sundhed.
