05/06/2011
Dravet syndrom er en sjælden og alvorlig form for epilepsi, der begynder i spædbarnsalderen og har dybtgående konsekvenser for patienter og deres familier. Ud over hyppige og ofte langvarige anfald, oplever patienter typisk forsinkelser i udviklingen, kognitive udfordringer og adfærdsproblemer. De nuværende behandlinger er ofte begrænsede i deres effektivitet og fokuserer primært på at kontrollere symptomerne snarere end at adressere den underliggende årsag. Men i horisonten tegner der sig et nyt håb. Forskere og medicinalvirksomheder arbejder intensivt på at udvikle genetiske terapier, der har potentialet til at være sygdomsmodificerende – det vil sige, at de kan ændre selve sygdomsforløbet ved at gå direkte til roden af problemet.
Hvad er Dravet Syndrom og dets Genetiske Årsag?
For at forstå potentialet i de nye behandlinger er det vigtigt at forstå, hvad der forårsager Dravet syndrom. I langt de fleste tilfælde skyldes sygdommen en mutation i et gen kaldet SCN1A. Dette gen er ansvarligt for at producere en del af en natriumkanal i hjernen, som er afgørende for nervecellernes evne til at kommunikere korrekt. Mutationen fører til, at den ene af de to kopier af SCN1A-genet ikke fungerer, som den skal. Dette fænomen kaldes haploinsufficiens.
Resultatet er en utilstrækkelig mængde af funktionelle natriumkanaler, hvilket forstyrrer den elektriske balance i hjernen og fører til den hyperaktivitet, der udløser epileptiske anfald. Den konstante byrde af anfald og den underliggende genetiske fejl påvirker hjernens udvikling negativt, hvilket forklarer de mangeartede symptomer, der er forbundet med syndromet.
Genterapier: En Revolutionerende Tilgang til Behandling
Traditionelle epilepsilægemidler virker ved at dæmpe den generelle elektriske aktivitet i hjernen for at reducere anfald. De reparerer dog ikke den grundlæggende genetiske defekt. Genterapier repræsenterer et paradigmeskifte. I stedet for blot at behandle symptomerne sigter de mod at kompensere for den defekte genkopi. Målet er at genoprette den normale funktion af SCN1A-genet og dermed normalisere hjernens aktivitet på en mere fundamental måde. Forskningen har ført til udviklingen af flere lovende lægemiddelkandidater, hvoraf to især skiller sig ud: zorevunersen og ETX101.
To Lovende Kandidater i Fokus
To forskellige bioteknologiske virksomheder, Stoke Therapeutics og Encoded Therapeutics, er i front med udviklingen af innovative behandlinger for Dravet syndrom. Selvom deres metoder er forskellige, deler de det samme overordnede mål: at øge produktionen fra den raske kopi af SCN1A-genet for at kompensere for den defekte.
Zorevunersen (STK-001): Målrettet RNA-terapi
Stoke Therapeutics' lægemiddelkandidat, zorevunersen (også kendt som STK-001), er en type medicin kaldet et antisense oligonukleotid (ASO). En ASO er et lille, syntetisk stykke genetisk materiale, der er designet til at binde sig til et specifikt RNA-molekyle i cellen. I tilfældet med zorevunersen er målet at øge produktiviteten af den sunde kopi af SCN1A-genet. Det virker ved at forhindre, at RNA-molekylet fra det sunde gen nedbrydes for tidligt, hvilket resulterer i produktionen af mere funktionelt natriumkanalprotein.
De tidlige kliniske data har været lovende og har vist potentiale for ikke kun at reducere anfaldsfrekvensen, men også for at have en positiv indvirkning på kognitive domæner hos patienterne. Zorevunersen forventes at gå ind i de afgørende fase 3-studier i 2025, hvilket er et stort skridt på vejen mod en eventuel godkendelse.
ETX101: En Engangs-Genregulerende Terapi
Encoded Therapeutics har udviklet ETX101, en potentiel engangs-genregulerende terapi. Denne tilgang er mere kompleks og involverer brugen af en modificeret virus som transportmiddel. ETX101 består af et specialdesignet genetisk materiale, en såkaldt "konstrueret transkriptionsfaktor", som er pakket ind i en adeno-associeret viruskapsel (AAV9). AAV9 er en velkendt og sikkerheds-testet virusvektor, der bruges i andre godkendte genterapier.
Når ETX101 administreres, leverer virusvektoren den genetiske last til de relevante hjerneceller. Her fungerer transkriptionsfaktoren som en "tænd/sluk-knap", der specifikt øger udtrykket (aktiviteten) af SCN1A-genet. Terapien er designet til at være målrettet mod de nerveceller i hjernen, der er mest påvirket af Dravet syndrom. Prækliniske studier i dyremodeller har vist, at ETX101 kunne reducere anfald og forbedre overlevelsen markant. Encoded Therapeutics har for nylig fået grønt lys fra myndighederne i USA og Australien til at starte de første kliniske forsøg med mennesker. Disse studier, navngivet ENDEAVOR (i USA) og WAYFINDER (i Australien), forventes at begynde i første halvdel af 2024 og vil evaluere sikkerheden og den foreløbige effekt af ETX101 hos små børn med Dravet syndrom.
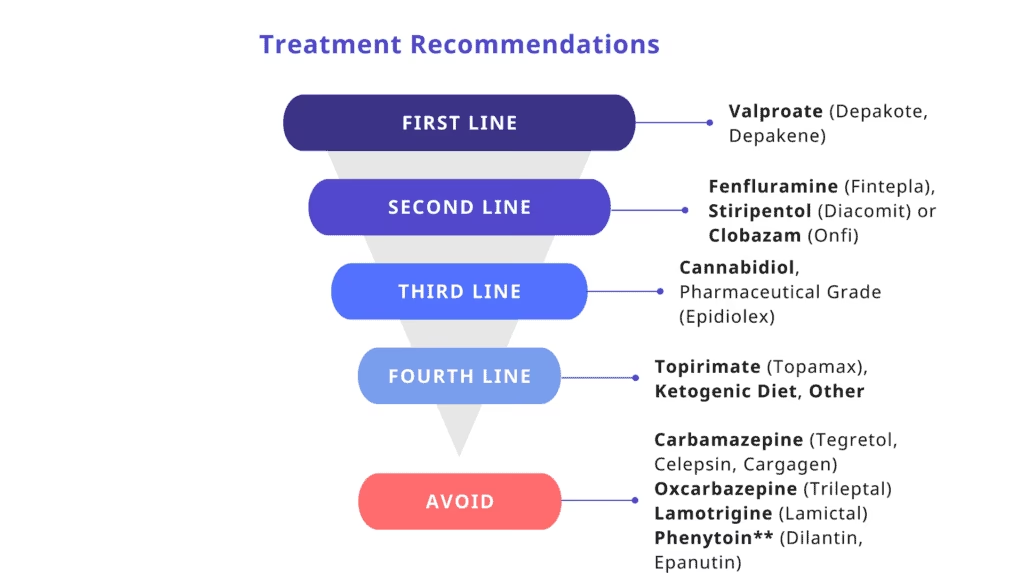
Sammenligning af de To Terapier
Selvom begge terapier har det samme mål, er deres teknologi og potentielle anvendelse forskellig. Nedenstående tabel giver et overblik over de vigtigste forskelle.
| Egenskab | Zorevunersen (STK-001) | ETX101 |
|---|---|---|
| Virksomhed | Stoke Therapeutics | Encoded Therapeutics |
| Terapi Type | Antisense Oligonukleotid (ASO) | AAV-baseret genregulerende terapi |
| Virkningsmekanisme | Øger mængden af protein produceret fra det sunde gens RNA. | Øger aktiviteten (transkriptionen) af selve det sunde gen. |
| Administration | Kræver sandsynligvis gentagne doser. | Designet som en potentiel engangsbehandling. |
| Udviklingsstatus | Forventes at starte fase 3-studier i 2025. | Starter fase 1/2-studier i 2024. |
Vejen Frem: Håb og Realisme
Annonceringen af nye kliniske forsøg er et monumentalt skridt fremad for Dravet-fællesskabet. Det er et resultat af årtiers grundforskning, utrættelig indsats fra forskere og en stærk involvering fra patientfamilier, der har skubbet på for udvikling og finansiering. Initiativer som Dravet ENGAGE, der har indsamlet viden om familiers behov og perspektiver, har været afgørende for at forme udviklingen af disse terapier.
Det er dog vigtigt at bevare en sund realisme. Disse behandlinger er stadig på et eksperimentelt stadie. Kliniske forsøg er designet til at besvare kritiske spørgsmål om sikkerhed og effektivitet hos mennesker. Processen er lang og grundig, og der er ingen garantier for succes. Ikke desto mindre repræsenterer disse fremskridt et konkret og velbegrundet håb. For første gang er der en reel mulighed for behandlinger, der ikke blot dæmper symptomerne, men som potentielt kan gribe ind i selve sygdommens kerne og give en bedre fremtid for dem, der lever med Dravet syndrom.
Ofte Stillede Spørgsmål (FAQ)
Hvad er haploinsufficiens?
Haploinsufficiens er en genetisk tilstand, hvor en person kun har én funktionel kopi af et gen, mens den anden kopi er muteret eller mangler. Når den ene raske kopi ikke er i stand til at producere nok af det nødvendige protein til, at kroppen kan fungere normalt, opstår der en sygdom, som det er tilfældet med SCN1A-genet i Dravet syndrom.
Er disse nye behandlinger en kur mod Dravet syndrom?
Det er for tidligt at tale om en "kur". Målet med disse sygdomsmodificerende terapier er at korrigere den underliggende genetiske fejl i en sådan grad, at symptomerne reduceres drastisk, og livskvaliteten forbedres markant. Håbet er, at de kan stoppe eller bremse sygdomsprogressionen, men de langsigtede effekter vil først blive kendt efter mange års opfølgning.
Hvornår vil disse behandlinger være tilgængelige for alle patienter?
Vejen fra de tidlige kliniske forsøg til en bredt tilgængelig, godkendt behandling er lang. Den involverer flere faser af kliniske studier (fase 1, 2 og 3) for at bevise sikkerhed og effekt. Denne proces tager typisk adskillige år. Hvis studierne er succesfulde, skal lægemidlerne efterfølgende godkendes af sundhedsmyndigheder som det Europæiske Lægemiddelagentur (EMA), før de kan markedsføres.
Hvad er forskellen på en ASO-terapi og en AAV-genterapi?
En ASO-terapi, som zorevunersen, er en kemisk baseret behandling, der påvirker RNA-molekylerne i cellen. Den har en begrænset varighed og kræver sandsynligvis gentagne doser. En AAV-genterapi, som ETX101, bruger en virus til at levere et stykke DNA til cellerne, som derefter kan udøve sin funktion i lang tid, potentielt permanent. Den er derfor designet som en engangsbehandling.
Hvis du vil læse andre artikler, der ligner Genterapier: Et Nyt Håb for Dravet Syndrom, kan du besøge kategorien Sundhed.
