07/12/2013
- Introduktion til en usynlig men afgørende kamp
- Hvad er Minimum Inhibitorisk Koncentration (MIC)?
- Hvordan bestemmes MIC-værdier i laboratoriet?
- Fortolkning af MIC: Fra laboratorietal til klinisk beslutning
- MIC's afgørende rolle i moderne medicin
- Udfordringer og begrænsninger
- Ofte Stillede Spørgsmål (FAQ)
- Konklusion
Introduktion til en usynlig men afgørende kamp
I en verden, hvor superbakterier og antibiotikaresistens udgør en stadigt voksende trussel mod global sundhed, er præcision i behandlingen af infektioner vigtigere end nogensinde før. Når en læge skal vælge det rette våben mod en bakteriel infektion, er det ikke nok blot at vide, hvilke antibiotika der generelt virker. Lægen har brug for specifik, kvantitativ information om, hvor effektivt et givent lægemiddel er mod netop den bakteriestamme, der har inficeret patienten. Her kommer et af mikrobiologiens mest centrale begreber i spil: Minimum Inhibitorisk Koncentration, eller MIC. Denne værdi er ikke bare et tal fra et laboratorium; det er en afgørende brik i puslespillet om at sikre en vellykket behandling, minimere bivirkninger og bremse udviklingen af yderligere resistens. I denne artikel dykker vi ned i, hvad MIC er, hvordan det måles, og hvorfor det har en fundamental betydning for din sundhed.

Hvad er Minimum Inhibitorisk Koncentration (MIC)?
Minimum Inhibitorisk Koncentration (MIC) er den laveste koncentration af et antibiotikum, som er nødvendig for synligt at hæmme væksten af en bestemt bakterie under kontrollerede laboratorieforhold. Det er med andre ord et mål for et antibiotikums styrke mod en specifik mikroorganisme. Resultatet udtrykkes typisk i mikrogram pr. milliliter (µg/mL) eller milligram pr. liter (mg/L). Det er vigtigt at understrege, at dette er en in vitro-måling, hvilket betyder, at den udføres i et reagensglas eller på en petriskål og ikke direkte i patienten. Selvom det ikke er et perfekt spejl af, hvad der sker i den menneskelige krop, giver det et utroligt værdifuldt fingerpeg om, hvilke lægemidler der har størst sandsynlighed for at virke.
En almindelig misforståelse er at sammenligne MIC-værdier direkte mellem forskellige typer antibiotika. En lav MIC-værdi for penicillin kan ikke sammenlignes med en MIC-værdi for ciprofloxacin for at afgøre, hvilket stof der er "bedst". Hvert antibiotikum har sin egen unikke virkningsmekanisme og sine egne specifikke koncentrationsniveauer, der er fastsat som effektive. MIC-værdien skal altid fortolkes i forhold til etablerede standarder for netop det lægemiddel.
Hvordan bestemmes MIC-værdier i laboratoriet?
For at sikre pålidelige og reproducerbare resultater følger mikrobiologiske laboratorier standardiserede procedurer. Der er primært to anerkendte metoder til at bestemme MIC:
1. Fortyndingsmetoder (Dilution Methods)
Dette betragtes som guldstandarden. Den mest almindelige fortyndingsmetode er bouillon-mikrofortynding. Processen foregår således:
- En række brønde i en mikroplade fyldes med et vækstmedie (bouillon).
- Antibiotikummet tilsættes i faldende koncentrationer til brøndene, så hver brønd har halvdelen af koncentrationen af den foregående. En brønd efterlades uden antibiotika som vækstkontrol.
- En standardiseret mængde af patientens bakterier (et inokulum) tilsættes til hver brønd.
- Pladen inkuberes ved en bestemt temperatur (typisk 35±1 °C) i 18-24 timer.
- Efter inkubation aflæses resultaterne. MIC-værdien er koncentrationen i den første klare brønd, hvor der ikke er nogen synlig bakterievækst.
En anden variant er agar-fortynding, hvor antibiotikummet blandes direkte i agar-mediet i petriskåle i forskellige koncentrationer. Princippet er det samme: at finde den laveste koncentration, der forhindrer vækst.
2. Gradientmetoden (E-test)
Denne metode er teknisk simplere og hurtigere. Den involverer en plastikstrimmel, der er imprægneret med en gradueret koncentration af et antibiotikum. Strimlen placeres på en agarplade, hvor patientens bakterier er blevet spredt ud. Under inkubationen diffunderer antibiotikummet ud i agaren. Dette skaber en elliptisk hæmningszone omkring strimlen. MIC-værdien aflæses der, hvor kanten af hæmningszonen krydser strimlen. Selvom denne metode er praktisk, kan den være mindre pålidelig for visse antibiotika-bakterie-kombinationer, såsom colistin og fosfomycin, hvor fortyndingsmetoden foretrækkes.
For alle metoder gælder det, at der udføres streng kvalitetskontrol med referencestammer – bakterier med kendte MIC-værdier – for at sikre, at testen er udført korrekt.
Fortolkning af MIC: Fra laboratorietal til klinisk beslutning
En rå MIC-værdi på f.eks. 2 mg/L er i sig selv meningsløs for en kliniker. For at oversætte dette tal til en brugbar klinisk anbefaling, sammenlignes det med såkaldte kliniske brydningspunkter (clinical breakpoints). Disse brydningspunkter er fastsat af internationale komitéer som EUCAST (European Committee on Antimicrobial Susceptibility Testing) og CLSI (Clinical and Laboratory Standards Institute) i USA. De er baseret på årtiers data om mikrobiologi, farmakologi og kliniske resultater.
Baseret på sammenligningen mellem den målte MIC-værdi og brydningspunktet, kategoriseres bakterien som en af følgende:
| Kategori | Betydning ifølge EUCAST | Klinisk handling |
|---|---|---|
| S – Følsom, standarddosering | Der er høj sandsynlighed for behandlingssucces ved brug af en standarddosis af antibiotikummet. | Lægen ordinerer den normale, anbefalede dosis. |
| I – Følsom, øget eksponering | Der er høj sandsynlighed for succes, fordi eksponeringen for lægemidlet øges ved at justere doseringen eller ved koncentrationen på infektionsstedet. | Lægen kan ordinere en højere dosis, kortere interval mellem doser eller skifte til intravenøs infusion for at opnå en højere koncentration af lægemidlet. |
| R – Resistent | Der er høj sandsynlighed for behandlingssvigt, selv ved øget eksponering. | Lægen skal vælge et andet antibiotikum, som bakterien er følsom over for. |
Denne S/I/R-klassificering er det, lægen bruger til at træffe en informeret beslutning om den videre behandling.

MIC's afgørende rolle i moderne medicin
Kendskabet til MIC-værdien er især kritisk i behandlingen af alvorligt syge patienter, patienter med svækket immunforsvar og infektioner forårsaget af multiresistente bakterier. Her er en kvalitativ S/R-vurdering ofte ikke nok. MIC-værdien giver et mere nuanceret billede og er essentiel for at optimere behandlingen gennem farmakokinetik og farmakodynamik (PK/PD).
Optimering med PK/PD
PK/PD er studiet af, hvordan en patients krop påvirker et lægemiddel (PK - farmakokinetik) og hvordan lægemidlet påvirker bakterien (PD - farmakodynamik). Ved at kombinere patientens farmakokinetiske data med bakteriens MIC-værdi kan man forudsige, om en given dosering vil være effektiv. Målet er at opnå en af tre PK/PD-indekser:
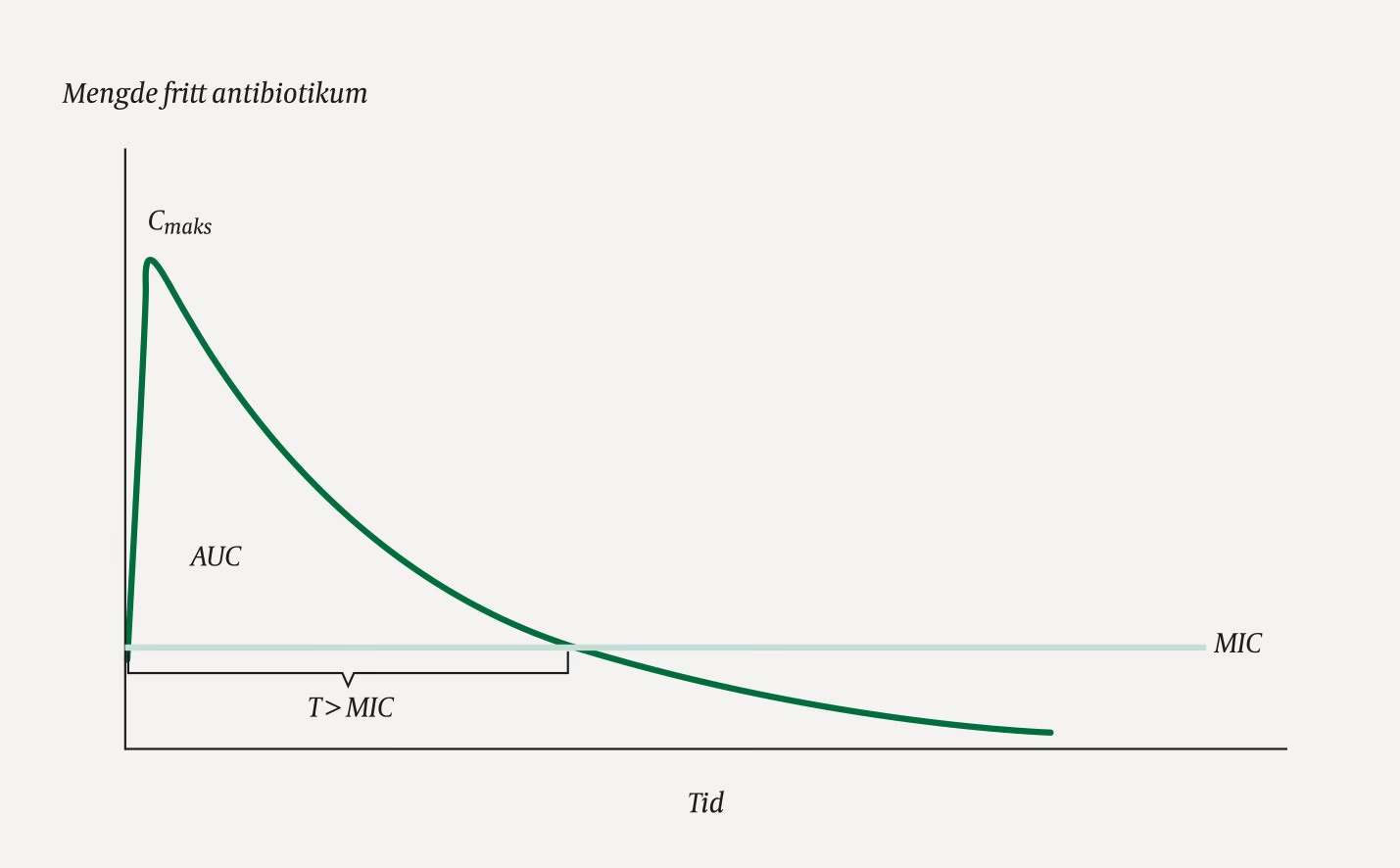
- T > MIC: For tidsafhængige antibiotika (f.eks. penicilliner og cefalosporiner) er målet, at koncentrationen af det frie lægemiddel i blodet er over MIC-værdien i en bestemt procentdel af tiden mellem doserne. En lavere MIC gør det lettere at opnå dette mål.
- Cmax/MIC: For koncentrationsafhængige antibiotika (f.eks. aminoglykosider) er målet at opnå en maksimal koncentration (Cmax), der er mange gange højere (typisk 8-10 gange) end MIC-værdien.
- AUC/MIC: For antibiotika, hvis effekt afhænger af den samlede eksponering (f.eks. vancomycin og fluorquinoloner), er målet, at det samlede "areal under kurven" (AUC) for lægemiddelkoncentrationen over 24 timer, divideret med MIC, overstiger en bestemt tærskel.
Ved at kende den præcise MIC-værdi kan læger skræddersy doseringen for den enkelte patient. For en bakterie med en MIC tæt på brydningspunktet (men stadig i 'I'-kategorien), kan det være nødvendigt at give høje doser eller bruge forlænget infusion for at sikre klinisk succes. Uden MIC-værdien ville man famle i blinde.
Udfordringer og begrænsninger
Selvom MIC er et kraftfuldt værktøj, er det ikke uden begrænsninger. Fænomener som heteroresistens (hvor en lille undergruppe af bakterier er resistente), tolerance (bakterier overlever, men vokser ikke) og persistens (sovende celler) kan føre til behandlingssvigt, selvom MIC-testen indikerer følsomhed. Desuden kan dannelsen af biofilm, en beskyttende slim, som bakterier danner på overflader (f.eks. i katetre eller implantater), gøre dem langt mere modstandsdygtige over for antibiotika, end MIC-testen forudsiger.
Ofte Stillede Spørgsmål (FAQ)
Er et antibiotikum med en lav MIC-værdi altid bedre end et med en høj MIC-værdi?
Nej, absolut ikke. MIC-værdier kan ikke sammenlignes direkte mellem forskellige klasser af antibiotika. En MIC på 0.06 mg/L for ét lægemiddel kan indikere resistens, mens en MIC på 8 mg/L for et andet kan indikere følsomhed. Tolkningen afhænger altid af de videnskabeligt fastsatte kliniske brydningspunkter for det specifikke lægemiddel mod den specifikke bakterie.
Hvorfor får jeg ikke altid en MIC-værdi for min infektion?
For mange ukomplicerede infektioner, som f.eks. en simpel halsbetændelse eller blærebetændelse hos en ellers rask person, er en kvalitativ test (følsom eller resistent) tilstrækkelig til at guide behandlingen. MIC-bestemmelse er mere ressourcekrævende og bruges typisk til alvorligt syge patienter, ved mistanke om behandlingssvigt, eller ved infektioner med kendte problematiske eller multiresistente bakterier.
Hvad betyder MIC90, som man nogle gange ser i videnskabelige artikler?
MIC90 er et epidemiologisk mål, der bruges til at overvåge resistensmønstre i en population af bakterier. Det er den MIC-værdi, der er nødvendig for at hæmme væksten af 90% af de testede bakteriestammer af en bestemt art. Hospitaler bruger denne data til at skabe lokale retningslinjer for, hvilke antibiotika der mest sandsynligt vil virke, før man har et specifikt svar for den enkelte patient.
Konklusion
Minimum Inhibitorisk Koncentration er meget mere end et teknisk tal fra et laboratorium. Det er et fundamentalt værktøj i kampen mod bakterielle infektioner og antibiotikaresistens. Det giver læger den præcision, der er nødvendig for at vælge det rigtige lægemiddel i den rigtige dosis, hvilket øger chancerne for en vellykket behandling, reducerer risikoen for bivirkninger og er med til at bevare effektiviteten af de dyrebare antibiotika, vi har til rådighed. Næste gang du eller en pårørende modtager antibiotikabehandling for en alvorlig infektion, kan du være sikker på, at en MIC-værdi sandsynligvis har spillet en afgørende, men usynlig, rolle i at sikre den bedst mulige pleje.
Hvis du vil læse andre artikler, der ligner MIC-værdier: Nøglen til effektiv antibiotikabehandling, kan du besøge kategorien Sundhed.