28/08/2000
Rejsen for et nyt lægemiddel, fra den første idé i et laboratorium til det øjeblik, det kan købes på apoteket, er en utrolig lang, kompleks og omkostningstung proces. Denne farmaceutiske udviklingstidslinje er en omhyggeligt struktureret rejse, der typisk strækker sig over 10 til 15 år og involverer adskillige stadier af forskning, testning og streng regulatorisk kontrol. At forstå denne proces er afgørende for at værdsætte det enorme arbejde, der ligger bag hver pille, vaccine eller behandling, vi har adgang til. Formålet er ikke kun at skabe effektive behandlinger, men frem for alt at garantere patienternes sikkerhed.
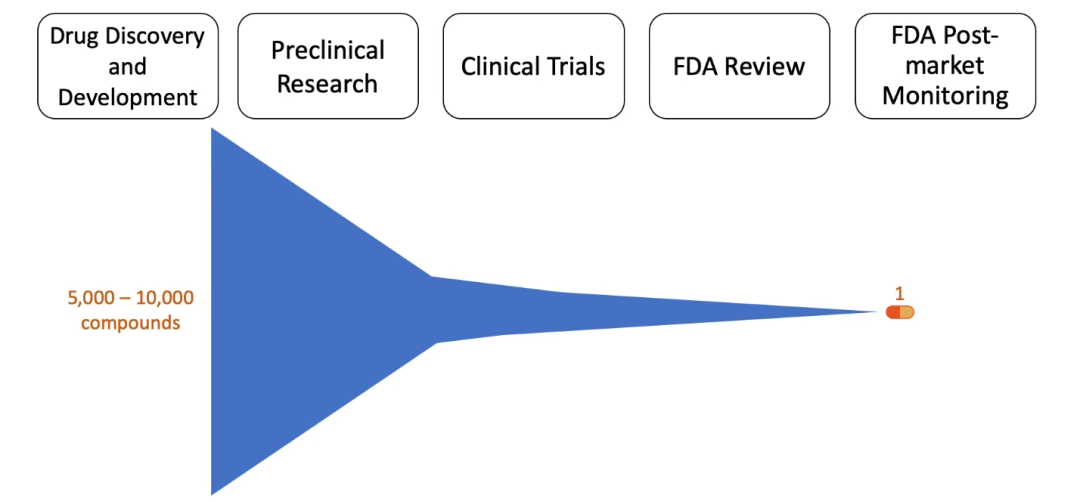
Hvert trin i processen er designet til at besvare specifikke spørgsmål: Er det potentielle lægemiddel sikkert? Virker det mod den pågældende sygdom? Hvad er den korrekte dosis? Hvilke bivirkninger har det? Kun de kandidater, der succesfuldt navigerer gennem alle disse faser, opnår den endelige godkendelse. Det er en proces med høj risiko, hvor kun omkring 1 ud af 5.000 undersøgte stoffer ender med at blive et godkendt lægemiddel.
De Fire Hovedfaser i Lægemiddeludvikling
Hele processen kan overordnet inddeles i fire primære faser: Opdagelse og udvikling, præklinisk forskning, kliniske forsøg og endelig myndighedsgodkendelse og markedsovervågning. Hver fase bygger på den foregående og øger gradvist mængden af viden om lægemiddelkandidaten.
Fase 1: Opdagelse og Udvikling
Alt begynder i laboratoriet. I opdagelsesfasen identificerer forskere et 'mål' – typisk et gen eller et protein, der spiller en central rolle i en sygdom. Målet er at finde et molekyle eller et biologisk stof, der kan interagere med dette mål for at modvirke sygdommens effekt. Dette indebærer ofte screening af tusindvis af kemiske forbindelser ved hjælp af avancerede teknologier som high-throughput screening og computermodellering (in silico-testning) for at finde de mest lovende kandidater. Når en håndfuld lovende stoffer er identificeret, optimerer medicinalkemikere deres struktur for at forbedre deres effektivitet og reducere potentielle bivirkninger. Denne indledende fase kan alene tage flere år.
Fase 2: Præklinisk Forskning
Før et potentielt lægemiddel kan testes i mennesker, skal det gennemgå en grundig præklinisk forskningsfase. Formålet er at indsamle essentielle data om sikkerhed og toksicitet. Denne fase involverer to typer af studier:
- In vitro-studier: Testning udføres i et kontrolleret laboratoriemiljø, f.eks. på celler i en petriskål.
- In vivo-studier: Testning udføres i levende organismer, typisk dyr som mus eller rotter, for at se, hvordan stoffet opfører sig i en kompleks biologisk organisme.
I denne fase undersøger forskerne lægemidlets farmakokinetik (hvordan kroppen absorberer, fordeler, metaboliserer og udskiller stoffet) og farmakodynamik (hvordan stoffet påvirker kroppen). Det vigtigste mål er at identificere eventuelle skadelige effekter og fastslå en foreløbig sikker dosis, før man går videre til mennesker. Samlet set kan opdagelses- og den prækliniske fase vare mellem fire og syv år. Hvis resultaterne er positive, samles al data i en ansøgning til de regulerende myndigheder (som FDA i USA eller EMA i EU) for at få tilladelse til at starte kliniske forsøg.
Fase 3: Kliniske Forsøg med Mennesker
Dette er den længste og mest ressourcekrævende del af udviklingen. Kliniske forsøg foregår i flere underfaser, der hver især har et specifikt formål.

Klinisk Fase I: Fokus på Sikkerhed
Den første test i mennesker. En lille gruppe på 20-100 raske frivillige deltager. Hovedformålet er at vurdere lægemidlets sikkerhedsprofil, fastlægge et sikkert dosisinterval og identificere almindelige bivirkninger. Forskerne overvåger nøje, hvordan stoffet opfører sig i menneskekroppen. Denne fase varer typisk op til et år.
Klinisk Fase II: Test af Effektivitet
Hvis fase I viser, at lægemidlet er sikkert, fortsætter man til fase II. Her testes stoffet på en større gruppe patienter (100-300), der rent faktisk har den sygdom, lægemidlet er tiltænkt at behandle. Hovedformålet er at vurdere lægemidlets effektivitet og fortsat overvåge sikkerheden. Forskerne forsøger at finde den optimale dosis, der giver den bedste effekt med færrest mulige bivirkninger. Denne fase kan tage op til to år.
Klinisk Fase III: Bekræftelse i Stor Skala
Dette er den afgørende og mest omfattende fase. Tusindvis af patienter (ofte 1.000-3.000 eller flere) deltager i disse studier, som ofte er multinationale. Formålet er endeligt at bekræfte lægemidlets effektivitet, overvåge bivirkninger over længere tid og sammenligne det med eksisterende standardbehandlinger eller placebo. Den store mængde data, der indsamles her, er afgørende for, om myndighederne vil godkende lægemidlet. De bivirkninger, der noteres her, er dem, der typisk vil fremgå af indlægssedlen. En fase III-undersøgelse varer i gennemsnit et til fire år.
Oversigt over de Kliniske Faser
| Fase | Formål | Deltagere | Typisk Varighed |
|---|---|---|---|
| Fase I | Vurdere sikkerhed og dosering | 20-100 raske frivillige | Op til 1 år |
| Fase II | Teste effektivitet og bivirkninger | 100-300 patienter | Op til 2 år |
| Fase III | Bekræfte effektivitet, overvåge langsigtede bivirkninger | 1.000-3.000+ patienter | 1-4 år |
Fase 4: Myndighedsgodkendelse og Lancering
Efter vellykkede fase III-studier samler medicinalfirmaet al data fra hele udviklingsprocessen i en omfattende ansøgning til de regulerende myndigheder. Denne ansøgning kan bestå af hundredtusindvis af sider med dokumentation. Et panel af eksperter hos myndighederne, herunder læger, kemikere og statistikere, gennemgår alle data for at vurdere lægemidlets fordele i forhold til dets risici. Denne gennemgang tager typisk 6-12 måneder. Hvis lægemidlet godkendes, kan det markedsføres og sælges. Herefter følger ofte prisforhandlinger med nationale sundhedssystemer eller forsikringsselskaber.
Efter Godkendelse: Overvågning på Markedet (Fase IV)
Arbejdet slutter ikke, når lægemidlet er på markedet. Fase IV-studier, også kendt som post-marketing surveillance, er afgørende. Her overvåges lægemidlets sikkerhed og effektivitet i den brede befolkning over lang tid. Disse studier kan afsløre sjældne bivirkninger eller interaktioner med andre lægemidler, som ikke blev opdaget i de mere kontrollerede kliniske forsøg. Dette sikrer en løbende overvågning og er en vigtig del af lægemiddelsikkerheden (farmakovigilans).

Udfordringer i Lægemiddeludvikling
Processen er fyldt med udfordringer, der kan forsinke eller stoppe udviklingen af et potentielt lægemiddel.
- Finansielle Byrder: Udviklingen af et enkelt lægemiddel kan koste over en milliard dollars. De enorme omkostninger og den høje fejlrate er en væsentlig faktor for de høje medicinpriser.
- Etiske Overvejelser: Især i kliniske forsøg er etik altafgørende. Patienternes sikkerhed og informerede samtykke skal altid have højeste prioritet.
- Regulatoriske Hürder: At navigere i det komplekse landskab af regler og krav fra myndigheder verden over kræver enorm ekspertise og ressourcer.
- Teknologiske Begrænsninger: Selvom teknologien konstant udvikler sig, er der stadig biologiske og teknologiske begrænsninger, der kan gøre det svært at udvikle effektive behandlinger for komplekse sygdomme.
Ofte Stillede Spørgsmål (FAQ)
Hvor lang tid tager det at udvikle et nyt lægemiddel?
I gennemsnit tager hele processen fra opdagelse til markedsgodkendelse mellem 10 og 15 år. For nogle avancerede terapier, som f.eks. genterapi, kan det tage endnu længere tid.
Hvorfor er ny medicin så dyr?
De høje priser afspejler de enorme omkostninger til forskning og udvikling, de mange års arbejde, og den meget høje risiko for, at et lægemiddel fejler undervejs. For hvert lægemiddel, der bliver godkendt, er der tusindvis, der ikke klarede den.
Hvad er forskellen på præklinisk og klinisk forskning?
Præklinisk forskning foregår i laboratorier og på dyr for at vurdere grundlæggende sikkerhed og potentiale. Klinisk forskning (eller kliniske forsøg) foregår på mennesker for at teste sikkerhed og effektivitet i den virkelige verden.
Er et lægemiddel 100% sikkert, når det er godkendt?
Intet lægemiddel er 100% uden risiko. Godkendelsen betyder, at myndighederne har vurderet, at fordelene ved lægemidlet opvejer de kendte risici for en bestemt patientgruppe. Fase IV-overvågning hjælper med at fange sjældne eller langsigtede bivirkninger, efter at lægemidlet er kommet på markedet.
Hvis du vil læse andre artikler, der ligner Tidslinjen for et nyt lægemiddel: Fra idé til apotek, kan du besøge kategorien Medicin.
