17/02/2008
I en verden, hvor moderne medicin har givet os kraftfulde våben mod sygdomme, lurer en voksende trussel i skyggerne: antibiotikaresistens. En af de mest bekymrende manifestationer af denne krise er fremkomsten af bakterier, der producerer Klebsiella pneumoniae carbapenemase (KPC). Disse mikroorganismer, ofte kaldet "superbakterier", har udviklet en formidabel forsvarsmekanisme, der gør dem immune over for nogle af vores mest potente antibiotika. Infektioner forårsaget af KPC-producerende bakterier er forbundet med betydelig sygelighed og dødelighed og udgør en alvorlig udfordring for læger og sundhedssystemer verden over. Denne artikel dykker ned i, hvad KPC er, hvorfor det er så farligt, og hvilke udfordringer vi står over for i kampen mod denne usynlige fjende.
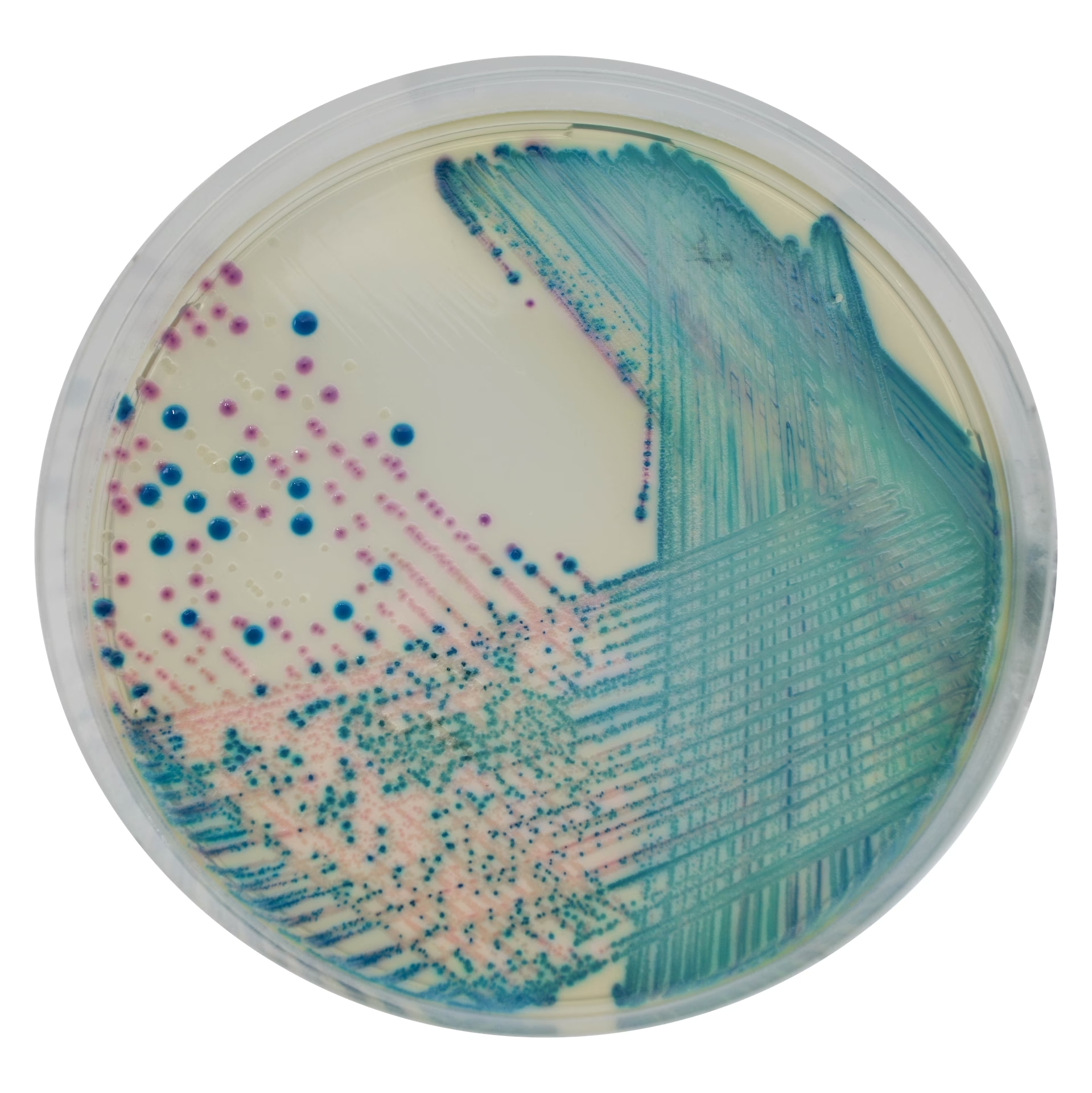
Hvad er Klebsiella pneumoniae carbapenemase (KPC)?
Klebsiella pneumoniae carbapenemase (KPC) er et enzym, der produceres af visse typer gramnegative bakterier. Dette enzym har en særlig og farlig evne: det kan nedbryde og inaktivere en klasse af meget kraftige antibiotika kendt som carbapenemer. Carbapenemer betragtes ofte som en sidste udvej til behandling af alvorlige infektioner forårsaget af multiresistente bakterier. Når en bakterie kan producere KPC, bliver den resistent over for disse kritiske lægemidler, hvilket efterlader læger med meget få, og ofte mindre effektive, behandlingsmuligheder.
Selvom navnet stammer fra bakterien Klebsiella pneumoniae, hvor enzymet først blev identificeret i stor stil, er KPC-resistensmekanismen ikke længere begrænset til denne ene art. Den genetiske kode for KPC-enzymet (kaldet blaKPC-genet) er placeret på et mobilt genetisk element kendt som en transposon (specifikt Tn4401). Denne transposon kan let overføres mellem forskellige bakteriearter via plasmider, som er små, cirkulære stykker DNA. Dette betyder, at resistensen kan sprede sig hurtigt fra Klebsiella pneumoniae til andre gramnegative bakterier som Escherichia coli (E. coli), Enterobacter-arter og endda Pseudomonas aeruginosa. Derfor er udtrykket Carbapenem-Resistente Enterobacteriaceae (CRE) blevet mere almindeligt for at beskrive denne bredere gruppe af resistente bakterier.
Epidemiologi: En global spredning
Historien om KPC er en fortælling om hurtig og global spredning. Den første KPC-producerende K. pneumoniae-stamme blev rapporteret i North Carolina, USA, i 2001. Før dette var carbapenemresistens i denne bakterie yderst sjælden i USA. Efter de første sporadiske udbrud i New York City blev KPC-producerende bakterier endemiske på mange hospitaler i New York og New Jersey-området.
I det efterfølgende årti spredte disse bakterier sig over hele USA og videre ud i verden. I 2005 blev det første tilfælde uden for USA rapporteret i Frankrig hos en patient, der for nylig havde været indlagt i New York. Kort efter fulgte store udbrud i Israel og Grækenland, hvor KPC nu er endemisk. Siden da er KPC-producerende bakterier blevet rapporteret i lande som Brasilien, Kina, Colombia, Storbritannien, Indien, Italien og de nordiske lande. Rejser, immigration og medicinsk behandling i endemiske områder har spillet en væsentlig rolle i den globale spredning. Molekylær epidemiologi har vist, at en enkelt dominerende stamme, kendt som multilocus sekvenstype 258 (ST258), har været ansvarlig for en stor del af den globale spredning af blaKPC-genet.
Hvem er i risikogruppen?
Ikke alle er lige udsatte for at få en infektion med en KPC-producerende bakterie. Infektionerne rammer oftest personer, der allerede er sårbare og syge. Identifikation af risikofaktorer er afgørende for at kunne målrette forebyggende indsatser. De vigtigste risikofaktorer omfatter:
- Langvarige hospitalsophold: Jo længere en patient er indlagt, især på en intensivafdeling (ICU), desto større er risikoen for eksponering.
- Alvorlig sygdom: Kritisk syge patienter med svækket immunforsvar er mere modtagelige.
- Indlagte medicinske anordninger: Brug af centrale venekatetre, urinkatetre eller respiratorer skaber indgangsporte for bakterier.
- Tidligere antibiotikabehandling: Især nylig brug af bredspektrede antibiotika som carbapenemer, fluorquinoloner og cephalosporiner kan forstyrre den normale tarmflora og give plads til resistente bakterier.
- Høj alder: Ældre patienter har ofte flere underliggende sygdomme og et svagere immunforsvar.
- Organtransplantation eller stamcelletransplantation: Disse patienter modtager immunsupprimerende medicin, hvilket gør dem ekstremt sårbare.
- Nylige kirurgiske indgreb: Især abdominalkirurgi øger risikoen.
- Ophold på sundhedsfaciliteter i endemiske områder: Rejser til lande med høj forekomst af KPC er en kendt risikofaktor.
Det er vigtigt at bemærke, at en person kan være koloniseret med KPC-bakterier uden at være syg. Kolonisering betyder, at bakterierne findes i eller på kroppen (oftest i tarmen) uden at forårsage en aktiv infektion. Disse koloniserede patienter udgør dog et reservoir for smittespredning til andre sårbare patienter på hospitalet.

Diagnose og laboratorieudfordringer
En af de største udfordringer ved KPC-producerende bakterier er, at de kan være svære at opdage med standard laboratoriemetoder. Automatiserede systemer, som mange hospitaler bruger til at teste for antibiotikafølsomhed, kan fejlagtigt rapportere disse bakterier som værende følsomme over for carbapenemer som imipenem eller meropenem. Dette kan føre til en kritisk forsinkelse i iværksættelsen af den korrekte behandling, hvilket har alvorlige konsekvenser for patientens overlevelse.
Forskere har opdaget, at resistens over for antibiotikummet ertapenem er en mere følsom indikator for tilstedeværelsen af KPC. Derfor anbefales det, at laboratorier, der finder nedsat følsomhed over for carbapenemer, udfører bekræftende tests. Den mest almindelige bekræftende test er den modificerede Hodge-test. Nyere og mere specifikke metoder inkluderer kromogene medier som CHROMagar KPC og molekylære metoder som PCR, der direkte kan påvise blaKPC-genet. Disse molekylære tests er dog dyre og ofte kun tilgængelige på specialiserede referencelaboratorier.
Behandlingsmuligheder: En kamp mod få alternativer
Behandling af infektioner forårsaget af KPC-producerende bakterier er yderst kompliceret på grund af den udbredte resistens. Læger er ofte tvunget til at bruge ældre, mindre anvendte antibiotika, som kan have betydelige bivirkninger. Den optimale behandling er stadig under debat, men ofte anvendes kombinationsbehandling, hvor flere lægemidler gives samtidigt for at opnå en synergistisk effekt og reducere risikoen for yderligere resistensudvikling.
Ældre antibiotika som redningsplanke
- Polymyxiner (Colistin): Disse er ofte de eneste midler, der viser aktivitet in vitro. Colistin er dog berygtet for sin toksicitet, især nyre- og nerveskader (nefrotoksicitet og neurotoksicitet). Doseringen er kompliceret, og resistens over for colistin er desværre også begyndt at dukke op.
- Tigecyclin: Dette nyere tetracyklin-derivat har god aktivitet mod mange KPC-stammer. Dets primære ulempe er, at det opnår lave koncentrationer i blodet og urinen, hvilket gør det uegnet til behandling af blodforgiftning (bakteriæmi) og urinvejsinfektioner. Der er også rapporteret om resistensudvikling under behandling.
- Aminoglykosider (Gentamicin, Amikacin): Nogle KPC-stammer er stadig følsomme over for aminoglykosider. Disse lægemidler er effektive, men kræver nøje overvågning på grund af risikoen for nyreskader og høreskader. Deres anvendelse som monoterapi er begrænset.
- Fosfomycin: Intravenøs fosfomycin har vist sig at være en værdifuld mulighed, især i kombination med andre lægemidler. Det bruges ofte i høje doser.
Nye våben i arsenalet
Den presserende trussel fra KPC har fremskyndet udviklingen af nye antibiotika. Flere nye kombinationer af beta-lactam-antibiotika og beta-lactamase-hæmmere er nu tilgængelige og har vist sig at være yderst effektive.
| Lægemiddelklasse | Eksempler | Fordele | Ulemper |
|---|---|---|---|
| Polymyxiner | Colistin | Ofte den eneste aktive mulighed blandt ældre stoffer | Høj risiko for nyre- og nerveskader; stigende resistens |
| Glycylcycliner | Tigecyclin | Bredspektret aktivitet | Lave koncentrationer i blod/urin; resistensudvikling under behandling |
| Aminoglykosider | Gentamicin, Amikacin | Hurtig bakteriedræbende effekt hos følsomme stammer | Risiko for nyre- og høreskader; stigende resistens |
| Nye β-lactamase-hæmmer kombinationer | Ceftazidim-avibactam, Meropenem-vaborbactam | Meget effektiv mod KPC; lavere toksicitet end colistin | Dyrt; resistens kan stadig udvikle sig |
Ceftazidim-avibactam og Meropenem-vaborbactam er to af de mest lovende nye behandlinger. Avibactam og vaborbactam er hæmmere, der specifikt blokerer KPC-enzymet, hvilket genopretter aktiviteten af henholdsvis ceftazidim og meropenem. Kliniske studier har vist, at disse nye lægemidler er mere effektive og sikrere end colistin-baserede regimer til behandling af alvorlige KPC-infektioner.

Forebyggelse og infektionskontrol
I betragtning af de begrænsede behandlingsmuligheder og den høje dødelighed er forebyggelse den absolut vigtigste strategi i kampen mod KPC. Da spredningen primært sker på hospitaler og andre sundhedsfaciliteter, er strenge infektionskontrolforanstaltninger afgørende. Nøgleelementerne i en effektiv strategi omfatter:
- Aktiv overvågning: Screening af højrisikopatienter (f.eks. patienter overført fra andre hospitaler eller fra endemiske områder) for KPC-kolonisering ved hjælp af rektale podninger.
- Kontaktisolation: Patienter, der er inficerede eller koloniserede med KPC, skal isoleres i enestuer. Sundhedspersonale skal bære handsker og kittel ved al kontakt med patienten og dennes omgivelser.
- Håndhygiejne: Urokkelig overholdelse af håndhygiejneprocedurer er fundamentalt for at forhindre krydskontaminering.
- Forbedret rengøring og desinfektion: KPC-bakterier kan overleve i miljøet i lang tid. Grundig daglig rengøring og desinfektion af patientstuer og udstyr er nødvendigt.
- Antimicrobial Stewardship: Programmer, der fremmer ansvarlig og korrekt brug af antibiotika, er essentielle for at bremse udviklingen af resistens generelt.
- Patientkohorter: At samle KPC-positive patienter i et bestemt område af hospitalet med dedikeret personale kan begrænse spredningen.
Ofte Stillede Spørgsmål (FAQ)
Hvad er KPC-bakterier?
KPC-bakterier er en gruppe af bakterier, typisk Klebsiella pneumoniae og andre Enterobacteriaceae, der har udviklet resistens mod carbapenem-antibiotika. De gør dette ved at producere et enzym kaldet Klebsiella pneumoniae carbapenemase (KPC), som ødelægger antibiotikaet, før det kan virke.
Hvor farlig er en infektion med KPC?
En infektion med en KPC-producerende bakterie er meget alvorlig. Dødeligheden, især ved blodforgiftning, er høj og kan variere fra 30% til over 70%. Faren ligger i, at infektionen er ekstremt svær at behandle, da bakterien er resistent over for de fleste tilgængelige antibiotika.
Hvordan smitter KPC?
KPC spredes primært på hospitaler og plejehjem gennem direkte kontakt med en inficeret eller koloniseret person, eller indirekte via kontakt med forurenede overflader eller udstyr. Det smitter ikke gennem luften som en almindelig forkølelse.
Kan KPC-infektioner behandles?
Ja, men det er meget udfordrende. Behandlingen kræver ofte en kombination af specialiserede og nogle gange giftige antibiotika. Nyere lægemidler som ceftazidim-avibactam har forbedret prognosen betydeligt, men adgangen til disse kan være begrænset, og resistens er stadig en bekymring.
Hvem har størst risiko for at få en KPC-infektion?
De mest udsatte er patienter, der er alvorligt syge, har et svækket immunforsvar, er indlagt i længere tid (især på intensivafdelinger), har medicinske anordninger som katetre, eller som for nylig har modtaget bredspektret antibiotikabehandling.
Hvis du vil læse andre artikler, der ligner KPC: Forstå den resistente superbakterie, kan du besøge kategorien Sundhed.
