18/06/2001
Tuberkulose (TB) er en sygdom, der har plaget menneskeheden i årtusinder, og selvom vi i dag har effektive lægemidler, udgør lægemiddelresistens en voksende og alvorlig trussel mod den globale folkesundhed. En af de mest centrale aktører i denne kamp er et lægemiddel kaldet isoniazid, og en af de mest berygtede modstandere er en lille genetisk ændring i tuberkulosebakterien. Denne artikel dykker ned i den komplekse verden af Mycobacterium tuberculosis, dens sårbarhed over for isoniazid, og hvordan en specifik mutation i et gen kaldet katG kan vende hele kampen på hovedet.
Hvad er Isoniazid og Hvordan Virker Det?
Isoniazid, ofte forkortet til isoniazid (INH), har siden 1950'erne været en hjørnesten i behandlingen af tuberkulose. Det er et yderst potent lægemiddel, der er effektivt til at dræbe de bakterier, der forårsager sygdommen. Men INH's virkningsmekanisme er ikke ligetil. Det er, hvad man kalder et 'prodrug', hvilket betyder, at det er inaktivt, når det indtages. For at blive dødeligt for tuberkulosebakterien skal det først aktiveres.
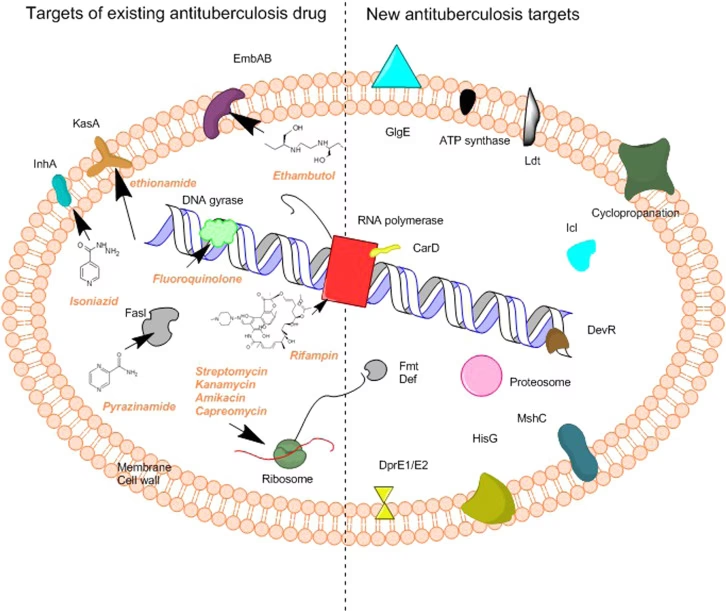
Denne aktivering sker inde i selve bakterien. Mycobacterium tuberculosis producerer et unikt enzym kaldet catalase-peroxidase, som er kodet af katG-genet. Når INH trænger ind i bakteriecellen, omdanner KatG-enzymet det inaktive INH til en aktiv, radikal form. Denne aktiverede form af lægemidlet angriber derefter adskillige vitale processer i bakterien, især syntesen af mycolsyre, som er en afgørende komponent i bakteriens cellevæg. Uden en stærk cellevæg kan bakterien ikke overleve, og den går til grunde. Denne elegante mekanisme gør INH til et målrettet og effektivt våben.
Den Centrale Rolle for katG-genet og Resistens
Da KatG-enzymet er nøglen til at aktivere INH, er det også bakteriens akilleshæl. Hvis der opstår en fejl – en mutation – i det katG-gen, der fungerer som enzymets byggeplan, kan det producerede enzym blive defekt. En mutation er simpelthen en ændring i den genetiske kode. Hvis denne ændring resulterer i et KatG-enzym, der ikke længere kan binde sig til og aktivere INH effektivt, bliver lægemidlet virkningsløst. Bakterien har dermed udviklet resistens.
Dette er den primære årsag til INH-resistens hos tuberkulosebakterier. Bakterien ofrer ikke hele enzymets funktion, men ændrer det lige nok til at undgå aktiveringen af lægemidlet. Dette er en smart overlevelsesstrategi, der desværre har enorme konsekvenser for patientbehandlingen.
S315T-mutationen: Den Mest Almindelige Skurk
Ikke alle mutationer i katG-genet er lige almindelige eller lige problematiske. Den absolut mest udbredte og klinisk relevante mutation kaldes S315T-mutationen. Denne kryptiske betegnelse dækker over en meget specifik ændring: I position 315 i enzymets aminosyrekæde bliver aminosyren Serin (S) udskiftet med aminosyren Threonin (T).
Denne tilsyneladende lille ændring har store konsekvenser. Studier viser, at S315T-mutationen findes i 40-90% af alle INH-resistente tuberkulosestammer verden over. Den er derfor en stærk markør for resistens. Det interessante ved S315T er, at den skaber en balance. Mutationen forringer enzymets evne til at aktivere INH markant, hvilket giver bakterien høj eller moderat resistens. Samtidig bevarer enzymet nok af sin oprindelige catalase-peroxidase-aktivitet til, at bakterien kan forblive levedygtig og virulent – altså i stand til at forårsage sygdom. Andre, mere drastiske mutationer, der fuldstændig ødelægger KatG-enzymet, kan svække bakterien så meget, at den har svært ved at overleve og sprede sig. S315T-stammerne er derimod både resistente og stærke, hvilket gør dem særligt farlige og succesfulde i at sprede sig mellem mennesker.
Denne mutation ses ofte i multiresistente (MDR-TB) og ekstremt resistente (XDR-TB) stammer, hvilket understreger dens alvorlige betydning for den globale TB-kontrol.
Hvordan Forskere Opdager Disse Mutationer
For at give patienter den korrekte behandling er det afgørende at vide, om deres infektion er forårsaget af en resistent stamme. Forskere og læger bruger to primære metoder til at afdække lægemiddelresistens.
Fænotypisk vs. Genotypisk Testning
Den traditionelle metode er fænotypisk testning. Her dyrker man patientens bakterier i et laboratorium og udsætter dem for forskellige koncentrationer af INH. Den laveste koncentration, der hæmmer 99% af bakteriens vækst, kaldes Minimum Inhibitory Concentration (MIC). En høj MIC-værdi indikerer resistens. Denne metode giver et direkte svar på, om lægemidlet virker, men den er langsom og kan tage flere uger.
En nyere og hurtigere metode er genotypisk testning, såsom helgenomsekventering (Whole Genome Sequencing - WGS). Her aflæser man bakteriens fulde DNA-kode og leder direkte efter kendte resistensmutationer som S315T i katG-genet. Dette giver et svar på få dage og kan guide behandlingen meget hurtigere.
Sammenligning af Diagnostiske Metoder
| Metode | Hvad den måler | Fordele | Ulemper |
|---|---|---|---|
| Fænotypisk Test (MIC) | Bakteriens faktiske modstandsdygtighed over for lægemidlet. | Giver et endegyldigt svar på resistensniveauet. Anses for guldstandarden. | Meget langsommelig (kan tage uger til måneder). Kræver specialiserede laboratorier. |
| Genotypisk Test (WGS) | Tilstedeværelsen af specifikke genetiske mutationer, der er kendt for at forårsage resistens. | Ekstremt hurtig (resultater på få dage). Giver detaljeret information om bakteriens arvemateriale. | Forudsiger resistens baseret på kendte mutationer. Kan overse nye eller sjældne resistensmekanismer. |
Konsekvenser for Behandling og Folkesundhed
Fremkomsten og spredningen af INH-resistente tuberkulosestammer, især dem med katG S315T-mutationen, har dybtgående konsekvenser. Når en patient er smittet med en sådan stamme, vil standardbehandlingen, der inkluderer INH, slå fejl. Dette fører til længere sygdomsforløb, øget risiko for at smitte andre og behov for at skifte til andengenerations-lægemidler.
Disse alternative behandlinger er ofte:
- Mindre effektive: De kræver længere behandlingsforløb, ofte op til to år.
- Mere giftige: De har flere og mere alvorlige bivirkninger, som kan være invaliderende for patienten.
- Meget dyrere: Behandlingen af en multiresistent TB-patient kan være hundredvis af gange dyrere end en standardbehandling.
Hurtig diagnostik, der kan identificere katG-mutationer, er derfor afgørende. Det giver læger mulighed for øjeblikkeligt at skræddersy en effektiv behandlingsplan og undgå at spilde dyrebar tid på et lægemiddel, der ikke virker. Det er et kapløb med tiden for at bremse spredningen af disse resistente bakterier og sikre, at vi fortsat har effektive våben i kampen mod tuberkulose.
Ofte Stillede Spørgsmål (FAQ)
Betyder en katG-mutation altid, at isoniazid er helt virkningsløst?
Ikke nødvendigvis. S315T-mutationen fører typisk til moderat til høj resistens, men ikke total immunitet. Nogle studier har undersøgt muligheden for at overvinde denne resistens ved at bruge en højere dosis af INH. Dette er dog en kompleks afvejning, da højere doser også øger risikoen for bivirkninger, og det er ikke en standardanbefaling. Effektiviteten afhænger af den specifikke MIC-værdi.
Er S315T den eneste mutation, der forårsager isoniazid-resistens?
Nej, det er den mest almindelige, men langt fra den eneste. Der findes mange andre mutationer i katG-genet samt i andre gener (f.eks. i promotoren for inhA-genet), der kan forårsage resistens. Disse andre mutationer er dog ofte forbundet med et lavere resistensniveau end S315T.
Hvorfor er bakterier med S315T-mutationen stadig farlige (virulente)?
Fordi KatG-enzymet har andre vigtige funktioner for bakteriens overlevelse end blot at aktivere INH. Det beskytter blandt andet bakterien mod oxidativt stress. S315T-mutationen er en 'perfekt' kompromisløsning for bakterien: den svækker INH-aktiveringen nok til at overleve lægemidlet, men bevarer tilstrækkelig enzymfunktion til at forblive en stærk og sygdomsfremkaldende organisme.
Kan vi bekæmpe denne form for resistens?
Ja, men det kræver en mangesidet indsats. Nøgleelementerne er: hurtig og præcis diagnostik for at identificere resistens tidligt; brug af korrekte kombinationsbehandlinger (TB behandles altid med flere lægemidler samtidigt for at minimere resistensudvikling); udvikling af nye lægemidler med nye virkningsmekanismer; og globalt fokus på at sikre, at patienter fuldfører deres behandling korrekt for at forhindre, at resistens opstår i første omgang.
Hvis du vil læse andre artikler, der ligner KatG-mutationen i Tuberkulose: En dybdegående guide, kan du besøge kategorien Sundhed.
