21/01/2017
I den komplekse verden af genetik og molekylærbiologi findes der fundamentale koncepter, som driver utrolige videnskabelige fremskridt. Et af disse, som måske lyder teknisk, men er essentielt, er begrebet k-mer. Forestil dig, at vores DNA er en gigantisk bog skrevet med kun fire bogstaver: A, T, C og G. For at forstå historien i denne bog, er forskere nødt til at bryde teksten ned i mindre, håndterbare 'ord'. En k-mer er netop det: et 'ord' af en bestemt længde (k) fra DNA-strengen. Denne simple metode til at opdele og analysere genetisk kode er en hjørnesten i moderne bioinformatik og har vidtrækkende konsekvenser for vores forståelse af sundhed og sygdom.
Hvad er en K-mer helt præcist?
En k-mer er defineret som en delsekvens af længden 'k' fra en længere DNA-sekvens. 'k' er simpelthen en variabel, der repræsenterer et tal. Hvis k=1, ser vi på individuelle bogstaver (nukleotider). Hvis k=3, ser vi på sekvenser af tre bogstaver. Ved at analysere forekomsten og fordelingen af disse k-merer kan forskere samle et væld af information om et genom uden nødvendigvis at kende hele sekvensen fra start til slut.
Lad os tage et praktisk eksempel for at illustrere konceptet. Betragt den korte DNA-sekvens: GTAGAGCTGT
Tabel: Eksempler på K-merer fra en DNA-sekvens
| K-værdi (længde) | Resulterende K-merer |
|---|---|
| k = 1 | G, T, A, G, A, G, C, T, G, T |
| k = 2 (Dinukleotider) | GT, TA, AG, GA, AG, GC, CT, TG, GT |
| k = 3 (Trinukleotider/Kodoner) | GTA, TAG, AGA, GAG, AGC, GCT, CTG, TGT |
| k = 4 (Tetranukleotider) | GTAG, TAGA, AGAG, GAGC, AGCT, GCTG, CTGT |
Som tabellen viser, genererer en højere k-værdi færre, men længere og mere specifikke, k-merer fra den samme oprindelige sekvens. Valget af 'k' afhænger af analysens formål. Små k-værdier er nyttige til at undersøge grundlæggende kompositionsmæssige skævheder, mens store k-værdier er afgørende for opgaver som at samle et helt genom fra små stykker.
De Kræfter, der Former Vores DNA's K-mer Frekvens
Hyppigheden af forskellige k-merer i et genom er ikke tilfældig. Den er formet af adskillige biologiske og kemiske kræfter, der opererer på forskellige niveauer. At forstå disse kræfter giver indsigt i genomers evolution og funktion.
Små Byggesten: k=1 og k=2
Selv på det mest basale niveau (k=1) er der en skævhed. Forholdet mellem G-C par og A-T par, kendt som GC-indhold, varierer betydeligt mellem arter og endda inden for forskellige regioner af det samme genom. G-C par er forbundet med tre hydrogenbindinger, mens A-T par kun har to, hvilket gør G-C rigere regioner mere termisk stabile. Mens man engang troede, at dette var drevet af tilpasning til temperatur, peger nyere forskning på en proces kaldet GC-partisk genkonvertering (gBGC) som en primær drivkraft. Dette er en reparationsmekanisme under rekombination, der har en tendens til at favorisere G og C nukleotider.
For k=2 (dinukleotider) ser vi også tydelige mønstre. For eksempel er CG-dinukleotidet ofte underrepræsenteret i mange genomer på grund af en proces, hvor methyleret C let kan deaminere og blive til et T. Disse dinukleotid-signaturer er bemærkelsesværdigt stabile inden for et genom og kan bruges som en slags 'genetisk fingeraftryk' til at måle den evolutionære afstand mellem beslægtede organismer.
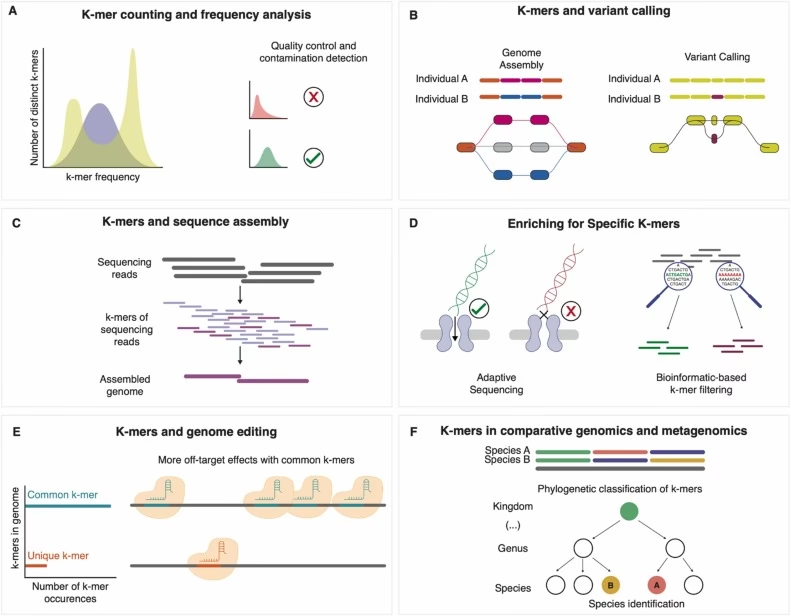
Sproget for Proteiner: k=3
Når k=3, træder vi ind i proteinernes verden. Grupper af tre nukleotider, kaldet kodoner, fungerer som instruktioner for, hvilken aminosyre der skal tilføjes til en voksende proteinkæde. Der er 64 mulige kodoner, men kun 20 aminosyrer. Det betyder, at flere kodoner kan kode for den samme aminosyre. Interessant nok bruges disse synonyme kodoner ikke med samme hyppighed. Dette fænomen, kendt som kodonbrugsbias, menes at være relateret til translationel effektivitet og nøjagtighed, hvor kodoner, der matcher mere rigelige tRNA-molekyler i cellen, foretrækkes.
Anvendelser inden for Sundhed og Medicin
K-mer analyse er ikke bare en teoretisk øvelse; det er et kraftfuldt værktøj med direkte anvendelser i sundhedssektoren.
- Genomsamling: Når forskere sekventerer et nyt genom, får de millioner af korte DNA-fragmenter. K-mer analyse er afgørende for at samle disse fragmenter korrekt, ligesom at samle et puslespil ved at matche overlappende mønstre.
- Identifikation af Patogener: Ved at analysere k-mer-frekvenser i en blod- eller vævsprøve kan man hurtigt identificere tilstedeværelsen af vira eller bakterier ved at matche deres unikke k-mer-signaturer.
- Kræftgenomik: Tumorer udvikler ofte specifikke mutationer. Ved at sammenligne k-mer-spektret fra en tumorprøve med en normal prøve kan læger identificere disse mutationer, hvilket kan guide behandlingsvalg.
- Analyse af Mikrobiom: Vores kroppe er hjemsted for billioner af mikrober. K-mer baserede metoder bruges til at analysere den genetiske sammensætning af f.eks. tarmfloraen fra en afføringsprøve, hvilket giver indsigt i vores helbred, kost og modtagelighed for sygdomme.
Ofte Stillede Spørgsmål (FAQ)
Hvad betyder det, når en analyse siger, at min prøve 'ikke har nogen k-merer af længde 8'?
Dette er en typisk fejlmeddelelse inden for bioinformatik, især i analyser som 16S rRNA-sekventering til at identificere bakterier. Det betyder højst sandsynligt, at nogle af de aflæste DNA-sekvenser er for korte (mindre end 8 nukleotider lange) eller af meget dårlig kvalitet. En sekvens, der er kortere end 'k', kan per definition ikke indeholde en k-mer af den længde. Det er en kvalitetskontrolmekanisme. I mange tilfælde er det sikkert at fjerne disse sekvenser, men hvis en stor andel af dine data giver denne fejl, kan det indikere et problem med selve sekventeringseksperimentet.
Er en længere k-mer altid bedre?
Ikke nødvendigvis. Der er en afvejning. Længere k-merer (f.eks. k=31 eller højere) er meget specifikke og er mindre tilbøjelige til at optræde tilfældigt flere steder i et genom. Dette gør dem ideelle til at identificere unikke regioner. Kortere k-merer (f.eks. k=15 til 25) er bedre til at finde overlap i fragmenterede data, hvilket er afgørende for genomsamling. Valget af 'k' er en kritisk parameter, som forskere justerer baseret på deres specifikke mål og datakvalitet.
Hvordan tælles k-merer i praksis?
At tælle milliarder af k-merer fra et helt genom er en beregningsmæssigt intensiv opgave, der kræver specialiseret software og kraftfulde computere. Værktøjer som Jellyfish, KMC og Gerbil er designet til effektivt at behandle enorme mængder sekvensdata. De bruger avancerede datastrukturer, som hash-tabeller, til at tælle og lagre forekomsten af hver unik k-mer hurtigt og med minimalt hukommelsesforbrug.
Hvis du vil læse andre artikler, der ligner K-merer: Forstå DNA's Byggesten, kan du besøge kategorien Sundhed.
