04/04/2006
JC-virus, et medlem af polyomavirusfamilien, er et patogen af betydelig interesse for lægevidenskaben. Selvom det forbliver i en sovende tilstand hos de fleste smittede individer, bærer det potentialet til at forårsage alvorlige neurologiske tilstande. Når immunforsvaret svækkes, kan virusset reaktiveres og føre til progressiv multifokal leukoencefalopati (PML), en sjælden, men ofte dødelig sygdom, der angriber hjernens hvide substans. En grundig forståelse af JC-virussets struktur, især dets kapsid, samt dets infektionsmekanismer og patogenese, er afgørende for at udvikle effektive behandlinger og diagnostiske metoder. Denne artikel vil udforske disse aspekter i dybden, belyse kroppens immunrespons og se på de nuværende forskningsindsatser, der sigter mod at bekæmpe denne formidable modstander.
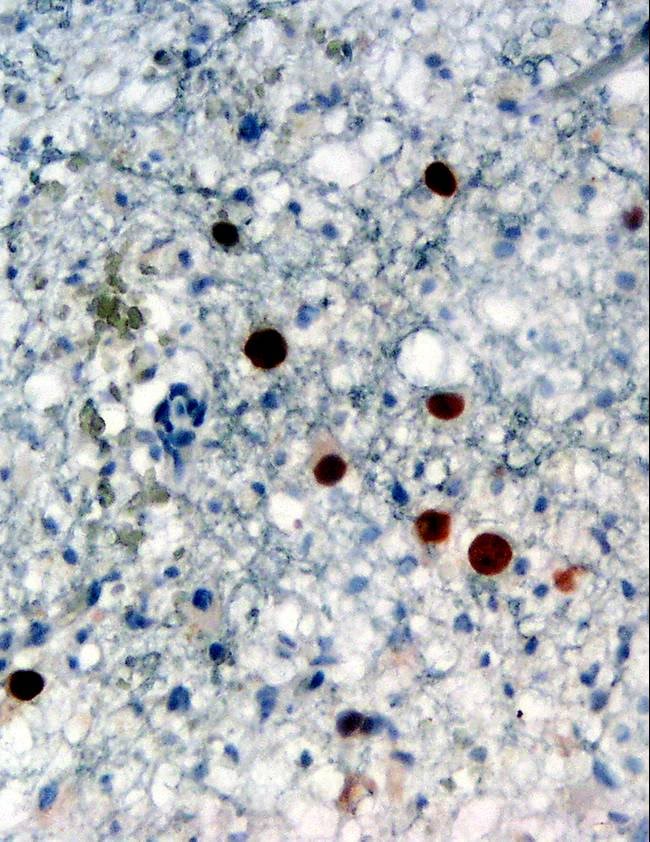
JC-Virussets Struktur: Et Nærmere Kig på Kapsidet
Kernen i forståelsen af JC-virus er dets unikke og robuste struktur. Virusset er klassificeret som et ikke-indkapslet virus, hvilket betyder, at det mangler en ydre lipidmembran. Dets beskyttende skal, kendt som kapsidet, er kendetegnet ved sin ikosaedriske form – en geometrisk struktur med 20 trekantede flader og 12 hjørner, der giver maksimal styrke og stabilitet. Dette kapsid har en diameter på cirka 40-45 nanometer, hvilket er utroligt lille, selv for en virus.
Kapsidet er bygget op af 72 pentamere kapsomerer. Forestil dig en fodbold, hvor hver lap er en gruppe af proteiner. Disse kapsomerer består primært af viralt protein 1 (VP1), som er det yderste og mest dominerende protein. VP1 spiller en afgørende rolle i virussets livscyklus, da det er ansvarligt for at binde sig til værtscellens receptorer, hvilket er det allerførste skridt i infektionsprocessen. Ud over VP1 findes også de mindre strukturelle proteiner VP2 og VP3, som er placeret inde i kapsidet og menes at spille en rolle i at stabilisere genomet og hjælpe med transporten ind i værtscellens kerne.
Inden i dette beskyttende proteinkapsid ligger virussets genetiske materiale. Genomet består af et cirkulært, dobbeltstrenget DNA-molekyle på omkring 5.130 basepar. Dette genom er ekstremt kompakt og koder for flere vigtige proteiner. Udover de strukturelle proteiner (VP1, VP2, VP3) koder det for regulatoriske proteiner, herunder det store T-antigen og det lille t-antigen. Det store T-antigen er særligt bemærkelsesværdigt for dets evne til at kapre værtscellens maskineri. Det tvinger cellen ind i en replikationsfase, hvilket skaber et ideelt miljø for produktionen af nye viruspartikler. Dette protein har også onkogene egenskaber, da det kan forstyrre cellens normale vækstreguleringsveje.
Infektionsmekanismen: Hvordan Virusset Overtager Cellen
JC-virussets infektionsproces er en nøje orkestreret sekvens af begivenheder, der udnytter værtscellens egne processer til sin fordel.
Trin 1: Binding og Indtrængen
Infektionen begynder, når virusset støder på en modtagelig celle. Ved hjælp af sit VP1-protein binder virusset sig til specifikke receptorer på celleoverfladen, som typisk er sialinsyreholdige glykoproteiner og glykosfingolipider. Denne binding er afgørende og fungerer som en nøgle i en lås. Når virusset er fastgjort, bliver det internaliseret af cellen gennem en proces kaldet clathrin-medieret endocytose. Cellen opsluger i bund og grund virusset og pakker det ind i en lille vesikel.
Trin 2: Transport til Kernen
Efter at være kommet ind i cellen, transporteres virusset gennem endosomale veje. Det bevæger sig fra tidlige endosomer til sene endosomer. I det sure miljø i de sene endosomer sker der konformationsændringer i viruskapsidet. Disse ændringer er nødvendige for at forberede frigivelsen af det virale genom. Virusset udnytter derefter værtscellens transportsystem, specifikt mikrotubuli-netværket, som en slags motorvej til at bevæge sig mod cellekernen, hvor alt cellens genetiske materiale opbevares.
Trin 3: Replikation og Samling
Når virusset når kernen, importeres dets DNA-genom ind i den. Her overtager det kontrollen. Ved hjælp af værtscellens DNA-polymerase og andre enzymer begynder virusset sin replikation. Det store T-antigen spiller en central rolle ved at aktivere transkriptionen af virale gener og starte DNA-syntesen. Efterhånden som nye virale genomer og proteiner produceres, samles de inde i kernen til tusindvis af nye viruspartikler. Til sidst akkumuleres så mange vira, at værtscellen sprænges (lyserer), hvilket frigiver de nye viruspartikler, der er klar til at inficere naboceller.
Patogenese i Hjernen: Vejen til PML
Hos de fleste mennesker forbliver JC-virus latent, typisk i nyrerne eller knoglemarven, uden at forårsage symptomer. Problemet opstår, når en persons immunforsvar bliver alvorligt kompromitteret, f.eks. hos personer med HIV/AIDS, patienter i kemoterapi eller personer, der modtager visse immunsupprimerende lægemidler. I disse tilfælde kan virusset reaktiveres og rejse til centralnervesystemet.
Man mener, at virusset krydser blod-hjerne-barrieren, muligvis ved at bruge inficerede B-lymfocytter som en 'trojansk hest'. Når det er inde i hjernen, har virusset en forkærlighed for specifikke celletyper. Dets primære mål er oligodendrocytter. Disse celler er ansvarlige for at producere myelin, et fedtholdigt stof, der danner en beskyttende skede omkring nervefibre (axoner). Myelinskeden er afgørende for hurtig og effektiv transmission af nervesignaler.
JC-virus inficerer og ødelægger oligodendrocytterne. Denne ødelæggelse fører til demyelinisering – tabet af myelinskeden – hvilket resulterer i de karakteristiske læsioner, der ses ved PML. Uden myelin kan neuronerne ikke kommunikere effektivt, hvilket fører til en bred vifte af alvorlige neurologiske symptomer. Disse kan omfatte:
- Kognitiv svækkelse (hukommelsestab, forvirring)
- Motorisk dysfunktion (svaghed i lemmer, klodsethed, lammelse)
- Synsforstyrrelser (sløret syn, tab af synsfelt)
- Talebesvær (afasi)
- Personlighedsændringer
Virusset kan også inficere astrocytter, en anden type gliacelle i hjernen, hvilket får dem til at antage en bizar, forstørret form og bidrager yderligere til hjerneskaden.
Diagnostiske Metoder: Fra Symptom til Bekræftelse
At diagnosticere PML forårsaget af JC-virus kræver en kombination af klinisk vurdering, billeddiagnostik og laboratorietests. Tidlig diagnose er afgørende, men kan være vanskelig, da de indledende symptomer ofte er vage.
Sammenligning af Diagnostiske Værktøjer
| Metode | Formål | Fordele | Begrænsninger |
|---|---|---|---|
| Magnetisk Resonans Imaging (MRI) | At visualisere de demyeliniserende læsioner i hjernens hvide substans. | Meget følsom over for at opdage de karakteristiske forandringer ved PML. Ikke-invasiv. | Kan ikke endeligt bekræfte JC-virus som årsag; andre tilstande kan ligne. |
| Polymerase Chain Reaction (PCR) | At påvise tilstedeværelsen af JC-virus DNA i cerebrospinalvæsken (CSF). | Meget specifik og følsom. Betragtes som guldstandarden for bekræftelse af aktiv infektion i hjernen. | Kræver en lumbalpunktur, som er en invasiv procedure. Virusmængden kan være meget lav i starten. |
| Hjernebiopsi | At tage en vævsprøve fra en hjernelæsion for histologisk undersøgelse. | Giver den mest definitive diagnose ved at vise både demyelinisering og tilstedeværelsen af virus. | Meget invasiv procedure med betydelige risici. Udføres sjældent og kun når andre metoder er inkonklusive. |
Nuværende Forskning og Fremtidsperspektiver
Der findes i øjeblikket ingen specifik antiviral behandling, der effektivt kan eliminere JC-virus. Den primære behandlingsstrategi for PML er at forsøge at genoprette patientens immunfunktion. Forskningen er dog i fuld gang og fokuserer på flere lovende områder:
- Antivirale Lægemidler: Forskere leder efter stoffer, der kan hæmme specifikke trin i virussets livscyklus, f.eks. ved at blokere replikationen af det virale DNA eller forhindre virusset i at trænge ind i cellerne.
- Immunbaserede Terapier: En anden tilgang er at styrke kroppens eget immunforsvar. Dette kan omfatte udvikling af terapeutiske vacciner eller infusion af JC-virus-specifikke T-celler, der kan genkende og dræbe inficerede celler i hjernen.
- Forståelse af Latens og Reaktivering: Ved at forstå de molekylære mekanismer, der holder virusset i en sovende tilstand, håber forskerne at finde måder at forhindre dets reaktivering hos patienter med immunsvækkelse.
Ofte Stillede Spørgsmål (FAQ)
Hvad betyder det, at et kapsid er ikosaedrisk?
Et ikosaedrisk kapsid er en virus' proteinskal, der er formet som et ikosaeder, en geometrisk figur med 20 identiske, trekantede sider. Denne form er ekstremt effektiv og stabil, hvilket giver maksimal beskyttelse af virussets genetiske materiale med et minimalt antal proteinenheder.
Hvem er i størst risiko for at udvikle PML?
Personer med alvorligt svækket immunforsvar er i størst risiko. Dette inkluderer patienter med fremskreden HIV/AIDS, personer der modtager visse typer kemoterapi for kræft, organtransplanterede patienter på immunsupprimerende medicin, og patienter med autoimmune sygdomme (som multipel sklerose), der behandles med specifikke lægemidler, der påvirker immunsystemet.
Findes der en kur mod PML?
Der er ingen specifik kur, der kan eliminere virusset. Den bedste chance for overlevelse og bedring er at genoprette immunforsvarets funktion så hurtigt som muligt. For eksempel hos en HIV-patient indebærer dette at starte eller optimere antiretroviral behandling. Resultatet afhænger stærkt af, hvor hurtigt immunforsvaret kan genopbygges, og hvor meget neurologisk skade der allerede er sket.
Hvordan smitter JC-virus?
Den præcise smittevej for JC-virus er ikke fuldt ud klarlagt, men det menes, at de fleste mennesker bliver smittet i barndommen eller de tidlige teenageår. Smitten er ekstremt udbredt, og op mod 80% af den voksne befolkning bærer antistoffer mod virusset. Smitten menes at ske via indånding af aerosoler eller via oral vej, men virusset forårsager ingen sygdom hos raske personer.
Hvis du vil læse andre artikler, der ligner JC Virus: Forståelse af dets Ikosaedriske Kapsid, kan du besøge kategorien Sundhed.
