28/03/2020
Influenza, almindeligt kendt som influenza, er meget mere end blot en slem forkølelse. Det er en smitsom luftvejssygdom forårsaget af influenzavirus, som hvert år fører til epidemier og i værste fald pandemier. Mens de fleste kender symptomerne som feber, hoste og ømme muskler, er de færreste klar over den intense kamp, der udkæmper sig på celleniveau. Vores krops immunforsvar har udviklet sofistikerede strategier til at opdage og eliminere virussen. En af de mest dramatiske og effektive strategier er programmeret celledød – en proces, hvor inficerede celler ofrer sig selv for at forhindre virussen i at sprede sig. Denne artikel dykker ned i den komplekse interaktion mellem influenzavirus og vores immunsystem og udforsker, hvordan denne liv-og-død-kamp er afgørende for, om vi oplever en mild sygdom eller en livstruende tilstand.
- Hvad er Influenzavirus? En Nærmere Betragtning
- Immunforsvarets Første Reaktion: Opdagelsen af Virussen
- Z-RNA: Et Skjult Signal for Fare
- Celledød som et Våben: En Dybdegående Analyse
- Nøglespillerne: ZBP1 og RIPK3-signalvejen
- Et Tveægget Sværd: Når Forsvaret Bliver til en Trussel
- Forskningsmysterier: Hvorfor er Studier Uenige?
- Ofte Stillede Spørgsmål (FAQ)
Hvad er Influenzavirus? En Nærmere Betragtning
For at forstå kroppens reaktion er det vigtigt først at forstå fjenden. Influenzavirus tilhører familien Orthomyxoviridae og findes i flere typer, hvoraf Influenzavirus A (IAV) er den mest berygtede. Det er IAV, der er ansvarlig for de fleste alvorlige epidemier og pandemier, da den kan inficere en bred vifte af arter, herunder mennesker, svin og fugle. Denne evne til at springe mellem arter giver virussen mulighed for at udvikle sig og skabe nye stammer, som vores immunforsvar ikke genkender.
En unik egenskab ved influenzavirus er dens genom. I modsætning til mange andre vira, hvis genetiske materiale er en enkelt, lang streng, består influenzavirussens genom af otte separate segmenter af RNA. Dette segmenterede RNA-genom er en afgørende faktor for virussens evne til at ændre sig hurtigt. Når to forskellige influenzastammer inficerer den samme celle, kan de udveksle RNA-segmenter og skabe en helt ny hybridvirus. Denne proces, kendt som 'antigenic shift', er årsagen til, at vi med jævne mellemrum ser nye, farlige influenzastammer dukke op.
Immunforsvarets Første Reaktion: Opdagelsen af Virussen
Når influenzavirus trænger ind i vores luftveje og begynder at inficere celler, går vores medfødte immunsystem straks i aktion. Dette er kroppens første forsvarslinje, og den er designet til at genkende generelle mønstre, der er forbundet med patogener, såkaldte PAMPs (Pathogen-Associated Molecular Patterns). For vira er et af de mest tydelige tegn tilstedeværelsen af viralt RNA inde i cellen, hvor det normalt ikke burde være.
Kroppen har specialiserede sensorproteiner, der patruljerer cellens indre. Når disse sensorer opdager viralt RNA, slår de alarm. Dette starter en kaskade af reaktioner, der har to hovedformål: at advare nærliggende celler om faren og at aktivere forsvarsmekanismer i den inficerede celle. En af de mest potente forsvarsmekanismer er at igangsætte programmeret celledød.
Z-RNA: Et Skjult Signal for Fare
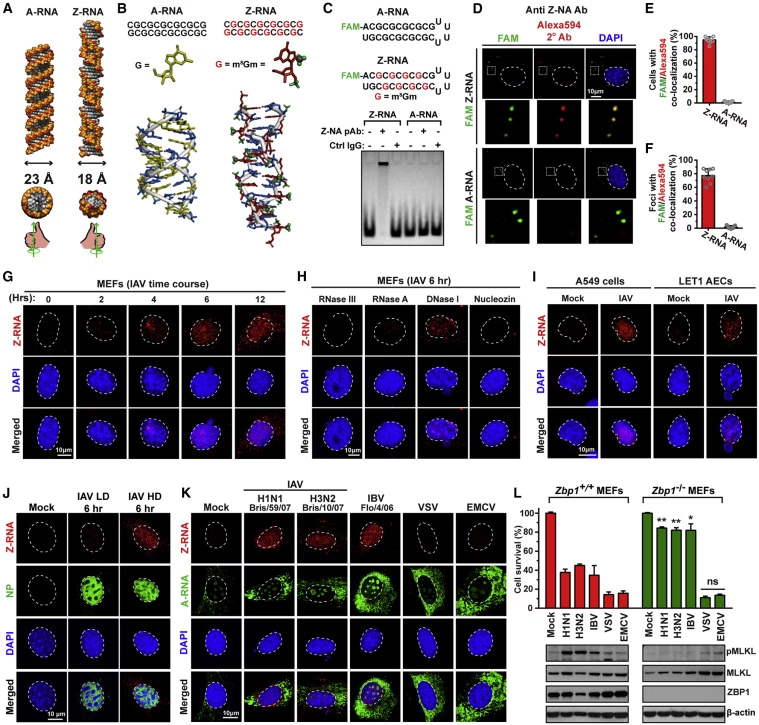
Forskere har for nylig opdaget en særlig form for viralt RNA, der spiller en afgørende rolle i immunresponset mod influenza. De fleste kender RNA som en enkelt- eller dobbeltstrenget helix, der typisk snor sig mod højre (kendt som A-RNA). Men under replikationen af influenzavirus dannes der også en usædvanlig, venstresnoet form af dobbeltstrenget RNA kaldet Z-RNA. Det viser sig, at vores celler har en specialiseret sensor, der er designet til specifikt at genkende denne Z-form.
Denne sensor er et protein kaldet ZBP1 (Z-DNA binding protein 1). Selvom navnet antyder, at det binder til DNA, har det vist sig at have en endnu vigtigere funktion i at genkende Z-RNA produceret under en virusinfektion. Når ZBP1 binder sig til Z-RNA, fungerer det som en molekylær tændsats, der aktiverer en række kraftfulde forsvarsmekanismer, herunder forskellige former for celledød.

Celledød som et Våben: En Dybdegående Analyse
Programmeret celledød er ikke en kaotisk proces. Det er en højt reguleret mekanisme, hvor cellen aktivt nedbryder sig selv på en kontrolleret måde. Formålet er at fjerne den 'fabrik', som virussen bruger til at formere sig, og samtidig begrænse skaden på det omkringliggende væv. I kampen mod influenza er der primært tre typer celledød, der er relevante.
Apoptose, Nekroptose og Pyroptose
Disse tre processer har det samme overordnede mål, men de adskiller sig i deres udførelse og de signaler, de sender til resten af immunsystemet. Forståelsen af disse forskelle er afgørende for at forstå, hvorfor en influenza-infektion kan have så forskellige udfald.
Nedenstående tabel giver et overblik over de tre centrale former for programmeret celledød:
| Type af Celledød | Beskrivelse | Rolle i Influenza-infektion |
|---|---|---|
| Apoptose | En "stille" og ordnet form for selvmord. Cellen skrumper, og dens indhold pakkes pænt i små blærer, som spises af immunceller (fagocytter) uden at skabe inflammation. | Betragtes ofte som den primære og mest gavnlige form for celledød for at kontrollere virusspredning med minimal vævsskade. |
| Nekroptose | En mere voldsom og inflammatorisk form for programmeret død. Cellen svulmer op og sprænges, hvilket frigiver dens indhold og fungerer som et kraftigt alarmsignal (DAMPs) for immunsystemet. | Kan fungere som en backup-mekanisme, hvis virussen blokerer for apoptose. Dog kan overdreven nekroptose føre til alvorlig lungebetændelse og skade. |
| Pyroptose | Betyder "ild-død". Det er en stærkt inflammatorisk proces, hvor cellen danner porer i sin membran, svulmer op og sprænges. Den er tæt knyttet til aktivering af inflammasomer og frigivelse af pro-inflammatoriske cytokiner. | Spiller en rolle i at tilkalde flere immunceller til infektionsstedet, men kan også bidrage til den farlige 'cytokinstorm', der ses ved alvorlige infektioner. |
Nøglespillerne: ZBP1 og RIPK3-signalvejen
Aktiveringen af disse celledødsprocesser er ikke tilfældig. Den styres af komplekse signalveje. Efter at ZBP1 har detekteret viralt Z-RNA, rekrutterer den et andet centralt protein ved navn RIPK3 (Receptor-interacting serine/threonine-protein kinase 3). RIPK3 fungerer som et omdrejningspunkt, der kan sende signalet i forskellige retninger.
- Mod Apoptose: RIPK3 kan interagere med andre proteiner (som FADD og Caspase-8) for at igangsætte den kontrollerede apoptose. Dette ser ud til at være den foretrukne forsvarsmekanisme mod influenza.
- Mod Nekroptose: Hvis apoptose-vejen er blokeret (noget vira ofte forsøger at gøre), kan RIPK3 i stedet aktivere et protein kaldet MLKL. MLKL er 'bødlen' i nekroptose-processen; det bevæger sig til cellemembranen og slår huller i den, hvilket får cellen til at sprænges.
Denne ZBP1-RIPK3-akse er altså en afgørende molekylær kontakt, der afgør, hvordan en inficeret celle dør. Balancen mellem den 'stille' apoptose og den 'larmende' nekroptose har stor betydning for sygdommens udfald.
Et Tveægget Sværd: Når Forsvaret Bliver til en Trussel
Selvom celledød og inflammation er essentielle for at bekæmpe infektioner, kan en overdreven eller dårligt reguleret reaktion forårsage mere skade end gavn. Ved alvorlige influenza-infektioner kan en massiv mængde nekroptose og pyroptose føre til omfattende ødelæggelse af lungevævet. Frigivelsen af store mængder inflammatoriske signaler kan udløse en såkaldt 'cytokinstorm', hvor immunsystemet går amok og angriber kroppens egne celler. Dette er ofte det, der fører til akut lungesvigt (ARDS) og død hos patienter med alvorlig influenza.
Forskningen peger på, at sværhedsgraden af influenza ikke kun afhænger af virussens aggressivitet, men i lige så høj grad af værtens immunrespons. En velafbalanceret reaktion, domineret af apoptose, kan effektivt fjerne virussen med minimale symptomer. En ude af kontrol-reaktion, domineret af nekroptose, kan føre til katastrofal sygdom.

Forskningsmysterier: Hvorfor er Studier Uenige?
Når forskere undersøger disse mekanismer i laboratoriet, ofte ved hjælp af genetisk modificerede mus, støder de på forvirrende og nogle gange modstridende resultater. I nogle studier beskytter RIPK3 mus mod influenza, mens det i andre studier ser ud til at forværre sygdommen. Hvorfor denne uenighed?
Svaret ligger sandsynligvis i de små, men afgørende forskelle i eksperimentelle opsætninger:
- Virusdosis: Effekten af en immunmekanisme kan være helt forskellig ved en lav, subletal dosis sammenlignet med en høj, dødelig dosis. En mekanisme, der er beskyttende ved lav dosis, kan blive skadelig ved høj dosis.
- Virusstamme: Forskellige stammer af influenza, f.eks. den muse-adapterede PR8-stamme versus H7N9, kan interagere forskelligt med immunsystemet.
- Administrationsvej: Om virussen gives via næsen (intranasalt) eller direkte i luftrøret (intratrakealt) kan påvirke, hvilke celler der først inficeres, og hvordan immunresponset udvikler sig.
- Måling af virusmængde: Laboratorier bruger forskellige metoder (pfu, EID50, LD50) til at kvantificere virus, hvilket gør det svært at sammenligne doser direkte.
Disse faktorer understreger kompleksiteten i immunologien og behovet for standardisering i forskningen for at kunne drage endelige konklusioner. Det er en påmindelse om, at biologi sjældent er sort-hvid.
Ofte Stillede Spørgsmål (FAQ)
Hvad er et segmenteret RNA-genom?
Et segmenteret genom betyder, at virussens genetiske information er fordelt på flere separate stykker (segmenter) af RNA i stedet for én lang streng. For influenza giver dette en evolutionær fordel, da det muliggør 'reassortment' – en proces, hvor to forskellige vira kan bytte segmenter og skabe en helt ny virusstamme, som immunsystemet ikke har set før.
Er celledød altid en god ting under en infektion?
Ikke nødvendigvis. Mens kontrolleret celledød som apoptose er afgørende for at fjerne inficerede celler og begrænse virusspredning, kan ukontrolleret eller stærkt inflammatorisk celledød som nekroptose forårsage alvorlig vævsskade. Balancen er nøglen. Et for svagt respons lader virussen løbe løbsk; et for stærkt respons ødelægger lungevævet.
Hvorfor er det så svært at forske i influenza?
Influenza er en kompleks sygdom, fordi udfaldet afhænger af en fin balance mellem tre faktorer: selve virussen, værtens genetik og værtens immunrespons. Som diskuteret i artiklen kan små ændringer i virusdosis eller -stamme føre til helt forskellige resultater i dyremodeller, hvilket gør det udfordrende at oversætte resultater direkte til mennesker.
Kan denne viden bruges til at udvikle nye behandlinger?
Absolut. Forståelsen af, hvordan ZBP1 og RIPK3 regulerer celledød, åbner op for nye terapeutiske muligheder. I stedet for kun at fokusere på at dræbe virussen (antivirale lægemidler), kan man udvikle lægemidler, der modulerer værtens immunrespons. For eksempel kunne man i tilfælde af alvorlig influenza forsøge at hæmme nekroptose-signalvejen for at reducere lungeskade og inflammation. Denne type 'værts-rettet terapi' er et lovende nyt forskningsområde.
Hvis du vil læse andre artikler, der ligner Forståelse af Influenza: Kroppens Skjulte Kamp, kan du besøge kategorien Sundhed.
