08/06/2021
Influenza, almindeligt kendt som influenza, er meget mere end blot en slem forkølelse. Det er en potentielt alvorlig luftvejssygdom forårsaget af influenzavirus, der hvert år er ansvarlig for sæsonbestemte epidemier og i værste fald globale pandemier. Historien har vist os virussens ødelæggende kraft, fra den spanske syge i 1918, der kostede millioner af menneskeliv, til nyere pandemier som H1N1 i 2009. Den konstante genetiske forandring i influenzavirus gør det til en vedvarende udfordring at udvikle rettidige og fuldt effektive vacciner. Derfor spiller antivirale lægemidler en afgørende rolle i kampen mod influenza, især mod aggressive stammer som fugleinfluenza H5N1 og H7N9.
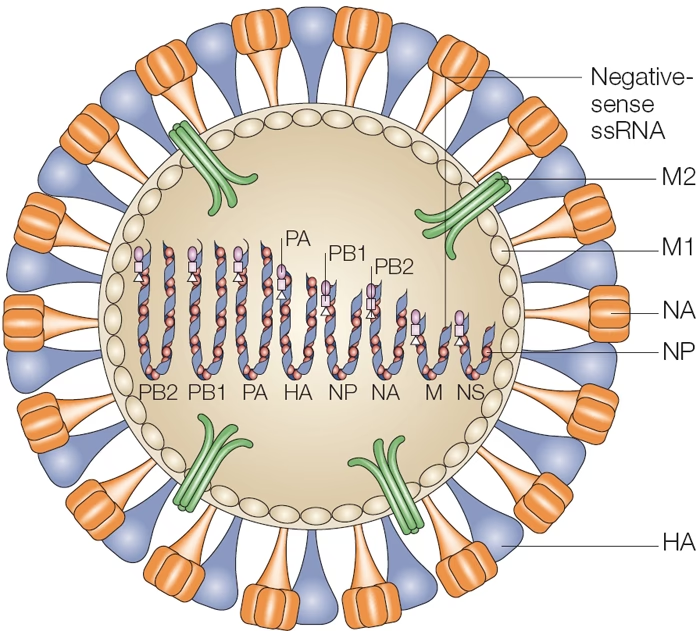
For at forstå, hvordan vi bekæmper influenza, må vi først forstå selve virussen. Influenzavirus A er en indkapslet virus med to afgørende overfladeproteiner: hæmagglutinin (HA) og neuraminidase (NA). Traditionelt har videnskaben tildelt dem meget specifikke roller: HA fungerer som nøglen, der låser op for adgang til vores celler, mens NA fungerer som saksen, der klipper de nye viruspartikler fri, så de kan inficere flere celler. Nyere forskning har imidlertid afsløret, at denne arbejdsdeling måske ikke er så sort-hvid. Der er stigende beviser for, at neuraminidase spiller en hidtil overset, men vital rolle i de allertidligste stadier af infektionen, hvilket ændrer vores grundlæggende forståelse af virussens livscyklus og åbner nye perspektiver for behandling.
Influenzavirussens Livscyklus: En Trin-for-Trin Gennemgang
For at værdsætte den nye opdagelse om NA, er det vigtigt at have en klar forståelse af influenzavirussens rejse ind i og ud af en værtscelle. Denne komplekse proces kan opdeles i fire hovedfaser:
- Binding og Indtrængen: Det hele starter, når virussen møder en potentiel værtscelle, f.eks. i vores luftveje. Her binder virussens hæmagglutinin (HA) protein sig til specifikke sukkermolekyler på cellens overflade, kendt som sialinsyrereceptorer. Denne binding er som et håndtryk, der signalerer til cellen, at den skal opsluge virussen. Cellen omslutter virussen i en lille blære kaldet et endosom.
- Frigørelse af Genetisk Materiale: Inde i endosomet falder pH-værdien (surhedsgraden stiger). Denne ændring i miljøet får virussens kappe til at smelte sammen med endosomets membran. Dette åbner en port, så virussens genetiske materiale (vRNP'er) kan frigives i cellens indre, cytoplasmaet. Herfra transporteres det ind i cellens kerne, som er cellens kontrolcenter.
- Replikation og Samling: Inde i kernen overtager virussens genetiske materiale kommandoen. Det tvinger cellens maskineri til at stoppe sit normale arbejde og i stedet producere tusindvis af kopier af virussens komponenter – både det genetiske materiale og proteiner som HA og NA. Disse nye komponenter transporteres ud af kernen og samles til nye, komplette viruspartikler ved cellens overflade.
- Frigørelse: Når de nye viruspartikler er samlet og klar til at forlade cellen for at inficere nye celler, opstår et problem. Deres eget HA-protein vil naturligt binde sig til de samme sialinsyrereceptorer på den celle, de lige er blevet skabt i. De sidder fast. Det er her, neuraminidase traditionelt set kommer ind i billedet. NA klipper disse sialinsyre-forbindelser over og frigør dermed de nye viruspartikler, så de kan sprede sig.
Neuraminidase (NA): Den Traditionelle Rolle som "Saksen"
Den klassiske forståelse af neuraminidase er, at dens primære og vigtigste funktion finder sted i infektionens absolut sidste fase. Uden NA ville influenzainfektionen stoppe brat. De nyproducerede viruspartikler, kendt som progeny-virioner, ville forblive klæbet til overfladen af den inficerede celle, ude af stand til at sprede sig. NA's enzymatiske aktivitet, kendt som sialidaseaktivitet, er afgørende. Den fungerer som en molekylær saks, der præcist klipper bindingen mellem virussens hæmagglutinin og værtscellens sialinsyre. Dette sikrer en effektiv frigørelse.
Derudover forhindrer NA også, at de nyfrigivne viruspartikler klumper sig sammen. Da de alle er dækket af HA, ville de uden NA's indgriben binde sig til hinanden og danne store, ineffektive aggregater. Ved at fjerne sialinsyre fra viruspartiklernes egne glykoproteiner sikrer NA, at hver enkelt viruspartikel er fri og mobil, klar til at finde en ny celle at inficere. Det er netop denne afgørende funktion, som de mest effektive antivirale lægemidler, neuraminidasehæmmere (NAI'er), er designet til at blokere.
En Overraskende Opdagelse: NAs Nye Rolle i Infektionens Start
I de senere år har forskere stillet spørgsmålstegn ved, om NA's rolle udelukkende er begrænset til virussens exit-strategi. Flere studier peger nu på, at NA også er en aktiv spiller i de indledende faser af infektionen – binding og indtrængen. Dette nye paradigme foreslår, at NA har mindst to yderligere funktioner i starten af livscyklussen.
For det første kan NA fungere som en slags "vejrydder". Vores luftveje er dækket af et beskyttende slimlag (mucus), som er rigt på sialinsyrer. Disse fungerer som lokkeduer, der kan fange influenzavirus, før de overhovedet når cellerne. Her kan NA's sialidaseaktivitet hjælpe virussen ved at klippe den fri fra disse slim-fælder, hvilket baner vejen mod de egentlige målceller på epitelet.
Endnu mere overraskende er opdagelsen af, at NA i visse tilfælde selv kan binde sig direkte til værtscellens receptorer. Dette udfordrer den klassiske model, hvor HA har monopol på bindingsfunktionen. Forskning har identificeret specifikke mutationer i NA-proteinet (f.eks. D151G-mutationen i H3N2-virus), som giver det en receptorbindende kapacitet. Denne funktion ser ud til at komplementere HA. Hvis HA's bindingsevne af en eller anden grund er svækket, kan NA træde til og sikre, at virussen får fodfæste på cellen. Denne dobbelte mekanisme giver virussen en øget fleksibilitet og tilpasningsevne. Denne bindingsfunktion kan, ligesom frigørelsesfunktionen, blokeres af antivirale lægemidler som Oseltamivir (Tamiflu).
Sammenligning af Neuraminidases Funktioner
| Funktion | Infektionsstadie | Mekanisme |
|---|---|---|
| Traditionel Rolle | Sen fase (Frigørelse) | Klipper sialinsyre for at frigøre nye viruspartikler fra værtscellen. Forhindrer virusaggregation. |
| Ny Rolle (Vejrydder) | Tidlig fase (Indtrængen) | Fjerner "lokkedue"-receptorer på slim, så virussen kan nå de faktiske værtsceller. |
| Ny Rolle (Binder) | Tidlig fase (Binding) | Binder direkte til værtscellens receptorer og komplementerer HA's bindingsfunktion. |
Opdagelsen af NA's dobbelte rolle har betydelige konsekvenser for, hvordan vi tænker på og udvikler behandlinger mod influenza. Neuraminidasehæmmere (NAI'er) som Oseltamivir, Zanamivir og Peramivir har i årevis været de primære våben i det medicinske arsenal mod influenza. Deres effektivitet blev oprindeligt tilskrevet deres evne til at blokere virussens frigørelse. Den nye viden bekræfter, at disse lægemidler er endnu mere potente end først antaget. Ved at hæmme NA blokerer de ikke kun virussens exit, men kan også forhindre den i at trænge ind i cellerne i første omgang. Dette giver en stærkere begrundelse for profylaktisk (forebyggende) brug af NAI'er, da de kan gribe ind på flere punkter i virussens livscyklus.
Dog er kampen mod influenza en evig kamp. Ligesom virussen udvikler resistens mod vacciner, opstår der også stammer, der er resistente over for NAI'er. Nogle virusstammer har endda udviklet dobbelt resistens mod både NAI'er og ældre lægemidler som amantadin. Derfor er det afgørende, at forskningen fortsætter. En dybere forståelse af de molekylære mekanismer, herunder den præcise balance og samspillet mellem HA og NA's funktioner, er nøglen til at udvikle en ny generation af antivirale lægemidler. Fremtidige strategier kan omfatte lægemidler, der er rettet mod andre virale mål, eller måske endda lægemidler, der kan forstyrre samspillet mellem HA og NA, og dermed lamme virussen på flere fronter samtidigt.
Ofte Stillede Spørgsmål (OSS)
Hvad er neuraminidase egentlig?
Neuraminidase (NA) er et af de to vigtigste overfladeproteiner på influenzavirus. Det er et enzym, der traditionelt er kendt for sin rolle i at klippe nye viruspartikler fri fra den inficerede værtscelle, så de kan sprede sig. Ny forskning viser, at det også kan hjælpe virussen med at trænge ind i celler i første omgang.
Hvorfor er denne nye rolle for NA vigtig?
Den ændrer vores grundlæggende forståelse af, hvordan influenza inficerer os. Det viser, at virussen er mere sofistikeret og har flere strategier for at lykkes. Det understreger også vigtigheden af de lægemidler, vi allerede har (neuraminidasehæmmere), da de virker på både virussens indgangs- og udgangsstrategi, hvilket potentielt gør dem mere effektive end tidligere antaget.
Virker nuværende influenzamedicin mod denne nye funktion?
Ja. De primære antivirale lægemidler mod influenza, de såkaldte neuraminidasehæmmere (NAI'er) som f.eks. Tamiflu, er designet til at blokere NA's enzymatiske aktivitet. Denne blokering forhindrer både den klassiske frigørelsesfunktion og den nyopdagede funktion, hvor NA hjælper med binding og indtrængen. Det gør dem til et centralt redskab i behandlingen.
Betyder det, at vi får bedre medicin mod influenza?
Potentielt ja. En dybere og mere detaljeret forståelse af virussens mekanismer er altid det første skridt mod at udvikle smartere og mere effektive lægemidler. Ved at kende alle NA's funktioner kan forskere designe nye lægemidler, der er endnu mere målrettede og bedre i stand til at overvinde det voksende problem med lægemiddelresistens.
Hvis du vil læse andre artikler, der ligner Forstå Influenza: Neuraminidases Dobbelte Rolle, kan du besøge kategorien Sundhed.

