15/03/2014
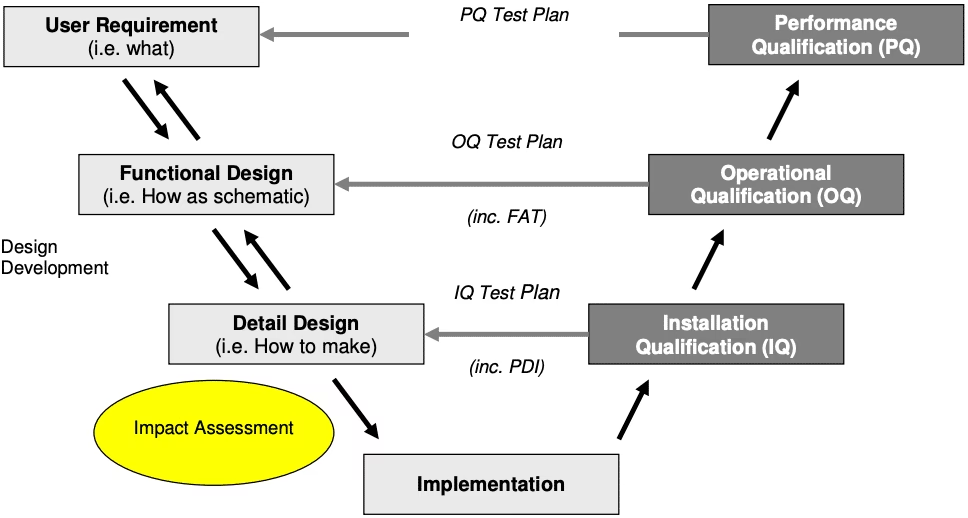
Højtydende væskekromatografi (HPLC) er en fundamental analyseteknik i mange laboratorier, især inden for medicinalindustrien, kvalitetskontrol og forskning. For at sikre, at resultaterne fra et HPLC-system er nøjagtige, pålidelige og reproducerbare, er det afgørende at gennemføre en grundig kvalifikationsproces. Denne proces sikrer, at instrumentet er egnet til sit formål, er korrekt installeret, fungerer som specificeret og konsekvent leverer resultater af høj kvalitet. Kvalifikationen er ikke en enkeltstående begivenhed, men en livscyklus bestående af fire nøglefaser: Designkvalifikation (DQ), Installationskvalifikation (IQ), Operationel Kvalifikation (OQ) og Performance Kvalifikation (PQ). Denne artikel vil guide dig gennem hver fase og give en dybdegående forståelse af, hvad der kræves for at opnå et fuldt kvalificeret HPLC-system.

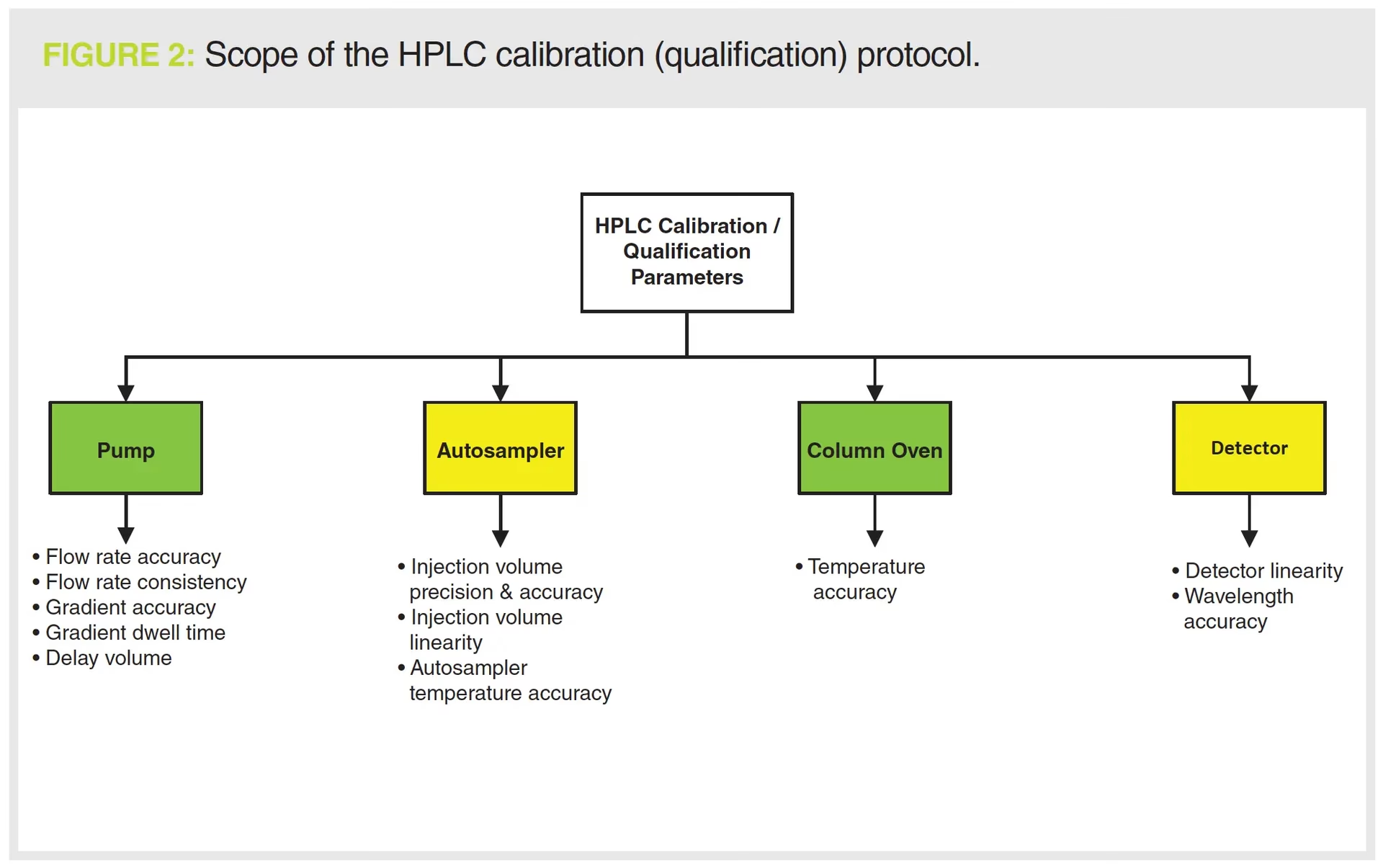
De Fire Søjler i HPLC Kvalifikation
Hele kvalifikationsprocessen kan ses som et fundament, hvor hver fase bygger oven på den foregående. Uden et solidt fundament i de tidlige faser, vil de senere faser være ustabile. De fire faser sikrer en systematisk og dokumenteret tilgang til validering af udstyret.
- Designkvalifikation (DQ): Definerer kravene til instrumentet, før det overhovedet er købt.
- Installationskvalifikation (IQ): Verificerer, at instrumentet er modtaget som bestilt og installeret korrekt i det rette miljø.
- Operationel Kvalifikation (OQ): Tester, om instrumentet fungerer i overensstemmelse med dets operationelle specifikationer.
- Performance Kvalifikation (PQ): Dokumenterer, at instrumentet konsekvent præsterer i henhold til de definerede kriterier under reelle arbejdsforhold.
Designkvalifikation (DQ): Fundamentet for Succes
Designkvalifikationen er det allerførste skridt og måske det vigtigste. Det er her, du som bruger definerer, hvad HPLC-systemet skal kunne. Formålet med DQ er at sikre, at det instrument, der overvejes til indkøb, har de nødvendige funktioner og den ydeevne, der kræves for de specifikke applikationer, det skal bruges til. En veludført DQ forhindrer dyre fejlkøb og sikrer, at udstyret fra starten er egnet til opgaven. DQ-dokumentet danner grundlaget for de tests, der senere udføres i OQ-fasen.
Nøgleelementer i en Designkvalifikation
En grundig kravspecifikation er kernen i DQ. Her er eksempler på elementer, der bør indgå:
- Tilsigtet anvendelse: Hvad skal HPLC-systemet primært bruges til? (f.eks. renhedsanalyse, kvantificering af aktivstoffer, stabilitetsstudier).
- Brugerkravspecifikation: Specifikke krav fra de personer, der skal betjene udstyret.
- Funktionelle specifikationer:
- Pumpe: Skal det være en isokratisk, binær eller kvaternær gradientpumpe? Hvilket flowområde og trykgrænse er nødvendig?
- Detektor: Hvilken type detektor er påkrævet? En Diode-Array Detektor (DAD) er ofte foretrukket for sin alsidighed.
- Autosampler: Hvad er kravet til prøvekapacitet, injektionsvolumen og temperaturkontrol?
- Kolonneovn: Er der behov for en termostateret kolonneovn for at sikre reproducerbar retentionstid?
- Computer og software: Skal softwaren overholde specifikke regulatoriske krav som f.eks. 21 CFR Part 11?
- Operationelle specifikationer:
- Detektor: Grundlinjestøj (f.eks. <5 x 10-5 AU).
- Autosampler: Præcision af injektionsvolumen (f.eks. <0,5% RSD), carry-over (f.eks. <0,1%).
- Pumpe: Præcision af retentionstid (f.eks. <0,5% RSD), præcision af blandingsforhold.
Installationskvalifikation (IQ): Korrekt Opsætning fra Start
Når instrumentet er valgt og leveret, begynder Installationskvalifikationen. IQ etablerer med dokumenteret bevis, at instrumentet er modtaget som designet og specificeret, at det er korrekt installeret i det valgte miljø, og at dette miljø er egnet til drift. Det er en systematisk gennemgang for at sikre, at alt er på plads, før man overhovedet tænder for udstyret.
Trin i Installationskvalifikationen
Processen opdeles typisk i handlinger før og under selve installationen.
Før Installation:
- Indhent producentens anbefalinger til krav for installationsstedet.
- Kontroller, at installationsstedet opfylder producentens anbefalinger (f.eks. stabil strømforsyning, temperatur- og fugtighedsforhold). Et korrekt installationsmiljø er kritisk.
- Sørg for tilstrækkelig hyldeplads til udstyr, SOP'er, manualer og software.
Under Installation:
- Sammenlign det modtagne udstyr med indkøbsordren (inklusive software, tilbehør, reservedele).
- Kontroller dokumentationen for fuldstændighed (betjeningsmanualer, vedligeholdelsesinstruktioner, sikkerhedscertifikater).
- Undersøg udstyret for eventuelle transportskader.
- Installer hardware (computer, udstyr, fittings, slanger, kolonner, strømkabler og datakabler).
- Kør en testprøve og sammenlign det opnåede kromatogram med et referencekromatogram for at verificere korrekt installation af alle moduler og forbindelser.
Operationel Kvalifikation (OQ): Fungerer Instrumentet som Forventet?
Operationel Kvalifikation er processen, hvor man demonstrerer, at instrumentet fungerer i henhold til dets operationelle specifikationer i det valgte miljø. OQ verificerer, at HPLC-systemet overholder de nøglefunktioner og operationelle krav, der blev specificeret i DQ. Det er her, man tester hver enkelt funktion af instrumentet for at sikre, at den virker korrekt og inden for de fastsatte grænser.
Sådan Opbygger du en Robust IQ/OQ-Protokol
Det er almindelig praksis at kombinere IQ- og OQ-tests i den samme protokol. Dette strømliner processen, letter fejlfinding og gør den endelige rapportering mere effektiv. Her er de vigtigste komponenter i en sådan protokol:
- Projektdetaljer: Inkluder projektnavn, udstyrsnavn, serienummer, producent, modelnummer og placering.
- Formål med protokollen: Definer klart formålet, som er at verificere installation og operationel funktion samt at fastlægge acceptkriterier.
- Protokollens omfang: Angiv præcist hvilket udstyr og hvilke delsystemer der er omfattet af protokollen.
- Beskrivelse af udstyr: Giv en detaljeret beskrivelse af udstyret og dets funktion, med fokus på GMP-relevante aspekter.
- Metodologi: Beskriv, hvordan kvalifikationsstudiet vil blive udført for at opfylde interne og eksterne krav. Henvis til eventuelle risikovurderinger.
- Acceptkriterier: Definer klare og målbare acceptkriterier for hver enkelt test. Udstyret betragtes som kvalificeret, når alle tests har opfyldt disse kriterier.
- Referencer: Angiv alle relevante dokumenter, såsom SOP'er, manualer og tidligere kvalifikationsdokumenter.
- Ansvarsfordeling: Tildel klare ansvarsområder til de involverede teams (f.eks. Validering, Ingeniørafdeling, Kvalitetssikring).
- Håndtering af afvigelser: Beskriv en procedure for, hvordan uventede afvigelser fra protokollen skal dokumenteres, undersøges og korrigeres.
- Ændringskontrol og revalidering: Etabler en procedure for håndtering af ændringer til protokollen eller udstyret.
- Appendikser: Inkluder testskemaer for hver verifikationstest.
- Underskriftsidentifikation: Opret en log, der identificerer alle personer, der deltager i kvalifikationen.
Performance Kvalifikation (PQ): Den Ultimative Test
Performance Kvalifikation er den sidste fase og har til formål at verificere og dokumentere, at HPLC-systemet fungerer som forventet under reelle, rutinemæssige forhold. Mens OQ tester individuelle funktioner under ideelle forhold, tester PQ systemets samlede ydeevne med faktiske prøver og metoder over en periode. Dette beviser, at systemet er pålideligt og egnet til sin tilsigtede anvendelse i den daglige drift.
Under PQ køres typisk en række analyser, der er repræsentative for det arbejde, systemet skal udføre. Alle procesparametre og resultater registreres og vurderes mod foruddefinerede specifikationer. Først når PQ er afsluttet med succes, kan HPLC-systemet frigives til rutinemæssig brug.
Sammenligning af Kvalifikationsfaserne
| Kvalifikationsfase | Formål | Hvornår | Nøgleaktiviteter |
|---|---|---|---|
| Design (DQ) | Sikre at det valgte design er egnet til formålet. | Før indkøb | Definere brugerkrav, funktionelle og operationelle specifikationer. |
| Installation (IQ) | Verificere at udstyret er installeret korrekt. | Ved levering og installation | Kontrol af leverance, dokumentation, installation og miljø. |
| Operationel (OQ) | Verificere at udstyret fungerer i henhold til specifikationerne. | Efter installation | Test af individuelle moduler (pumpeflow, detektorrespons, etc.). |
| Performance (PQ) | Dokumentere at udstyret konsekvent præsterer under reelle forhold. | Efter OQ og løbende | Analyse af reelle prøver, systemegnethedstest (SST), stabilitet over tid. |
Ofte Stillede Spørgsmål (FAQ)
Hvad er forskellen på OQ og PQ?
Den primære forskel ligger i testbetingelserne og formålet. OQ tester, om instrumentets individuelle komponenter *kan* fungere i henhold til deres specifikationer, ofte ved hjælp af standarder og uden en fuld kromatografisk metode. PQ tester, om hele systemet *gør* det konsekvent og pålideligt, når det bruges til en specifik analysemetode med rigtige prøver over tid.
Hvorfor er det en god idé at kombinere IQ og OQ i én protokol?
At kombinere IQ og OQ strømliner valideringsprocessen. Det giver en mere sammenhængende arbejdsgang, hvor installationen umiddelbart efterfølges af funktionstest. Dette kan reducere den samlede tid, forenkle dokumentationen, gøre fejlfinding lettere og give en mere effektiv samlet rapportering.

Skal alle HPLC-systemer kvalificeres?
Ja, i regulerede miljøer som medicinalindustrien (under cGMP) eller i laboratorier, der er akkrediteret under standarder som ISO/IEC 17025, er kvalifikation et absolut krav. Det er afgørende for at sikre dataintegritet, sporbarhed og for at kunne forsvare analyseresultater over for myndigheder. Selv i ikke-regulerede forskningsmiljøer er kvalifikation en god praksis, der sikrer kvaliteten og pålideligheden af de genererede data.
Konklusion
En systematisk og veldokumenteret kvalifikationsproces (DQ, IQ, OQ, PQ) er ikke blot et regulatorisk krav, men en fundamental del af god videnskabelig praksis og kvalitetssikring. Ved at følge disse fire faser sikrer et laboratorium, at deres HPLC-udstyr er egnet til formålet og konsekvent producerer data af højeste kvalitet. Dette opbygger tillid til analyseresultaterne, sikrer overholdelse af gældende regler og minimerer risikoen for dyre fejl og omarbejde.
Hvis du vil læse andre artikler, der ligner HPLC Kvalifikation: Fra Design til Performance, kan du besøge kategorien Sundhed.
