02/12/2011
Udvikling af lægemidler er en lang, kompleks og ekstremt omkostningstung rejse. At omdanne en videnskabelig idé til en godkendt behandling tager ofte mellem 10 og 15 år og kan koste milliarder af kroner. På trods af disse udfordringer fortsætter nye lægemidler og vacciner med at redde liv og forbedre den globale sundhed. De høje indsatser gør det klart: innovation inden for dette felt er ikke bare vigtig, den er essentiel. Processen er fyldt med usikkerhed, hvor færre end 10% af de eksperimentelle terapier, der påbegynder forsøg i mennesker, nogensinde opnår myndighedsgodkendelse. Denne virkelighed lægger et enormt pres på forskere for at arbejde smartere, hurtigere og mere effektivt.
- Faserne i Lægemiddeludvikling: En Oversigt
- Trin 1: Målidentifikation og Validering
- Trin 2: Lead-Opdagelse og Optimering
- Trin 3: Præklinisk Udvikling
- Trin 4: Kliniske Forsøg i Mennesker
- Trin 5: Myndighedsgodkendelse og Overvågning
- Traditionel vs. AI-drevet Lægemiddeludvikling
- Udfordringer og Fremtidsudsigter
- Ofte Stillede Spørgsmål (FAQ)
- Konklusion
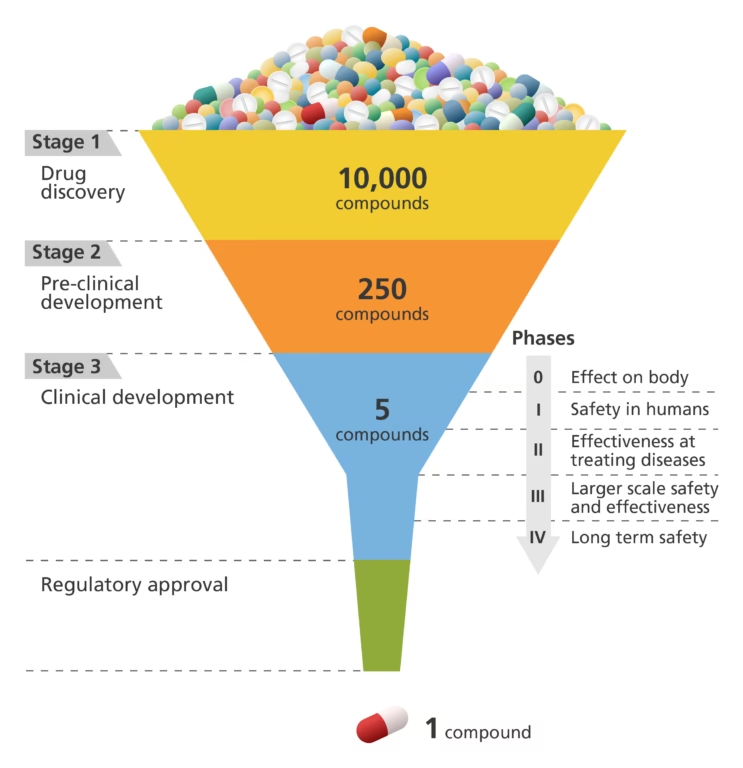
Faserne i Lægemiddeludvikling: En Oversigt
Processen kan groft opdeles i flere nøglefaser, der hver især bygger på den foregående. Fra den indledende opdagelse af et potentielt mål i kroppen til de afsluttende godkendelsesprocedurer er hver etape kritisk for succes. Disse faser omfatter målidentifikation, lead-opdagelse og -optimering, prækliniske studier, kliniske forsøg i flere faser, og til sidst den regulatoriske godkendelse og efterfølgende markedsovervågning.
Trin 1: Målidentifikation og Validering
Det allerførste skridt i opdagelsen af et nyt lægemiddel er at identificere et biologisk mål, der er knyttet til en specifik sygdom. Disse mål kan være proteiner, receptorer, enzymer eller gener, som spiller en nøglerolle i sygdommens udvikling. Forskere bruger ofte genetisk forskning, sygdomsbiologi og screeningsteknikker til at afdække disse mål. For eksempel kan genom-dækkende associationsstudier (GWAS) afsløre gener, der er forbundet med en bestemt tilstand, mens CRISPR-screens kan hjælpe med at identificere essentielle biologiske signalveje.
Traditionelt involverede opdagelsen af mål en kombination af laboratorieforskning og kliniske data. Forskere testede tusindvis af stoffer i sygdomsmodeller for at finde stærke kandidater. Ud af tusindvis af potentielle leads er det kun få, der viser tilstrækkelig relevans til at gå videre. Dette gør den tidlige opdagelsesfase til en af de mest ressourcekrævende etaper i hele processen. Nu omformer kunstig intelligens (AI) og big data dette trin. Værktøjer drevet af store sprogmodeller kan scanne massive biomedicinske datasæt på sekunder, analysere videnskabelige artikler, patenter og genetiske databaser for at spotte nye terapeutiske mål, som forskere måske ellers ville overse.
Trin 2: Lead-Opdagelse og Optimering
Når forskere har valideret et mål, er næste skridt at finde en såkaldt "lead-forbindelse". Her søger forskere efter kemiske "hits", der kan binde sig til målet og udvise biologisk aktivitet. Disse molekyler skal interagere med målet på en måde, der potentielt kan føre til en terapeutisk fordel. Traditionelt indebar denne proces at screene tusindvis af stoffer fra store kemiske biblioteker. Hvert lovende hit gennemgik derefter flere runder af kemisk optimering for at forbedre styrke, selektivitet og lægemiddellignende egenskaber.
I dag accelererer AI denne proces dramatisk. I stedet for fysisk at screene massive biblioteker bruger forskere nu virtuelle kemiske biblioteker og deep-learning-modeller. Disse modeller kan forudsige, hvilke stoffer der sandsynligvis vil binde sig effektivt og sikkert. Et skelsættende eksempel kom i 2020, da MIT-forskere brugte AI til at opdage et nyt antibiotikum, halicin, som viste sig effektivt mod lægemiddelresistente bakterier. Efter identifikation af hits følger optimeringen, hvor man evaluerer, hvordan stoffet opfører sig i kroppen. AI hjælper også her ved at forudsige, hvilke kemiske justeringer der vil forbedre ydeevnen eller reducere bivirkninger, hvilket minimerer gætværk og mislykkede eksperimenter.
Trin 3: Præklinisk Udvikling
Efter at have udvalgt en lovende lead-forbindelse, går den ind i præklinisk udvikling. Denne fase involverer strenge laboratorietests, før der overhovedet kan blive tale om forsøg i mennesker. Forskere udfører in vitro-eksperimenter (i cellekulturer) og in vivo-studier (i dyremodeller) for at vurdere det nye stofs biologi, effekt og toksicitet. Målet er at afgøre, om lægemidlet virker sikkert nok til at blive testet i mennesker.
Alle prækliniske laboratoriearbejder skal følge standarder for God Laboratoriepraksis (GLP) for at sikre dataintegritet og kvalitet. Typiske prækliniske studier undersøger:
- Toksicitet: Test af doser i dyr for at finde skadelige virkninger.
- Farmakologi: Vurdering af, hvordan lægemidlet absorberes, distribueres, metaboliseres og udskilles (ADME).
- Formulering: Udvikling af en stabil doseringsform (pille, injektion osv.).
Disse prækliniske studier kan tage flere år at gennemføre. Kun hvis data viser en acceptabel sikkerhedsprofil, kan sponsoren ansøge om at starte forsøg i mennesker.
Trin 4: Kliniske Forsøg i Mennesker
Hvis de prækliniske resultater er positive, går lægemidlet videre til kliniske forsøg – studier i frivillige mennesker – for grundigt at vurdere sikkerhed og effekt. Den kliniske forskning er typisk opdelt i tre progressive faser:
Fase I
De første tests i mennesker involverer en lille gruppe på 20-100 raske frivillige (eller patienter, for visse sygdomme). Disse forsøg fokuserer primært på sikkerhed, tolerabilitet og grundlæggende farmakologi. Deltagerne modtager lægemidlet i stigende doser, mens forskere overvåger bivirkninger og hvordan kroppen behandler lægemidlet. Fase I fastlægger det sikre dosisområde for yderligere test.
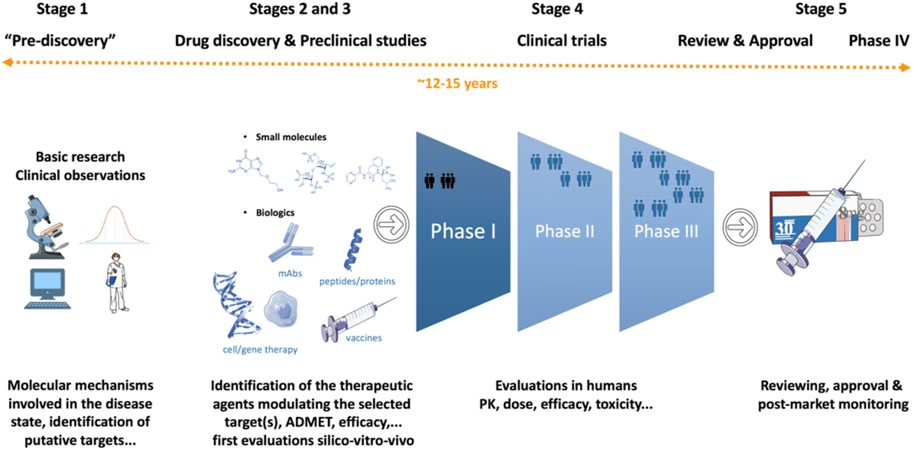
Fase II
Fase II-forsøg omfatter hundreder af patienter, der har den pågældende sygdom. Disse studier tester, om lægemidlet har nogen terapeutisk effekt, og fortsætter med at overvåge sikkerheden. Fase II er ofte randomiseret og kan inkludere en placebo- eller standardbehandlings-kontrolgruppe. Det hjælper med at identificere den optimale dosis. Cirka 30% af lægemidlerne fejler i denne fase på grund af utilstrækkelig effekt eller sikkerhedsproblemer.
Fase III
Dette er de afgørende forsøg med hundreder til tusinder af patienter. Fase III sigter mod at levere endegyldigt bevis for, at lægemidlet virker (effekt) og er sikkert til bredere anvendelse. Store, multicenterstudier sammenligner det nye lægemiddel med placebo eller standardbehandling. De indsamler de fleste sikkerhedsdata og identificerer sjældne bivirkninger. Kun omkring en tredjedel af de lægemidler, der går ind i fase III, gennemfører dette stadie med succes.
Trin 5: Myndighedsgodkendelse og Overvågning
Efter vellykkede fase III-forsøg samler sponsoren alle data til en regulatorisk gennemgang. I Europa betyder det typisk en ansøgning til Det Europæiske Lægemiddelagentur (EMA). Ansøgningspakken er omfattende og indeholder alle prækliniske og kliniske studierapporter, statistiske analyser, foreslået mærkning og produktionsdetaljer. Målet er at demonstrere, at lægemidlet er sikkert og effektivt til den tilsigtede anvendelse.
Myndighederne evaluerer derefter ansøgningen. En standardgennemgang kan tage omkring et år, men der findes hurtigere veje for lægemidler, der opfylder presserende, udækkede behov. Hvis det godkendes, er lægemidlet klar til markedsføring. Men udviklingen slutter ikke her. Overvågning efter markedsføring (ofte kaldet fase IV) fortsætter med at vurdere lægemidlets ydeevne i den virkelige verden. Efterhånden som millioner af patienter bruger terapien, dukker der flere data op om sikkerhed og effektivitet. Denne proces sikrer, at lægemidlets sande fordele og risici bliver tydeligere over tid.
Traditionel vs. AI-drevet Lægemiddeludvikling
Den teknologiske udvikling, især inden for kunstig intelligens, er i gang med at transformere hele landskabet for lægemiddelopdagelse. Nedenstående tabel sammenligner den traditionelle tilgang med den nye, AI-drevne metode.
| Aspekt | Traditionel Tilgang | AI-drevet Tilgang |
|---|---|---|
| Målidentifikation | Eksperimentel screening, manuel litteraturgennemgang | AI-modeller scanner data og litteratur for at finde nye mål |
| Lead-Opdagelse | High-throughput screening af fysiske stoffer | Virtuel screening og generativt design af nye molekyler |
| Præklinisk Evaluering | In vitro/in vivo studier (dyreforsøg) | Forudsigende toksikologimodeller, organ-on-chip |
| Design af Kliniske Forsøg | Protokoller fastsat af ekspertkomitéer | AI-drevne adaptive designs; algoritmer til patientvalg |
| Tid til Klinik | Årtier | Potentielt reduceret med 30-50% i tidlige faser |
| Succesrate | ~1 ud af 10 kandidater når markedet | Tidlige tegn på højere succesrate i fase I |
Udfordringer og Fremtidsudsigter
Selvom teknologien forbedrer effektiviteten, er omkostninger, tid og fejl-rater fortsat store udfordringer. At udvikle et nyt lægemiddel koster stadig milliarder, hovedsageligt på grund af fejl i de sene stadier. Den gennemsnitlige tid fra opdagelse til marked er stadig omkring et årti. Nuværende tendenser som accelererede godkendelser, personlig medicin og digitale forsøg hjælper med at forme en mere effektiv fremtid. Især personlig medicin, hvor lægemidler skræddersys til patientundergrupper baseret på biomarkører, viser stort potentiale. Udsigterne er dog lovende. AI er ved at transformere landskabet ved at muliggøre mere effektiv målidentifikation og beslutningstagning. I den nærmeste fremtid kan vi se hybridteams af mennesker og AI, hvor forskere bruger intelligente assistenter i hvert trin af processen, hvilket bringer håb til patienter over hele verden.
Ofte Stillede Spørgsmål (FAQ)
- Hvor lang tid tager det at udvikle et nyt lægemiddel?
- Det tager typisk mellem 10 og 15 år fra den indledende opdagelse til et lægemiddel er godkendt og tilgængeligt på markedet.
- Hvorfor er lægemiddeludvikling så dyrt?
- Omkostningerne er høje primært på grund af den ekstremt høje fejl-rate. Over 90% af lægemiddelkandidaterne fejler undervejs, og omkostningerne til disse fejl skal dækkes af de få succesfulde lægemidler. De lange og komplekse kliniske forsøg er også en stor udgift.
- Hvad er forskellen på prækliniske og kliniske forsøg?
- Prækliniske forsøg udføres i laboratoriet (i celler og dyr) for at vurdere grundlæggende sikkerhed og virkningsmekanisme, før et lægemiddel testes i mennesker. Kliniske forsøg udføres i mennesker i flere faser for at bekræfte sikkerhed og effekt i en virkelig population.
- Hvordan ændrer kunstig intelligens (AI) lægemiddelopdagelse?
- AI accelererer processen ved at analysere enorme mængder data for at identificere nye sygdomsmål, designe nye molekyler virtuelt, forudsige toksicitet og optimere designet af kliniske forsøg. Dette kan potentielt reducere både tid og omkostninger markant.
Konklusion
Rejsen fra laboratoriebænk til patientens sengebord er en monumental opgave, der involverer mange stadier: identifikation af et biologisk mål, opdagelse og optimering af stoffer, strenge prækliniske og kliniske tests, og navigation i komplekse regulatoriske processer. Takket være digital innovation er landskabet for lægemiddelopdagelse i rivende udvikling. Kunstig intelligens og datadrevne værktøjer strømliner forskningen og muliggør hurtigere hypotesegenerering og smartere kandidatvalg. Selvom udfordringerne er store, forbliver kernemissionen den samme: at levere sikre og effektive nye terapier til patienter. Ved at integrere banebrydende teknologi med streng videnskab sigter medicinalindustrien mod at forkorte tidslinjer, reducere omkostninger og forbedre succesraterne til gavn for os alle.
Hvis du vil læse andre artikler, der ligner Lægemiddelopdagelse: Fra idé til patient, kan du besøge kategorien Sundhed.

