28/11/2019
Human immundefektvirus, bedre kendt som HIV, er en mester i at infiltrere det menneskelige immunsystem. Kernen i dens succes ligger i en sofistikeret molekylær mekanisme, der tillader den at låse sig fast på og trænge ind i værtsceller. Denne mekanisme er drevet af et kompleks af proteiner på virussens overflade, kendt som envelope glykoproteinet (Env). Dette kompleks består af to tæt forbundne enheder, gp120 og gp41, der tilsammen fungerer som virussens nøgle til at låse op for vores celler. At forstå den detaljerede tredimensionelle struktur og funktion af dette gp120-gp41-kompleks er ikke kun en akademisk øvelse; det er afgørende for at designe effektive lægemidler og en længe ventet vaccine.
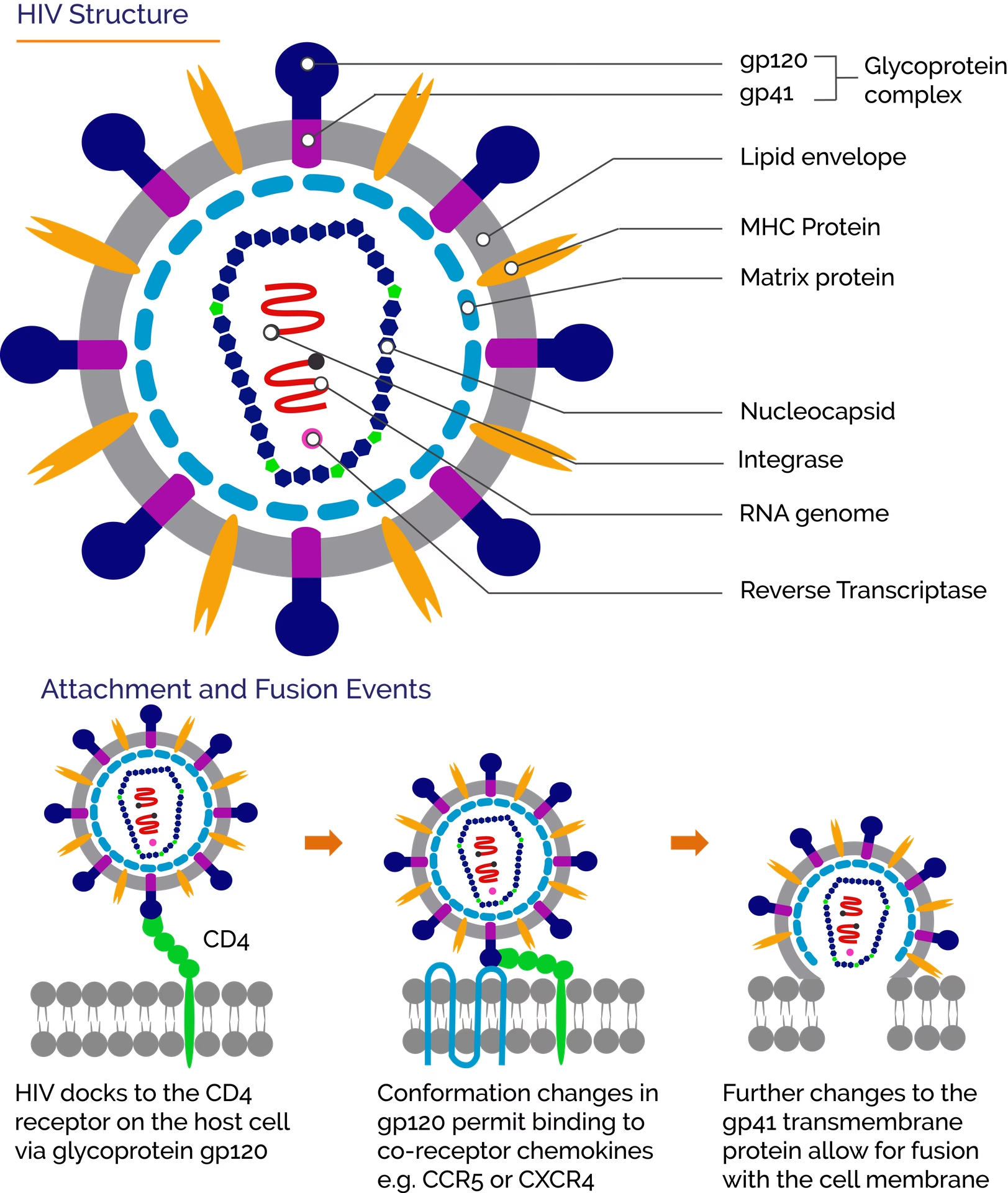
Den Overordnede Arkitektur: Et Tredelt Tårn
Forestil dig HIV-virussen som en kugle dækket af pigge. Hver af disse pigge er et Env-kompleks. Strukturen er ikke blot et enkelt molekyle, men en trimer – det vil sige, den består af tre identiske enheder af gp120-gp41 heterodimerer, der er samlet i en svampelignende form. Oprindeligt syntetiseres disse proteiner som et enkelt, stort forstadieprotein kaldet gp160. Inde i den inficerede celle bliver gp160 kløvet af værtscellens enzymer (specifikt furin) til de to funktionelle underenheder: overfladeproteinet (SU) gp120 og det transmembrane protein (TM) gp41. Selvom de er kløvet, forbliver de tæt, men ikke-kovalent, bundet til hinanden. Denne forbindelse er afgørende, men også sårbar, hvilket virussen udnytter i sin livscyklus.
Hele komplekset er tungt glykosyleret, hvilket betyder, at det er dækket af sukkermolekyler. Denne "sukkersky" udgør næsten halvdelen af kompleksets samlede masse og fungerer som et skjold, der skjuler de mere konserverede dele af proteinerne for kroppens immunsystem. Dette er en af hovedårsagerne til, at det har været så utroligt svært at udvikle en effektiv vaccine.
gp120: Virussens Fangarme
gp120 udgør den yderste del af Env-piggen – selve "hovedet" af svampen. Dets primære opgave er at genkende og binde sig til specifikke receptorer på overfladen af immunceller, primært T-hjælperceller. Den primære receptor er et molekyle kaldet CD4.
Strukturelt er gp120 opdelt i konserverede (C1-C5) og hypervariable (V1-V5) regioner. De konserverede regioner er essentielle for proteinets grundlæggende struktur og funktion, herunder bindingen til CD4. De hypervariable loops er derimod under konstant evolutionært pres og muterer hurtigt. Dette skaber en bevægelig, evigt foranderlig overflade, der gør det svært for antistoffer at få et solidt greb. Bindingen mellem gp120 og CD4-receptoren er det første, afgørende skridt i infektionsprocessen. Denne interaktion er ikke passiv; den udløser en dramatisk kaskade af konformationsændringer i hele Env-komplekset.
gp41: Den Skjulte Fusionsmaskine
Mens gp120 er spejderen, er gp41 henrettelsesmanden. Det er et transmembrant protein, hvilket betyder, at en del af det er forankret i selve virusmembranen, mens en anden del strækker sig ud og interagerer med gp120. I sin hvilende tilstand er gp41 foldet i en metastabil, energirig konformation, hvor dens mest potente del – fusionspeptidet – er skjult dybt inde i komplekset.
gp41's struktur indeholder flere nøgleelementer:
- Fusionspeptid: En kort, hydrofob sekvens ved N-terminalen, der fungerer som en harpun.
- Heptad Repeats (HR1 og HR2): To regioner med en tendens til at danne spiralformede strukturer (alfa-helixer). Disse regioner er afgørende for den endelige fusionsproces.
- Membran-Proximal External Region (MPER): En højt konserveret region tæt på virusmembranen, som er et mål for nogle sjældne, men potente, bredt neutraliserende antistoffer.
Når gp120 binder til CD4, sker der en omstrukturering, der afslører et nyt bindingssted på gp120 for en co-receptor, typisk CCR5 eller CXCR4. Først når gp120 har bundet til BÅDE CD4 og en co-receptor, udløses den fulde konformationsændring i gp41. Denne ændring er som at slippe en spændt fjeder. Fusionspeptidet skydes fremad og borer sig ind i værtscellens membran.
En Trin-for-Trin Guide til HIV's Indtrængen
Hele processen kan sammenfattes i en række præcist koreograferede trin, der illustrerer den utrolige effektivitet af denne molekylære maskine:
- Binding: gp120-delen af Env-piggen binder sig til en CD4-receptor på en T-celle.
- Konformationsændring og Co-receptor Binding: Den første binding får gp120 til at ændre form. Dette afslører et bindingssted for en co-receptor (CCR5 eller CXCR4), som gp120 efterfølgende binder sig til.
- Aktivering af gp41: Denne dobbelte binding sender et signal til gp41, som nu gennemgår sin egen dramatiske konformationsændring. Den går fra sin inaktive, metastabile tilstand til en aktiv, pre-hairpin intermediær tilstand.
- Membran-insertion: gp41's fusionspeptid skydes ud og integreres i værtscellens membran, hvilket skaber en fysisk bro mellem virus og celle.
- Kollaps og Fusion: gp41 kollapser nu ind i sin mest stabile form. HR2-regionen folder sig tilbage og lægger sig op ad HR1-regionen, hvilket danner en ekstremt stabil seks-helix-bundtstruktur. Denne foldningsproces trækker de to membraner – virussets og cellens – tæt sammen, indtil de smelter sammen. Indholdet af virussen, herunder dens genetiske materiale, kan nu strømme ind i cellen, og infektionen er en realitet.
Udfordringer og Muligheder for Behandling
Den detaljerede viden om gp120-gp41-komplekset har åbnet døren for målrettede behandlingsstrategier. Den konstante mutation af gp120's variable loops er en enorm udfordring for vaccineudvikling. Men de konserverede regioner, der er nødvendige for funktion, er attraktive mål.

En succesfuld klasse af lægemidler er fusionshæmmere. Det mest kendte eksempel er Enfuvirtide (T-20). Dette lægemiddel er et syntetisk peptid, der efterligner en del af gp41's HR2-region. Det virker ved at binde sig til HR1-regionen under pre-hairpin-intermediatet. Derved blokerer det gp41 i at fuldføre sin foldning til seks-helix-bundtet, og fusionen forhindres. Virussen er effektivt stoppet ved celledøren.
Forskere arbejder også intenst på at identificere og fremkalde bredt neutraliserende antistoffer (bNAbs), som er antistoffer, der kan genkende de konserverede, funktionelt vigtige dele af Env-komplekset, som er fælles for mange forskellige HIV-stammer. Ved at forstå præcis, hvor disse antistoffer binder, kan forskere designe immunogener (vaccinekomponenter), der specifikt træner immunsystemet til at producere netop disse effektive antistoffer.
Sammenligning af gp120 og gp41
| Egenskab | gp120 | gp41 |
|---|---|---|
| Primær Funktion | Receptor-binding (CD4 og co-receptor) | Membranfusion |
| Placering | Ydre overflade af Env-komplekset | Transmembran, forankret i virusmembranen |
| Nøglestrukturer | Konserverede regioner, variable loops (V1-V5), CD4-bindingssted | Fusionspeptid, Heptad Repeats (HR1, HR2), seks-helix-bundt |
| Variabilitet | Meget høj, især i V-loops | Relativt lav, da mekanismen er stærkt konserveret |
| Rolle som Lægemiddelmål | Mål for neutraliserende antistoffer og bindingshæmmere | Mål for fusionshæmmere (f.eks. Enfuvirtide) |
Ofte Stillede Spørgsmål (FAQ)
Hvad er den grundlæggende forskel på gp120 og gp41?
Den grundlæggende forskel ligger i deres funktion. gp120 er 'genkendelses'-delen, der binder til værtscellens receptorer. gp41 er den 'mekaniske' del, der efterfølgende udfører selve sammensmeltningen af virus- og cellemembranen.
Hvorfor er det så svært at lave en vaccine mod HIV's overfladeproteiner?
Der er to hovedårsager. For det første muterer de ydre, variable loops på gp120 ekstremt hurtigt, så immunsystemet konstant jager et bevægeligt mål. For det andet er hele komplekset dækket af et tæt skjold af sukkermolekyler (glykaner), som fysisk blokerer adgangen for mange antistoffer til de mere sårbare, konserverede dele af proteinet.
Hvordan virker fusionshæmmere som medicin?
Fusionshæmmere virker ved at afbryde den mekaniske proces, som gp41 udfører. De binder sig til gp41 i et kritisk mellemstadium (pre-hairpin intermediatet) og forhindrer det i at folde sig færdigt. Dette svarer til at kaste en skruenøgle ind i en maskine; processen går i stå, og fusionen kan ikke gennemføres.
Hvad betyder det, at gp41 er i en 'metastabil' tilstand?
En metastabil tilstand betyder, at proteinet er i en midlertidig, energirig form, der er stabil nok til at eksistere, men som venter på et signal (en trigger) for at kollapse til en meget mere stabil, lavere energitilstand. For gp41 er den hvilende form metastabil. Bindingen til receptorerne er triggeren, der tillader den at kollapse til den ekstremt stabile seks-helix-bundtstruktur, hvorved den frigiver den energi, der er nødvendig for at drive membranfusionen.
Afslutningsvis er HIV's gp120-gp41-kompleks et storslået eksempel på molekylær evolution. Det er en elegant, men dødelig maskine, der er perfektioneret til at omgå vores immunsystem og invadere vores celler. Men ved at afdække dets strukturelle hemmeligheder, bid for bid, giver forskere os de værktøjer, vi har brug for til at sabotere denne maskine og i sidste ende besejre virussen.
Hvis du vil læse andre artikler, der ligner HIV's Nøgle: Forståelse af gp120-gp41 Strukturen, kan du besøge kategorien Sundhed.
