25/09/2002
For tyve år siden opdagede videnskaben en ny type enzymer kaldet histon lysin demethylaser, eller KDM'er. Siden da har forskningen taget fart, og det er blevet klart, at disse små molekylære maskiner spiller en fundamental rolle i alt fra udviklingen af arter til de komplekse processer i vores egen krop. Deres betydning er især kommet i fokus i forbindelse med sygdomme som kræft, hvor de har vist sig at være både en del af problemet og en potentiel del af løsningen. Denne artikel dykker ned i KDM'ernes verden for at forstå, hvad de er, hvorfor de er så vigtige, og hvordan de kan blive nøglen til fremtidens medicin.
Epigenetik: Den Skjulte Styring af Vores Gener
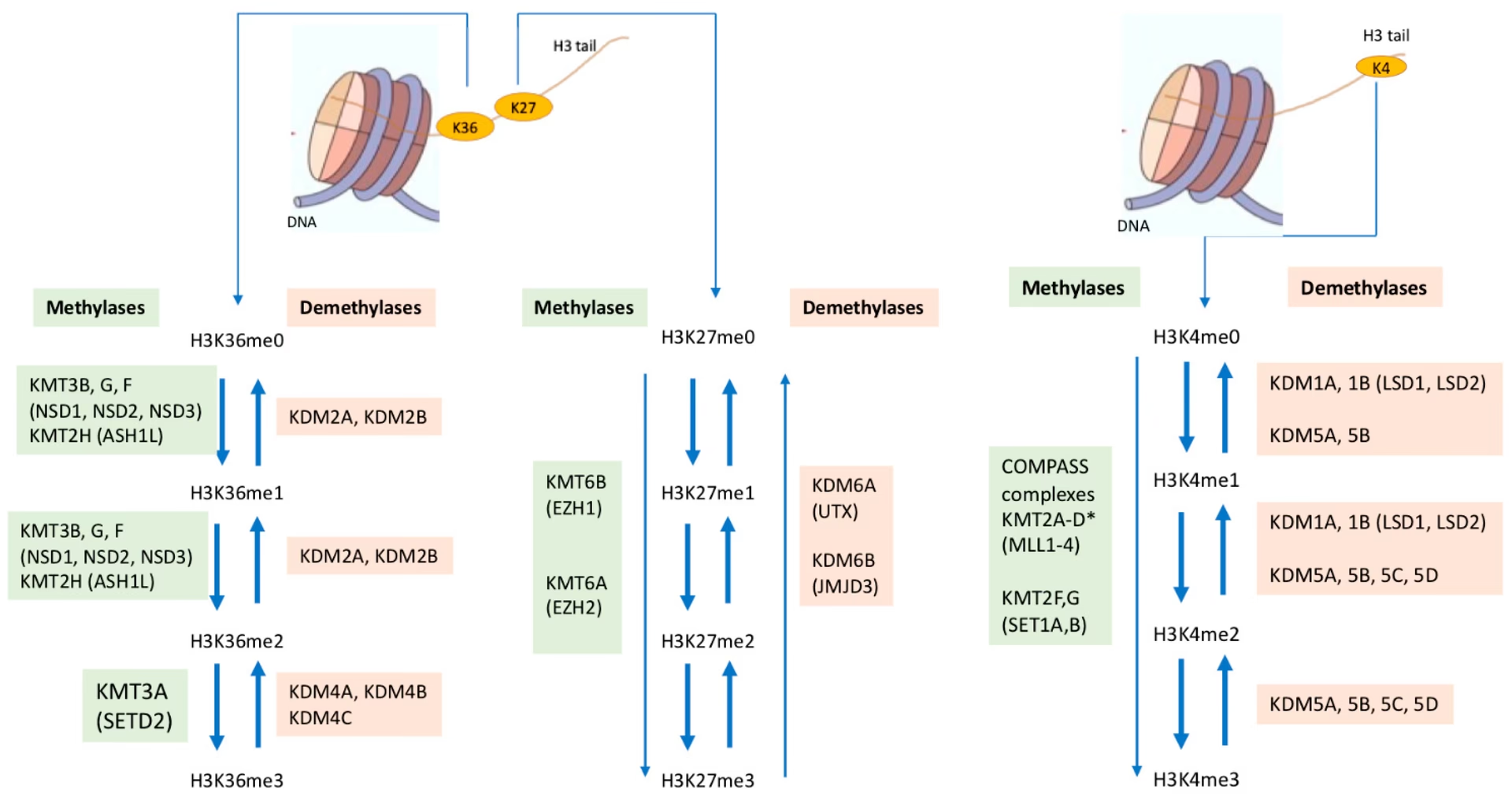
For at forstå KDM'er må vi først se på det felt, de tilhører: epigenetik. Vores DNA indeholder opskriften på, hvem vi er, men det er epigenetikken, der bestemmer, hvilke dele af opskriften der skal læses, og hvornår. Forestil dig DNA som en enorm kogebog. Epigenetikken er de små noter, bogmærker og overstregninger, der fortæller kokken (cellen), hvilke opskrifter der skal bruges i dag. Disse ændringer sker uden at ændre selve DNA-sekvensen.
En af de vigtigste måder, cellen gør dette på, er ved at modificere de proteiner, som DNA'et er viklet omkring. Disse proteiner kaldes histoner. Små kemiske grupper kan sættes på og tages af histonerne, hvilket enten gør DNA'et mere eller mindre tilgængeligt for at blive læst. Dette system er utroligt dynamisk og afgørende for cellens funktion.
De Tre Hovedaktører: "Skrivere", "Viskelædere" og "Læsere"
Inden for epigenetikken taler man ofte om tre typer regulatorer, der styrer disse kemiske modifikationer:
- "Skrivere" (Writers): Enzymer, der tilføjer kemiske mærker (som methylgrupper) til histonerne.
- "Viskelædere" (Erasers): Enzymer, der fjerner disse mærker igen.
- "Læsere" (Readers): Proteiner, der genkender og binder sig til specifikke mærker, og derefter igangsætter en biologisk proces, som f.eks. at tænde eller slukke for et gen.
Histon lysin demethylaser (KDM'er) tilhører kategorien "viskelædere". Deres specifikke opgave er at fjerne methylgrupper fra en aminosyre kaldet lysin på histon-proteinerne. Ved at fjerne disse mærker kan KDM'er ændre geners aktivitet og dermed have en enorm indflydelse på cellens adfærd.
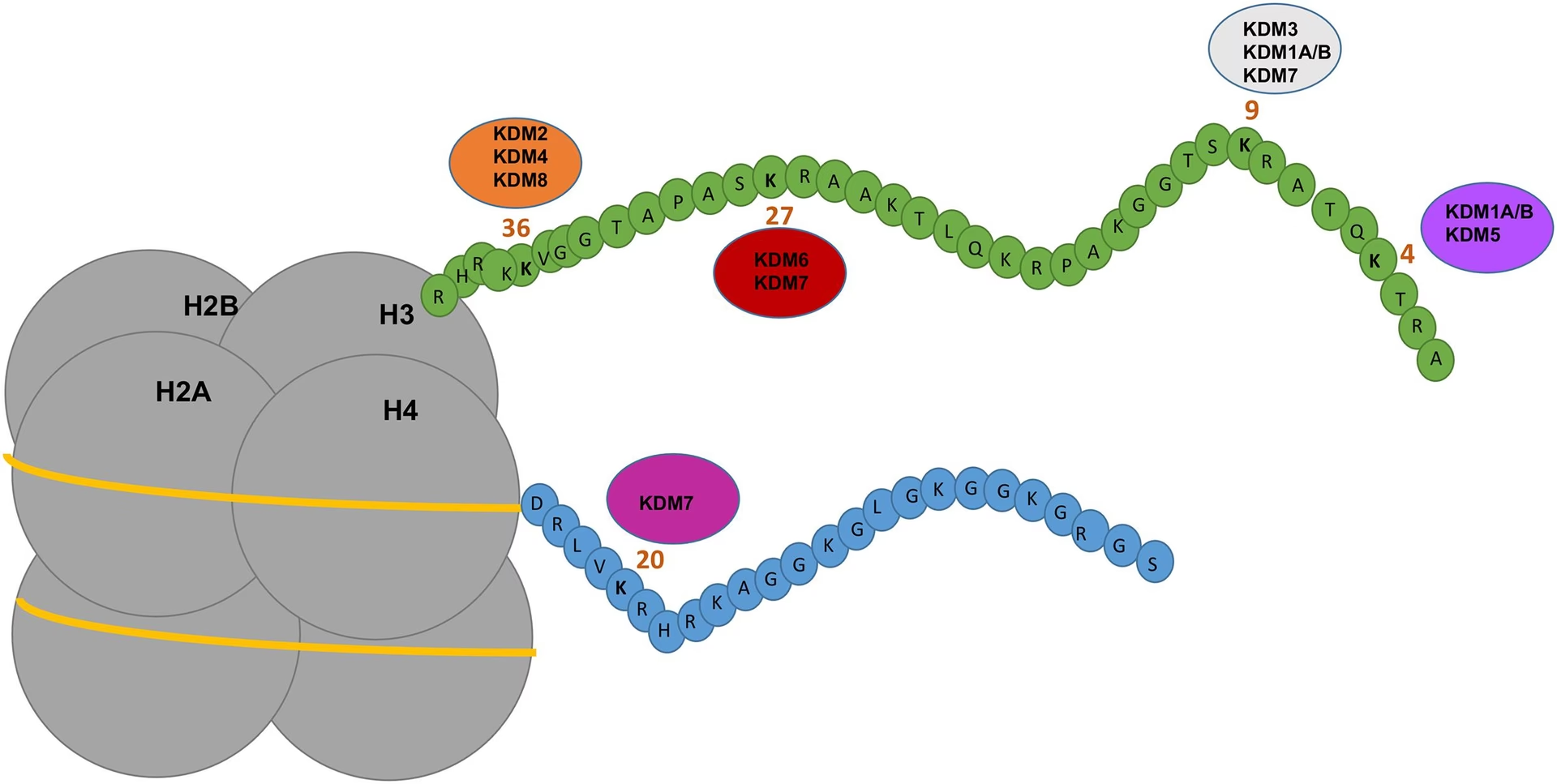
To Familier af KDM'er: Forskellige Værktøjer til Samme Job
KDM-enzymerne er ikke én homogen gruppe. De er opdelt i to hovedklasser, som bruger forskellige kemiske mekanismer til at fjerne methylgrupper.

1. KDM1-familien (LSD1/LSD2)
Den første klasse, der blev opdaget, er KDM1-familien, som også kaldes LSD1 og LSD2. Disse enzymer er afhængige af et co-enzym kaldet FAD (flavin-adenin-dinukleotid). Deres mekanisme kræver, at der er et frit elektronpar på det nitrogenatom, som methylgruppen er bundet til. Det betyder, at de effektivt kan fjerne én (mono-) eller to (di-) methylgrupper fra et lysin-molekyle, men de kan ikke fjerne tre (tri-). Denne begrænsning gør dem specialiserede til bestemte opgaver i cellen.
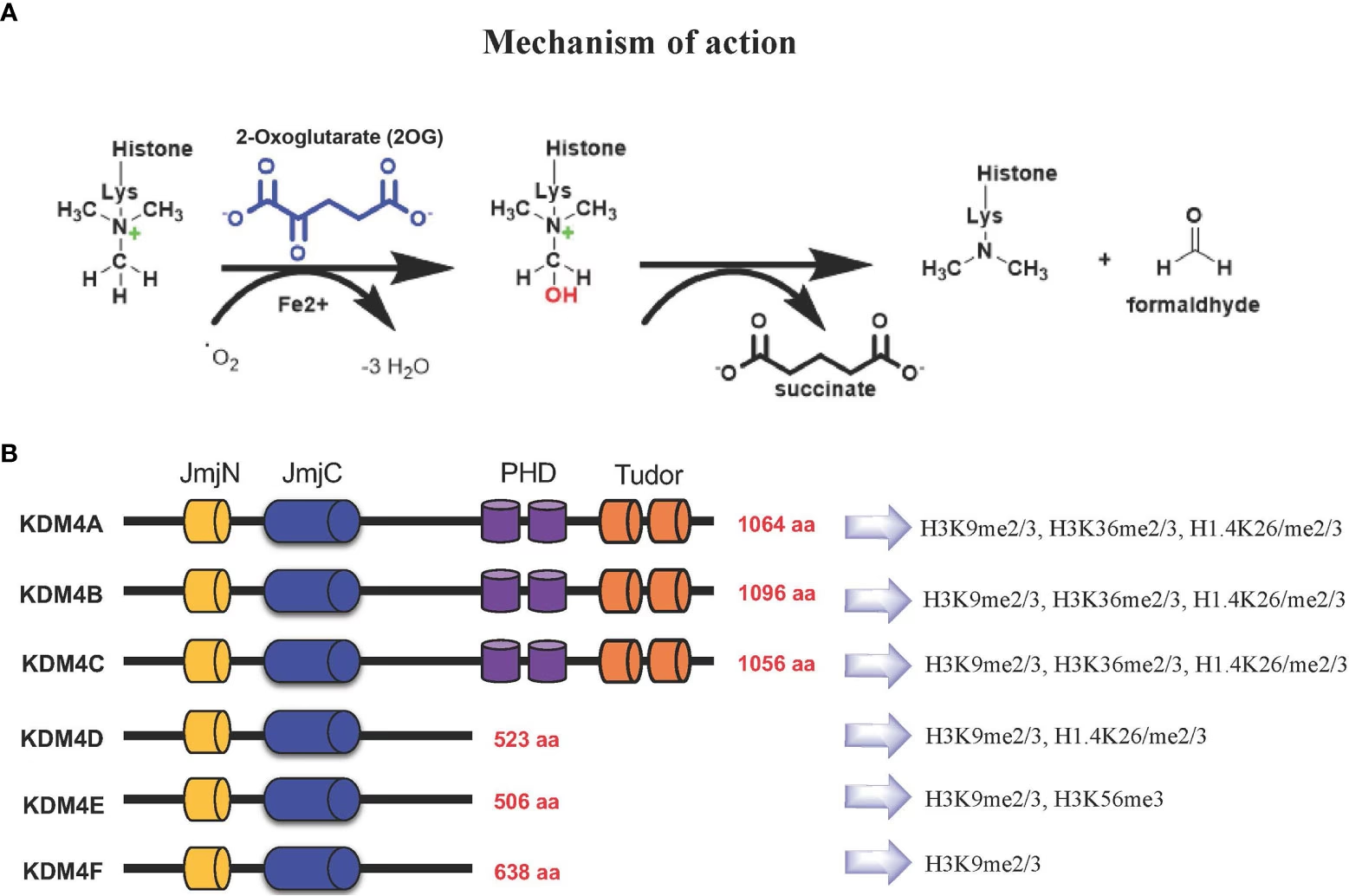
2. JmjC KDM-familien (KDM2-7)
Den anden, og større, klasse er JmjC KDM'erne. Disse enzymer er metalloenzymer, hvilket betyder, at de er afhængige af et metal-ion – i dette tilfælde jern (Fe(II)) – samt et molekyle kaldet α-ketoglutarat for at fungere. Deres mekanisme er anderledes og involverer en oxidation af methylgruppen. Fordi de ikke er afhængige af et frit elektronpar, kan JmjC-enzymerne fjerne alle tre typer af methylering: mono-, di- og trimethyl-lysin. Dette giver dem en bredere vifte af mål og funktioner end KDM1-familien.
Sammenligning af KDM-familier
For at give et klart overblik er her en tabel, der sammenligner de to hovedklasser af KDM'er:
| Egenskab | KDM1-familien (LSD1/2) | JmjC KDM-familien (KDM2-7) |
|---|---|---|
| Mekanisme | Aminoxidase (FAD-afhængig) | Oxygenase (Jern- og α-ketoglutarat-afhængig) |
| Substrater | Fjerner mono- og di-methyl-lysin | Fjerner mono-, di- og tri-methyl-lysin |
| Krav til substrat | Kræver et frit elektronpar på nitrogen | Kræver ikke et frit elektronpar |
| Antal underfamilier | 1 (KDM1) | 6 (KDM2 til KDM7) |
KDM'ernes Rolle i Sygdom – Især Kræft
Når den fine balance i genreguleringen forstyrres, kan det føre til alvorlige sygdomme. Fordi KDM'er er så magtfulde "viskelædere", kan fejl i deres funktion have katastrofale konsekvenser. Forskning har vist, at unormal aktivitet eller mutationer i KDM-gener er tæt forbundet med udviklingen og vedligeholdelsen af kræft.
Når et KDM-enzym er overaktivt, kan det fjerne methylgrupper, der normalt holder kræftfremmende gener (onkogener) slukkede. Resultatet er, at disse gener bliver tændt, hvilket kan føre til ukontrolleret cellevækst. Omvendt, hvis et KDM-enzym, der normalt aktiverer et kræfthæmmende gen (tumor-suppressorgen), er underaktivt, kan det gen forblive slukket, hvilket fjerner en af kroppens vigtige forsvarsmekanismer mod kræft.

KDM'er er blevet impliceret i en lang række kræftformer, herunder:
- Brystkræft (især østrogenreceptor-negativ)
- Prostatakræft
- Ikke-småcellet lungekræft (NSCLC)
- Blærekræft
- Neuroblastom
- Akut myeloid leukæmi (AML)
Denne tætte forbindelse mellem KDM'er og kræft har gjort dem til et yderst attraktivt mål for udvikling af nye lægemidler.
Fremtidens Behandling: Målrettede KDM-hæmmere
Inspireret af succesen med andre epigenetiske lægemidler, såsom HDAC-hæmmere, er der i det seneste årti sket en eksplosion i forskningen inden for KDM-hæmmere. Disse er små molekyler designet til specifikt at blokere aktiviteten af et bestemt KDM-enzym. Ved at hæmme et overaktivt KDM-enzym i en kræftcelle håber man at kunne genoprette den normale epigenetiske balance og dermed stoppe kræftens vækst eller endda dræbe kræftcellerne.
Udviklingen er gået stærkt, og flere KDM-hæmmere er allerede nået til kliniske forsøg på mennesker. Disse lægemidler testes for deres effekt mod forskellige kræftformer, og de første resultater er lovende. Det store potentiale ligger i præcisionsmedicin – altså at man kan skræddersy behandlingen til den enkelte patient. Ved at analysere en patients tumor kan man identificere, hvilke KDM'er der er unormalt aktive, og derefter vælge den KDM-hæmmer, der er mest effektiv mod netop den type kræft.
Dette repræsenterer et skift væk fra traditionel kemoterapi, der rammer alle hurtigt delende celler, mod en mere intelligent og målrettet behandling med færre bivirkninger.
Ofte Stillede Spørgsmål (OSS)
Hvad er en histon lysin demethylase (KDM)?
En KDM er et enzym, der fungerer som et epigenetisk "viskelæder". Dets primære funktion er at fjerne kemiske mærker (methylgrupper) fra histon-proteiner, som DNA er viklet omkring. Denne proces er afgørende for at regulere, hvilke gener der er tændt eller slukket i en celle.
Hvorfor er KDM'er vigtige i forbindelse med kræft?
I kræftceller er KDM-enzymer ofte ude af balance. De kan være overaktive, hvilket tænder for kræftfremmende gener, eller underaktive, hvilket slukker for gener, der normalt beskytter mod kræft. Denne dysregulering er en drivkraft i udviklingen af mange kræftformer.
Findes der allerede medicin, der virker på KDM'er?
Ja, der er udviklet en række lægemiddelkandidater kaldet KDM-hæmmere, som er designet til at blokere disse enzymer. Flere af disse er i øjeblikket i kliniske forsøg, hvor de testes som behandling mod forskellige typer kræft. De er endnu ikke standardbehandling, men repræsenterer en meget lovende ny front inden for kræftmedicin.
Hvad er forskellen på de to hovedtyper af KDM'er?
Den primære forskel ligger i deres virkningsmekanisme og de co-faktorer, de bruger. KDM1-familien (LSD1/2) er FAD-afhængig og kan kun fjerne én eller to methylgrupper. JmjC KDM-familien er jern-afhængig og kan fjerne alle tre grader af methylering (mono-, di- og tri-methyl-lysin), hvilket giver dem en bredere funktionel rækkevidde.
Hvis du vil læse andre artikler, der ligner KDM'er: Nøglen til Genregulering og Kræftbehandling, kan du besøge kategorien Sundhed.