28/08/2013
Malaria, især den dødelige form forårsaget af parasitten Plasmodium falciparum, har været en af de mest potente drivkræfter i menneskets nyere evolution. Sygdommens enorme pres på befolkninger i historisk malaria-ramte områder har efterladt et uudsletteligt aftryk i vores DNA. Mange af de bedst undersøgte beskyttende genetiske varianter påvirker de røde blodlegemer, hvor malariaparasitten tilbringer en kritisk del af sin livscyklus. Blandt disse er mutationer i globin-generne, som koder for hæmoglobin, særligt bemærkelsesværdige. Disse mutationer giver en overlevelsesfordel mod malaria, men denne fordel kommer ofte med en høj pris: risikoen for alvorlige arvelige blodsygdomme, kendt som hæmoglobinopatier. To af de mest kendte eksempler er hæmoglobin S (HbS), årsagen til seglcelleanæmi, og hæmoglobin C (HbC).
Hæmoglobin S (HbS): Et Tveægget Sværd mod Malaria
Hæmoglobin S opstår fra en enkelt punktmutation i beta-globin-genet, hvor aminosyren glutaminsyre erstattes med valin på position 6. Denne lille ændring har dramatiske konsekvenser. Personer, der arver to kopier af denne mutation (genotype SS), lider af seglcelleanæmi, en alvorlig og ofte smertefuld blodsygdom, hvor de røde blodlegemer antager en unormal seglform, hvilket fører til blodpropper, organskader og nedsat levetid.
Paradoksalt nok tilbyder det at arve kun én kopi af mutationen (genotype AS), kendt som seglcelletræk, en betydelig beskyttelse mod alle former for alvorlig malaria. Denne beskyttelse er så markant, at den har drevet frekvensen af HbS-allelen op til 18% i visse dele af Afrika syd for Sahara og Mellemøsten. Forskere har foreslået flere mekanismer for denne beskyttelse:
- Nedsat parasitvækst: Under lav iltspænding, som kan forekomme i de små blodkar, har P. falciparum-parasitten sværere ved at formere sig i røde blodlegemer, der indeholder HbS.
- Ændret proteinvisning: Parasitten ændrer overfladen af det inficerede røde blodlegeme ved at indsætte proteiner som PfEMP-1. I AS-celler menes denne proces at være forstyrret, hvilket reducerer cellens evne til at klæbe til blodkarvæggene (cytoadhærens) og dermed forhindrer de alvorlige komplikationer af malaria.
- Forbedret immunrespons: Der er tegn på, at personer med seglcelletræk hurtigere opnår en effektiv immunitet mod malaria.
Den høje genetiske byrde, som seglcelleanæmi (SS) udgør, skaber en situation med balanceret polymorfi. I malaria-endemiske områder har AS-individer en overlevelsesfordel i forhold til både AA-individer (modtagelige for alvorlig malaria) og SS-individer (lider af seglcelleanæmi). Dette er et klassisk eksempel på heterozygot fordel.
Hæmoglobin C (HbC): En Mildere Fætter med Beskyttende Evner
Ligesom HbS er hæmoglobin C også forårsaget af en mutation på position 6 i beta-globin-kæden, men her erstattes glutaminsyre med lysin. Denne mutation (βC) har også konsekvenser for malariabeskyttelse. En nylig meta-analyse konkluderede, at homozygoter for βC (genotype CC) er stærkt beskyttet mod alvorlig malaria, mens heterozygoter (genotype AC) er mildt beskyttet. Blodsygdommen forbundet med CC-genotypen er desuden relativt mild sammenlignet med den ødelæggende seglcelleanæmi.
Dette fører til et åbenlyst spørgsmål: Hvorfor er HbC, med dens lavere omkostninger, begrænset til specifikke lommer i Vestafrika, mens HbS er udbredt over hele kontinenter? Dette er et centralt genetisk paradoks i studiet af menneskelig evolution.
Det Store Kapløb: Hvorfor HbS Vinder over HbC
Svaret på paradokset ligger i den direkte konkurrence mellem de to alleler, βS og βC. Selvom HbC tilbyder beskyttelse med en mindre ulempe, viser epidemiologiske studier, at beskyttelsen fra seglcelletræk (AS) er markant stærkere end den, der tilbydes af AC-genotypen. Fitnessfordelen kan udtrykkes som: wAS > wAC.
Ydermere fører kombinationen af at arve en βS-allel fra den ene forælder og en βC-allel fra den anden (genotype SC) til en klinisk signifikant blodsygdom, omend mindre alvorlig end SS. Den lave fitness hos SC-individer skaber en stærk selektiv barriere mod, at begge alleler kan have høj frekvens i den samme population. Dette fænomen kaldes konkurrerende udelukkelse.
På grund af den overlegne beskyttelse, som AS-individer nyder, vil βS-allelen simpelthen udkonkurrere βC-allelen, hvis de begge introduceres samtidigt i en befolkning med malaria. Studier i Burkina Faso, hvor begge alleler eksisterer side om side, tyder på, at βC-allelen har været til stede i befolkningen cirka fire gange så længe som βS. Kun ved at have et solidt forspring har HbC formået at opretholde en relativt høj frekvens på trods af den senere invasion af den mere 'aggressive' HbS-allel.

Sammenligning af Hæmoglobin S og Hæmoglobin C
| Egenskab | Hæmoglobin S (HbS) | Hæmoglobin C (HbC) |
|---|---|---|
| Mutation (Beta-globin pos. 6) | Glutaminsyre → Valin | Glutaminsyre → Lysin |
| Beskyttelse (Heterozygot) | Stærk beskyttelse (AS) | Mild beskyttelse (AC) |
| Beskyttelse (Homozygot) | Ikke relevant pga. sygdom | Stærk beskyttelse (CC) |
| Sygdom (Homozygot) | Alvorlig seglcelleanæmi (SS) | Mild hæmolytisk anæmi (CC) |
| Geografisk Udbredelse | Udbredt i Afrika, Mellemøsten, Indien | Primært begrænset til Vestafrika |
En Overraskende Vending: Smitsomhed til Myg
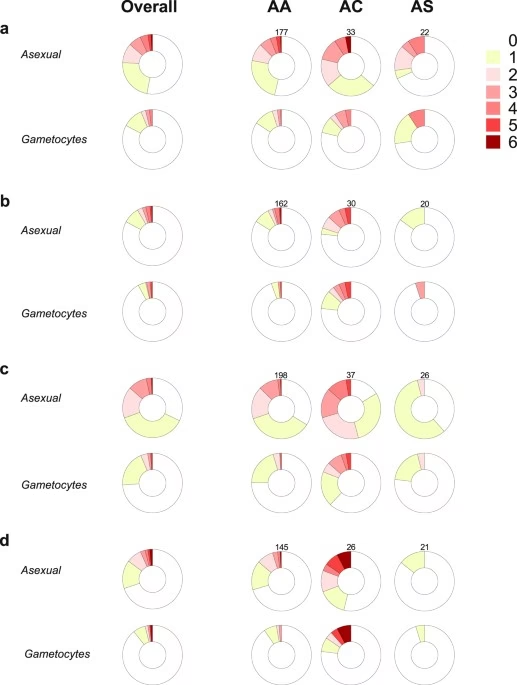
Historien bliver endnu mere kompleks, når vi betragter malariaparasittens livscyklus. For at malaria kan spredes, skal en myg stikke et inficeret menneske og indtage gametocytter – parasittens seksuelle stadie. Nogle studier har antydet, at individer med HbS- eller HbC-træk potentielt kan være mere smitsomme over for myg. Forskning har vist, at AC-individer kan have en højere forekomst af mikroskopisk detekterbare gametocytter, og at AS-bærere kan inficere flere myg end AA-bærere. Dette kunne skabe en feedback-loop: tilstedeværelsen af disse beskyttende gener i en befolkning kan øge den lokale malaria-transmission, hvilket igen øger det selektive pres for selvsamme gener. Denne dynamik illustrerer den utroligt indviklede sameksistens mellem vært, parasit og sygdomsvektor.
Konklusion: Evolution i Aktion
Forholdet mellem hæmoglobin-varianter og malaria er et af de klareste eksempler på menneskelig evolution i aktion. Det demonstrerer, hvordan en enkelt sygdom kan forme vores genetiske landskab og tvinge fremkomsten af træk, der repræsenterer en delikat balanceakt mellem overlevelse og sygdom. Mens HbS tilbyder en stærkere beskyttelse mod malaria, kommer det med den høje omkostning af seglcelleanæmi. HbC er en mildere løsning, men dens svagere beskyttende effekt har betydet, at den er blevet udkonkurreret i det meste af verden. Denne genetiske saga er en stærk påmindelse om, at i biologi er der sjældent simple løsninger, men snarere komplekse kompromiser formet af miljøets ubarmhjertige pres.
Ofte Stillede Spørgsmål (OSS)
Giver seglcelletræk (AS) fuld immunitet mod malaria?
Nej, det giver ikke fuld immunitet. Personer med seglcelletræk kan stadig blive smittet med malaria, men de har en markant lavere risiko for at udvikle den alvorlige, livstruende form af sygdommen.
Er det altid en fordel at have HbS- eller HbC-genet?
Nej, fordelen eksisterer kun i områder, hvor malaria er eller har været udbredt. I regioner uden malaria, som f.eks. Danmark, er der ingen overlevelsesfordel til at opveje risikoen for blodsygdomme. Her vil naturlig selektion arbejde imod disse gener.
Hvorfor er disse mutationer mest almindelige i Afrika og dele af Asien?
Fordi disse er de regioner, hvor Plasmodium falciparum malaria historisk set har haft den største udbredelse og forårsaget den højeste dødelighed. Dette skabte et intenst selektivt pres, der favoriserede individer med beskyttende mutationer som HbS og HbC.
Kan man have både seglcelle- og hæmoglobin C-træk?
Ja, en person kan arve en βS-allel fra den ene forælder og en βC-allel fra den anden, hvilket resulterer i genotypen SC. Denne tilstand, kendt som Hæmoglobin SC-sygdom, er en klinisk signifikant blodsygdom, selvom den typisk er mindre alvorlig end seglcelleanæmi (SS).
Hvis du vil læse andre artikler, der ligner Genetisk Skjold: HbS og Malaria Beskyttelse, kan du besøge kategorien Sundhed.
