30/04/2004
Vores immunsystem er et utroligt komplekst og fintunet netværk af celler og proteiner, der er designet til at beskytte os mod infektioner og sygdomme. En af de mest potente dele af dette forsvar er komplementsystemet, en kaskade af proteiner i blodet, der kan aktiveres for at ødelægge patogener og fremkalde inflammation. Traditionelt har vi kendt til tre hovedveje for aktivering af dette system. Men ny forskning har afsløret en fjerde, mere direkte og potentielt farlig vej, der orkestreres af et enkelt enzym: Granzym K (GZMK). Denne opdagelse ændrer vores forståelse af, hvordan inflammation kan opstå og vedligeholdes i kroppens væv, og åbner døren for nye behandlingsstrategier for en række kroniske sygdomme.
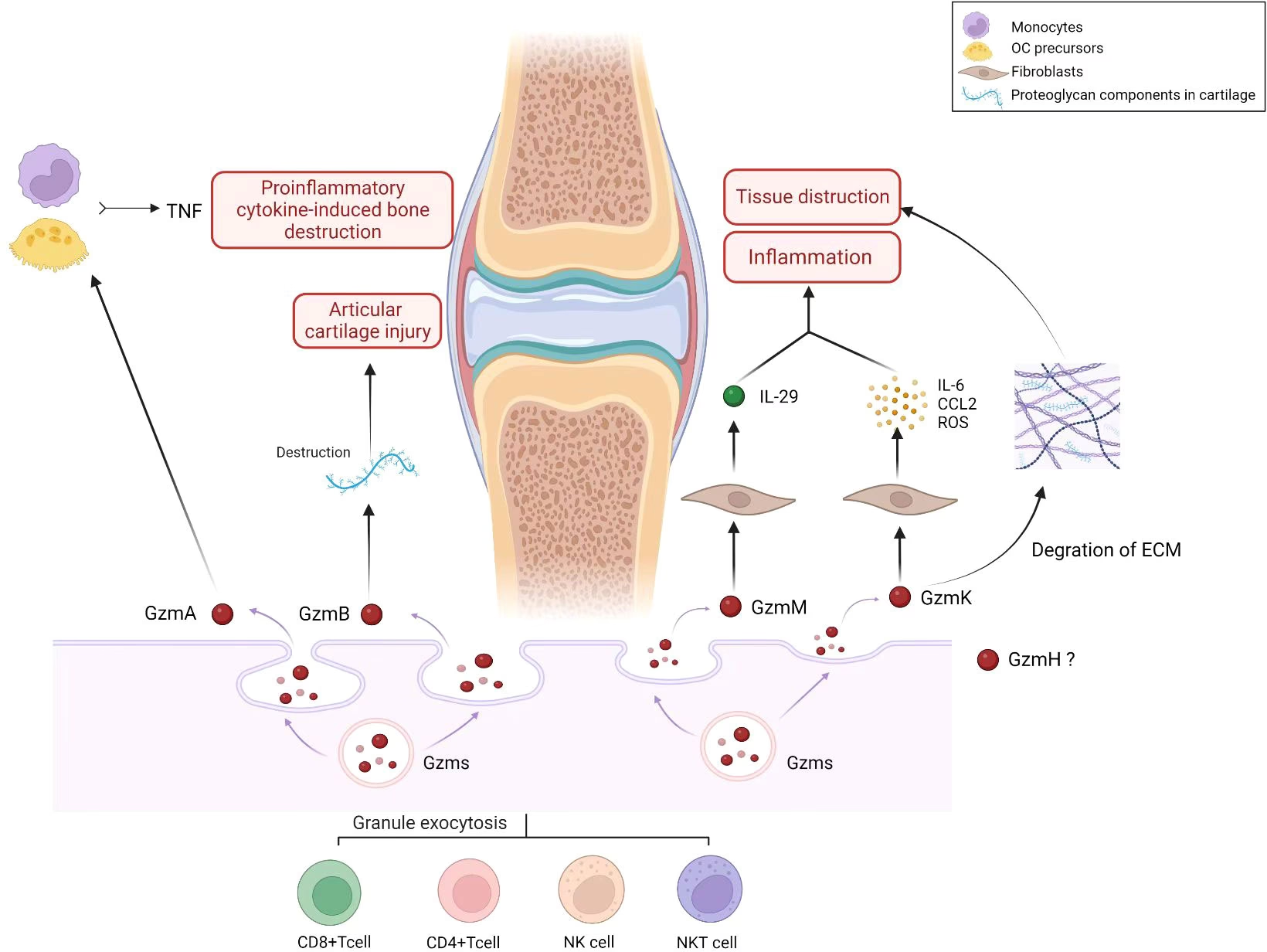
I denne artikel vil vi dykke ned i den fascinerende verden af Granzym K og komplementsystemet. Vi vil udforske, hvordan dette enzym, som frigives af vores egne immunceller, kan kapre en del af vores forsvarssystem og vende det mod os selv, hvilket fører til vedvarende vævsinflammation og skade. Forståelsen af denne mekanisme er ikke kun akademisk interessant; den har dybtgående implikationer for patienter, der lider af autoimmune lidelser, hjerte-kar-sygdomme og andre inflammatoriske tilstande.
Hvad er Granzym K? En dybere introduktion
Granzym K tilhører en familie af enzymer kendt som serinproteaser. Disse enzymer fungerer som molekylære sakse, der klipper andre proteiner på specifikke steder, hvilket enten aktiverer eller deaktiverer dem. GZMK produceres og opbevares primært i specialiserede immunceller, især cytotoksiske T-lymfocytter (også kendt som CD8+ T-celler) og Natural Killer (NK) celler. Disse celler er immunsystemets frontlinjesoldater, hvis primære opgave er at identificere og eliminere virusinficerede celler og kræftceller.
Historisk set har man anset granzymers hovedfunktion for at være at inducere celledød (apoptose) i målceller. Når en T-celle genkender en inficeret celle, frigiver den granzymer, der trænger ind i målcellen og starter en proces, der fører til cellens selvdestruktion. Men nyere forskning har vist, at Granzym K har en bredere rolle. I modsætning til nogle af sine søskendeenzymer, som Granzym B, er GZMK ikke særlig effektiv til at dræbe celler. I stedet ser det ud til at specialisere sig i at fremme inflammation. En vigtig detalje er, at CD8+ T-celler kan frigive GZMK konstant, selv uden direkte stimulering via deres T-celle-receptor, hvilket betyder, at der kan være et vedvarende niveau af dette pro-inflammatoriske enzym i væv, hvor disse T-celler er til stede.
Komplementsystemet: Kroppens dobbeltsidede sværd
Før vi kan forstå Granzym K's unikke rolle, er det nødvendigt at have en grundlæggende forståelse af komplementsystemet. Forestil dig det som en sovende vagthund i dit blod og væv. Når den vækkes af faretegn, reagerer den hurtigt og kraftfuldt. Systemet består af over 30 proteiner, der hovedsageligt produceres i leveren og cirkulerer i en inaktiv form.
Aktivering kan ske via tre anerkendte veje:
- Den klassiske vej: Aktiveres typisk af antistoffer, der har bundet sig til en mikrobe eller et andet mål. Dette er en bro mellem det adaptive og det medfødte immunsystem.
- Lektinvejen: Aktiveres, når et protein kaldet mannose-bindende lektin (MBL) genkender specifikke sukkerstrukturer på overfladen af mikroorganismer.
- Den alternative vej: Er en form for konstant, lav-niveau overvågning, der kan eskalere hurtigt på overflader, der mangler beskyttende proteiner (som findes på vores egne celler, men ikke på mikrober).
Uanset aktiveringsvejen fører de alle til en central begivenhed: kløvningen af komplementproteinet C3. Dette starter en kaskadereaktion, der resulterer i tre primære effekter:
- Inflammation: Små fragmenter (C3a og C5a) fungerer som kraftige signalstoffer, der tiltrækker immunceller til området.
- Opsonisering: Større fragmenter (C3b) dækker målet (f.eks. en bakterie) og gør det 'velsmagende' for fagocyterende celler, der spiser og fjerner det.
- Celledrab: Den ultimative del af kaskaden er dannelsen af det terminale komplementkompleks (TCC), også kendt som Membrane Attack Complex (MAC). Dette kompleks danner en pore i målcellens membran, hvilket fører til dens ødelæggelse.
Den nye mekanisme: Hvordan Granzym K kaprer systemet
Her kommer den revolutionerende opdagelse ind i billedet. Granzym K kan starte sin helt egen aktiveringsvej, der på mange måder ligner den klassiske og lektinvejen, men med en afgørende forskel: den behøver ikke de indledende genkendelsesmolekyler som antistoffer eller MBL.
Processen foregår således:
- Frigivelse og binding: CD8+ T-celler, der befinder sig i et væv, frigiver Granzym K. Enzymet har en naturlig affinitet for bestemte molekyler på celleoverflader kaldet heparansulfat-glykosaminoglykaner (HSGAGs). Det binder sig direkte til cellemembranen i det lokale miljø.
- Initiativet tages: Når GZMK er bundet til celleoverfladen, fungerer det som en initiator-protease. Det klipper direkte komplementproteinerne C4 og C2, som er til stede i vævsvæsken. Dette skaber fragmenterne C4b og C2b.
- Samling af konvertasen: Det nydannede C4b kan binde sig kovalent til cellemembranen lige ved siden af, hvor det blev dannet. Her samles det med C2b for at danne et aktivt enzymkompleks kaldet C3-konvertasen (C4b2b).
- Amplifikation og eksekvering: Denne C3-konvertase gør præcis, hvad navnet antyder: den klipper store mængder af C3-protein til C3a (inflammatorisk signal) og C3b (opsonin og forstærker). Når C3b binder sig til C3-konvertasen, dannes en C5-konvertase, som derefter klipper C5. Dette frigiver det ekstremt potente inflammatoriske signal C5a og starter dannelsen af det celledræbende TCC.
Det smarte og samtidig skræmmende ved denne mekanisme er, at Granzym K kombinerer de to første faser af komplementaktivering – genkendelse og initiering – i ét enkelt molekyle. Det behøver ikke en ekstern fare-sensor; dets evne til at binde sig til almindelige celleoverflader og dets enzymatiske aktivitet er nok til at starte hele den destruktive kaskade.
Sammenligning af aktiveringsveje
For at illustrere forskellene kan vi opstille en tabel, der sammenligner den GZMK-medierede vej med de traditionelle veje. Denne sammenligning understreger, hvor afgørende GZMK's unikke funktion er.
| Egenskab | Klassisk / Lektin Vej | Granzym K Vej |
|---|---|---|
| Genkendelse | Kræver specifikke genkendelsesmolekyler som antistof-komplekser (C1q) eller sukkerstrukturer (MBL) på et mål. | GZMK binder sig direkte til almindeligt forekommende HSGAGs på celleoverflader. Kræver ingen specifik fare-signal. |
| Initiator Protease | Aktiverede proteaser som C1s eller MASP-1/2 kløver C4 og C2. | Granzym K fungerer selv som initiator protease og kløver C4 og C2. |
| Regulering | Stramt reguleret af behovet for et specifikt fare-signal for at starte. | Mindre reguleret; kan potentielt aktiveres overalt, hvor der er GZMK-frigivende T-celler og HSGAGs. |
| Resultat | Effektiv eliminering af patogener og inficerede celler. | Potentielt vedvarende, lokal inflammation og vævsskade i kroniske sygdomme. |
Implikationer for sygdom og fremtidig behandling
Opdagelsen af GZMK-vejen har store konsekvenser. I mange kroniske inflammatoriske sygdomme, såsom leddegigt, aterosklerose (åreforkalkning) og visse nyresygdomme, finder man en ophobning af CD8+ T-celler i det berørte væv. Disse celler frigiver konstant GZMK, hvilket skaber et pro-inflammatorisk miljø. Tidligere har man måske tilskrevet inflammationen andre årsager, men nu ved vi, at GZMK direkte kan tænde for komplementsystemet lige der, hvor skaden sker.
Dette kan skabe en ond cirkel: T-cellerne tiltrækkes af en indledende inflammation, de frigiver GZMK, som aktiverer komplement, hvilket skaber endnu mere inflammation (via C3a og C5a), som tiltrækker flere immunceller, inklusiv flere T-celler. Denne selvforstærkende cyklus kan være en central drivkraft bag den kroniske vævsnedbrydning, man ser i disse sygdomme.
Den gode nyhed er, at en ny forståelse også åbner for nye behandlingsmuligheder. Hvis GZMK er en central aktør, kan man udvikle lægemidler, der specifikt hæmmer dette enzym. En sådan behandling ville teoretisk set kunne dæmpe den komplement-drevne inflammation lokalt i vævet uden at slukke for hele komplementsystemet i resten af kroppen, hvilket ville bevare patientens evne til at bekæmpe infektioner. Forskning i GZMK-inhibitorer er allerede i gang og repræsenterer et spændende nyt håb for patienter med kroniske inflammatoriske lidelser.
Ofte Stillede Spørgsmål (FAQ)
- Er inflammation altid en dårlig ting?
- Nej, absolut ikke. Akut inflammation er en essentiel og sund reaktion på skade eller infektion. Det er kroppens måde at fjerne truslen og starte helingsprocessen. Problemet opstår, når inflammationen bliver kronisk – det vil sige, at den ikke slukker igen, men fortsætter med at 'simre' i vævet, hvilket fører til gradvis skade.
- Hvorfor har kroppen en så farlig mekanisme som GZMK-vejen?
- Det er sandsynligt, at denne vej har en nyttig funktion under visse omstændigheder, f.eks. til hurtigt at skabe et stærkt inflammatorisk respons mod visse vira eller kræftceller. Som med mange biologiske systemer er det balancen, der er afgørende. I en sund krop holdes mekanismen i skak, men i sygdomstilstande kan den komme ud af kontrol.
- Er dette en helt ny opdagelse inden for immunologi?
- Mens Granzym K har været kendt i et stykke tid, er dets specifikke rolle som en direkte, uafhængig aktivator af komplementsystemet en relativt ny og banebrydende opdagelse. Det tilføjer et helt nyt kapitel til lærebøgerne om immunologi og inflammation.
- Kan jeg blive testet for høje niveauer af Granzym K?
- Måling af Granzym K udføres primært i forskningssammenhænge. Det er endnu ikke en standard klinisk test, som en læge vil bestille. Relevansen ligger ofte i koncentrationen af GZMK lokalt i vævet, hvilket er svært at måle, frem for i en blodprøve.
- Hvad er den vigtigste 'take-home message' om Granzym K?
- Den vigtigste pointe er, at vores egne immunceller kan frigive et enzym, der kortslutter en af de mest potente dele af vores immunsystem, komplementsystemet. Dette skaber en direkte vej til inflammation, som kan drive kronisk sygdom, og det repræsenterer et spændende nyt mål for fremtidens medicin.
Hvis du vil læse andre artikler, der ligner Granzym K: Nøglen til vævsinflammation, kan du besøge kategorien Sundhed.
