04/11/2024
God Fremstillingspraksis, bedre kendt under forkortelsen GMP (Good Manufacturing Practice), er et afgørende regelsæt og system, der anvendes i industrier som medicinal-, fødevare-, kosmetik- og medicinsk udstyrsindustrien. Formålet med GMP er at sikre, at produkter konsekvent produceres og kontrolleres i henhold til strenge kvalitetsstandarder. Dette minimerer de risici, der er forbundet med enhver produktion, som ikke kan elimineres fuldstændigt gennem testning af det endelige produkt. GMP dækker alle aspekter af produktionen, fra startmaterialer, lokaler og udstyr til personalets uddannelse og personlige hygiejne. Ved at implementere GMP beskytter virksomheder ikke kun forbrugerne mod skadelige eller ineffektive produkter, men sikrer også overholdelse af lovgivningen og opbygger et stærkt omdømme for kvalitet og pålidelighed.
Hvad er Forskellen på GMP og cGMP?
Du er måske stødt på både termen GMP og cGMP og undret dig over forskellen. I de fleste tilfælde kan de bruges i flæng, men det lille 'c' i cGMP har en vigtig betydning. 'c' står for 'current' (aktuel), hvilket understreger, at praksis skal være opdateret med de nyeste teknologier, systemer og videnskabelige fremskridt. Den amerikanske fødevare- og lægemiddelmyndighed (FDA) implementerede cGMP for at fremme en kultur af kontinuerlig forbedring hos producenterne. Mens GMP udgør de grundlæggende regler, indebærer cGMP en forpligtelse til konstant at stræbe efter de højest tilgængelige kvalitetsstandarder. Det betyder, at en proces eller et system, der var acceptabelt for ti år siden, måske ikke længere lever op til nutidens cGMP-krav, hvis mere moderne og pålidelige metoder er blevet tilgængelige. I praksis forventer de fleste regulerende myndigheder, herunder Det Europæiske Lægemiddelagentur (EMA), at virksomheder følger en aktuel og moderne tilgang, selvom de ikke eksplicit bruger termen 'cGMP'.
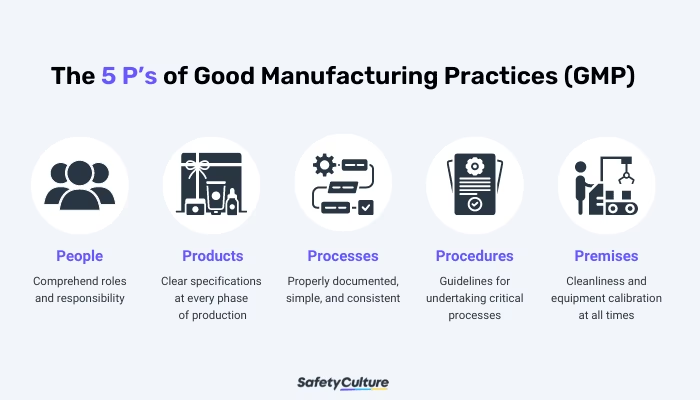
De 5 Kernekomponenter i GMP: De 5 P'er
For at gøre de komplekse GMP-retningslinjer mere håndgribelige, opsummeres de ofte i fem kernekomponenter, kendt som de 5 P'er. Disse elementer hjælper organisationer med at overholde de strenge standarder gennem hele produktionsprocessen.
1. Mennesker (People)
Mennesker er kernen i enhver produktionsproces. Ifølge GMP skal alle medarbejdere være kvalificerede og have den nødvendige uddannelse til at udføre deres opgaver korrekt. Dette inkluderer grundig træning i GMP-principper, specifikke arbejdsinstruktioner og hygiejneprocedurer. Deres roller og ansvarsområder skal være klart definerede og dokumenterede. Regelmæssig vurdering af deres præstationer og løbende efteruddannelse er afgørende for at opretholde kompetenceniveauet og sikre, at de strengt overholder alle processer og regler.

2. Produkter (Products)
Alle produkter og de materialer, der indgår i dem, skal opfylde specificerede kvalitetskrav. Dette starter med råmaterialerne, som skal testes og godkendes, inden de tages i brug. Gennem hele produktionsprocessen skal der udføres konstante tests og kvalitetssikring for at sikre, at produktet lever op til specifikationerne i hver fase. Før et færdigt produkt frigives til forbrugerne, skal det gennemgå en endelig kvalitetskontrol. Standardiserede metoder for pakning, testning og prøveudtagning skal følges nøje.
3. Processer (Processes)
Alle processer, der er involveret i fremstillingen, skal være klart definerede, validerede og konsekvent fulgt. En valideret proces er en proces, hvor der er dokumenteret bevis for, at den konsekvent vil producere et produkt, der opfylder sine forudbestemte specifikationer og kvalitetsattributter. Processerne skal være tydeligt dokumenterede og tilgængelige for alle relevante medarbejdere. Enhver afvigelse fra de etablerede processer skal undersøges og dokumenteres for at forhindre gentagelser og sikre produktkvaliteten.
4. Procedurer (Procedures)
En procedure, ofte kaldet en Standard Operating Procedure (SOP), er en detaljeret, skriftlig instruktion om, hvordan man udfører en specifik opgave. GMP kræver, at der findes SOP'er for alle kritiske processer for at sikre ensartethed og reproducerbarhed. Alle medarbejdere skal trænes i og følge disse procedurer nøjagtigt. Enhver afvigelse fra en standardprocedure skal øjeblikkeligt rapporteres, undersøges og dokumenteres. Dette sikrer, at alle opgaver udføres på samme måde hver gang, uanset hvem der udfører dem.
5. Præmisser (Premises)
Produktionsfaciliteterne, eller præmisserne, skal være designet, konstrueret og vedligeholdt på en måde, der minimerer risikoen for fejl og forurening. Dette indebærer en logisk indretning, der forhindrer krydskontaminering mellem forskellige materialer og produkter. Renlighed er altafgørende, og der skal være faste procedurer for rengøring og sanitet. Alt udstyr skal være korrekt placeret, opbevaret og regelmæssigt kalibreret for at sikre, at det fungerer efter hensigten og leverer konsistente resultater. Udstyrets vedligeholdelse skal dokumenteres for at forhindre udstyrsfejl, der kan påvirke produktkvaliteten.

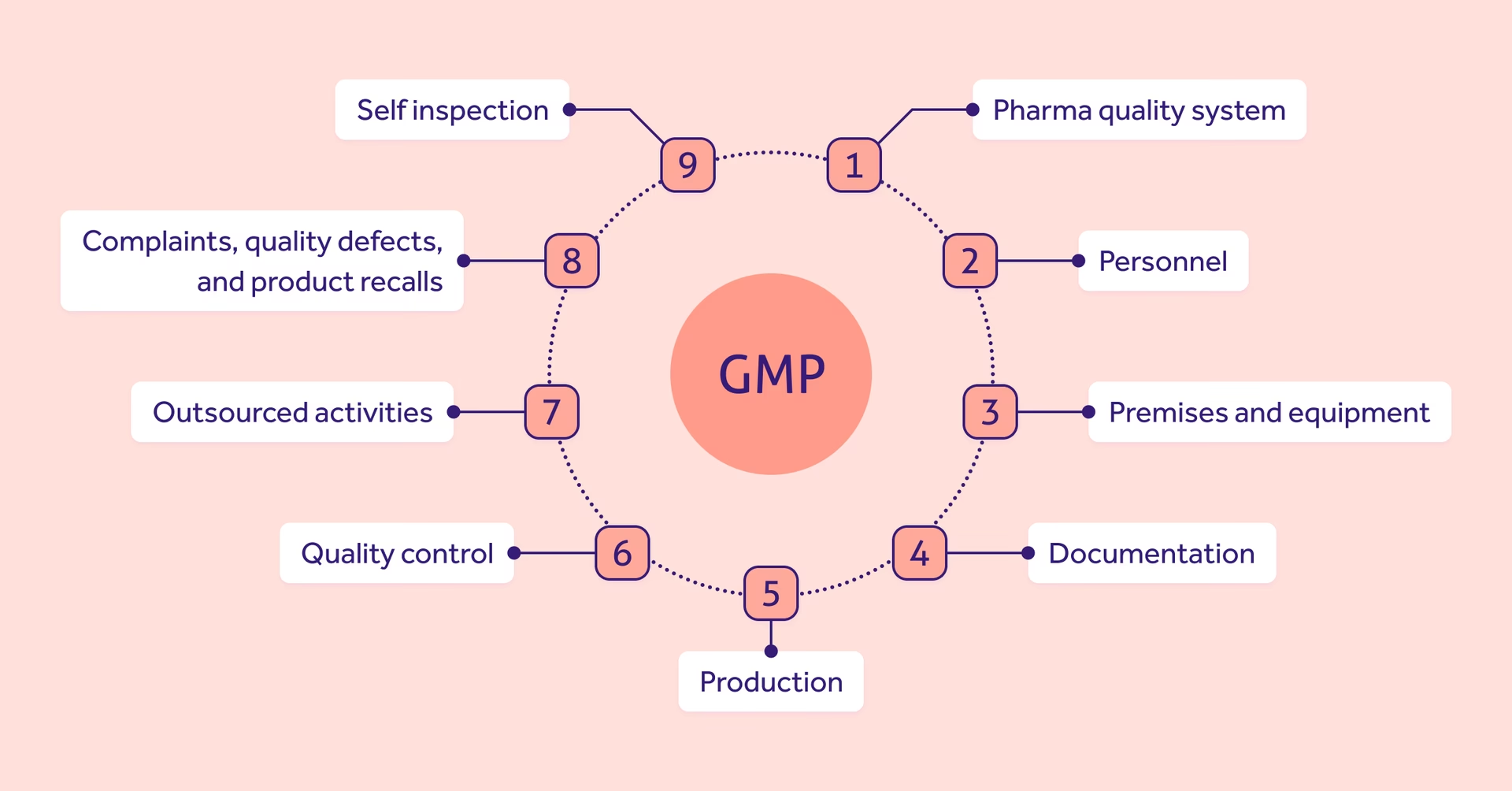
De 10 Grundlæggende Principper for GMP
Ud over de 5 P'er kan GMP-filosofien koges ned til 10 grundlæggende principper, som fungerer som en praktisk guide for enhver produktionsvirksomhed:
- Opret Standardiserede Driftsprocedurer (SOP'er): Udvikl klare, trinvise skriftlige instruktioner for alle kritiske opgaver.
- Håndhæv og Implementer SOP'er og Arbejdsinstruktioner: Sørg for, at alle medarbejdere konsekvent følger de godkendte procedurer.
- Dokumenter Procedurer og Processer: Alt, hvad der gøres, skal dokumenteres i realtid. God dokumentation er beviset på overholdelse.
- Valider Effektiviteten af SOP'er: Bevis, at dine processer og procedurer rent faktisk virker og konsekvent producerer det ønskede resultat.
- Design og Anvend Funktionelle Systemer: Design faciliteter og udstyr for at forhindre fejl, forvekslinger og forurening.
- Vedligehold Systemer, Faciliteter og Udstyr: Sørg for regelmæssig vedligeholdelse og kalibrering for at holde alt i en valideret og kontrolleret tilstand.
- Udvikl Medarbejdernes Jobkompetence: Invester i grundig og løbende træning for at sikre, at personalet er kompetent til deres opgaver.
- Forebyg Kontaminering Gennem Renlighed: Implementer strenge hygiejne- og rengøringsprogrammer for både personale og faciliteter.
- Prioriter Kvalitet og Integrer Det i Arbejdsgangen: Gør kvalitet til en integreret del af alle operationer, ikke blot en eftertanke eller en separat afdelings ansvar.
- Gennemfør GMP-audits Regelmæssigt: Udfør både interne og eksterne audits for at vurdere overholdelse og identificere områder til forbedring.
GMP-reguleringer Verden Over
GMP-krav er lovpligtige og håndhæves af nationale regulerende myndigheder. Selvom de grundlæggende principper er de samme globalt, kan de specifikke regler variere fra region til region. Nedenstående tabel giver et overblik over de vigtigste myndigheder og deres regelsæt.
| Region | Regulerende Myndighed | Vigtigste Regulering/Retningslinje |
|---|---|---|
| USA | Food and Drug Administration (FDA) | Current Good Manufacturing Practices (cGMP) under 21 CFR Parts 210, 211 (lægemidler), 820 (medicinsk udstyr) |
| Europa | European Medicines Agency (EMA) & Nationale Myndigheder | EudraLex Volume 4 - EU Guidelines for Good Manufacturing Practice for Medicinal Products for Human and Veterinary Use |
| Internationalt | World Health Organization (WHO) | WHO Good Manufacturing Practices (bruges ofte som grundlag for nationale regler i mange lande) |
Disse myndigheder udfører inspektioner af produktionsfaciliteter for at vurdere, om en virksomhed overholder de gældende GMP-regler. Hvis der findes alvorlige overtrædelser, kan myndighederne pålægge sanktioner, såsom tilbagekaldelse af produkter, bøder eller endda inddragelse af produktionstilladelsen, hvilket kan have katastrofale konsekvenser for en virksomhed.
Ofte Stillede Spørgsmål (FAQ)
Hvad står GMP for i produktion?
GMP står for God Fremstillingspraksis (Good Manufacturing Practice). Det er et lovpligtigt kvalitetssikringssystem, der sikrer, at produkter som lægemidler, fødevarer og medicinsk udstyr konsekvent produceres og kontrolleres i henhold til fastsatte kvalitetsstandarder. Formålet er at beskytte folkesundheden ved at minimere risici som forurening, forvekslinger og fejl i produktionsprocessen.
Hvem er omfattet af GMP-retningslinjerne?
GMP-retningslinjerne dækker alle virksomheder, der er involveret i fremstilling, forarbejdning, pakning eller opbevaring af produkter inden for regulerede industrier. Dette inkluderer producenter af lægemidler, aktive farmaceutiske ingredienser (API'er), medicinsk udstyr, visse fødevarer, kosttilskud og kosmetik. Reglerne gælder for hele produktionskæden, fra modtagelse af råmaterialer til distribution af det færdige produkt.
Hvorfor er kvalitet så vigtigt i GMP?
Kvalitet er kernen i GMP, fordi svigt i produktkvaliteten kan have direkte og alvorlige konsekvenser for forbrugernes helbred og sikkerhed. I modsætning til mange andre produkter kan fejl i f.eks. et lægemiddel være livstruende. GMP sikrer kvalitet ved at bygge den ind i selve produktionsprocessen gennem kontrol, validering og dokumentation, i stedet for kun at forlade sig på test af det endelige produkt. Dette skaber tillid hos forbrugere og myndigheder og er en forudsætning for at få adgang til markedet.
Udsteder FDA GMP-certifikater?
Nej, den amerikanske FDA udsteder ikke formelle GMP-certifikater. I stedet udfører de inspektioner af faciliteter. Efter en vellykket inspektion anses virksomheden for at være i overensstemmelse med cGMP. I modsætning hertil udsteder de kompetente myndigheder i EU-lande et GMP-certifikat efter en vellykket inspektion. Disse certifikater er offentligt tilgængelige i EudraGMDP-databasen og er ofte en forudsætning for handel inden for EU.
Hvis du vil læse andre artikler, der ligner God Fremstillingspraksis (GMP) Forklaret, kan du besøge kategorien Sundhed.
