29/03/2021
Hjernen er et af de mest komplekse organer i den kendte verden, bestående af milliarder af neuroner forbundet i et indviklet netværk. At forstå dette netværks 'ledningsdiagram' er en af de største udfordringer inden for moderne neurovidenskab. For at tackle denne udfordring har forskere udviklet innovative værktøjer, og et af de mest kraftfulde er en genetisk modificeret version af rabiesvirussen. Specifikt er den G-slettede rabiesvirusvektor blevet en game-changer, der giver forskere mulighed for at spore neuronale forbindelser med hidtil uset præcision og sikkerhed.
Hvad er en Rabiesvirus Vektor?
Rabiesvirus har en unik og for forskere meget interessant egenskab: den er neurotrop, hvilket betyder, at den selektivt inficerer nerveceller (neuroner). Ikke nok med det, den spreder sig også mellem synaptisk forbundne neuroner i en udelukkende retrograd retning. Det betyder, at den bevæger sig 'baglæns' fra en postsynaptisk neuron til en præsynaptisk neuron – altså fra den neuron, der modtager et signal, til den neuron, der sendte det. Denne naturlige evne gør den til en ideel kandidat som et sporingsværktøj til at kortlægge neuronale kredsløb.
I sin vilde form er rabiesvirus dog farlig og dens spredning er ukontrolleret. Når den først inficerer en neuron, vil den fortsætte med at replikere og sprede sig til alle forbundne neuroner, og derefter til deres forbundne neuroner, og så videre. Dette skaber et kaotisk billede, der gør det umuligt at identificere specifikke, direkte forbindelser. Desuden er den høje grad af viral replikation giftig for neuronerne, hvilket hurtigt dræber dem og forhindrer langsigtet undersøgelse.
Glykoprotein (G): Virussens Nøgle
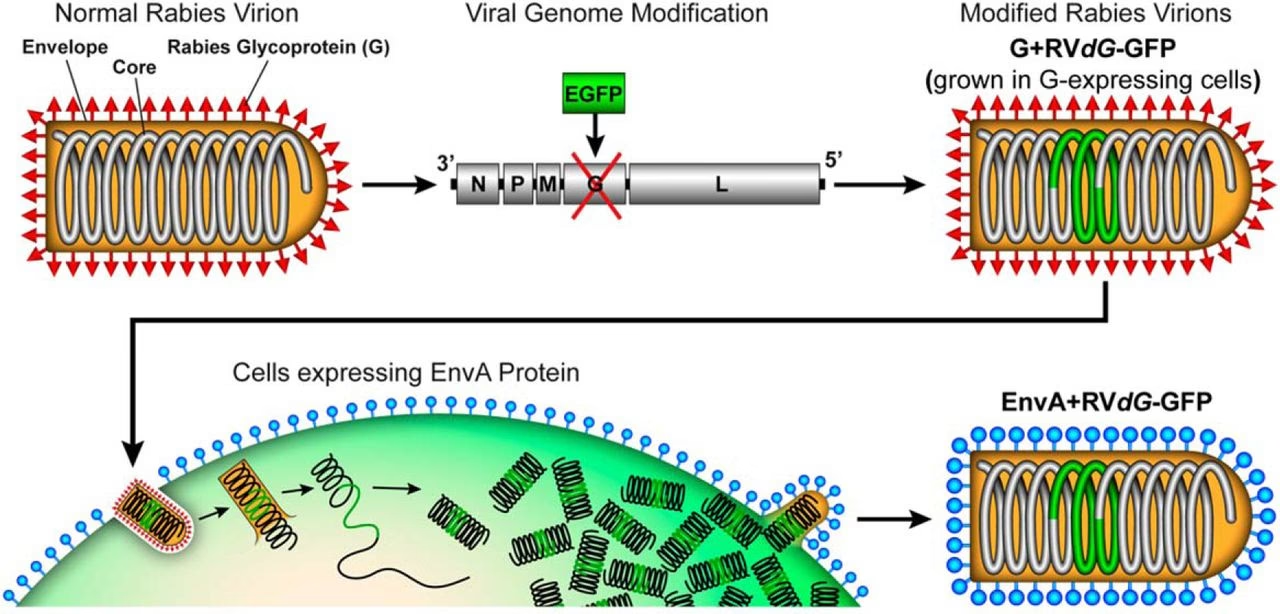
For at forstå, hvordan forskere tæmmede rabiesvirussen, må vi se på dens anatomi. På overfladen af rabiesviruspartiklen sidder der spidse proteiner kaldet glykoprotein, eller blot 'G'. Dette glykoprotein fungerer som virussens nøgle. Det er G-proteinet, der binder sig til specifikke receptorer på overfladen af en neuron, hvilket giver virussen mulighed for at trænge ind i cellen. G-proteinet er også afgørende for, at nye viruspartikler, der produceres inde i en inficeret celle, kan spire ud og efterfølgende inficere den næste neuron i kæden. Uden G-proteinet er virussen i det væsentlige låst fast og kan ikke sprede sig.
Revolutionen: Den G-slettede (ΔG) Vektor
Gennembruddet kom, da forskere indså, at de kunne fjerne genet, der koder for G-proteinet, fra virussens genom. Resultatet er en G-slettet rabiesvirusvektor (ofte skrevet som ΔG-RV). Denne modificerede virus har mistet sin evne til at sprede sig trans-synaptisk.
Dette åbner op for en utrolig grad af kontrol. Forskere kan nu udføre det, der kaldes monosynaptisk sporing, hvor de kun kortlægger de neuroner, der er direkte forbundet til en specifik startpopulation af neuroner. Processen fungerer typisk sådan her:
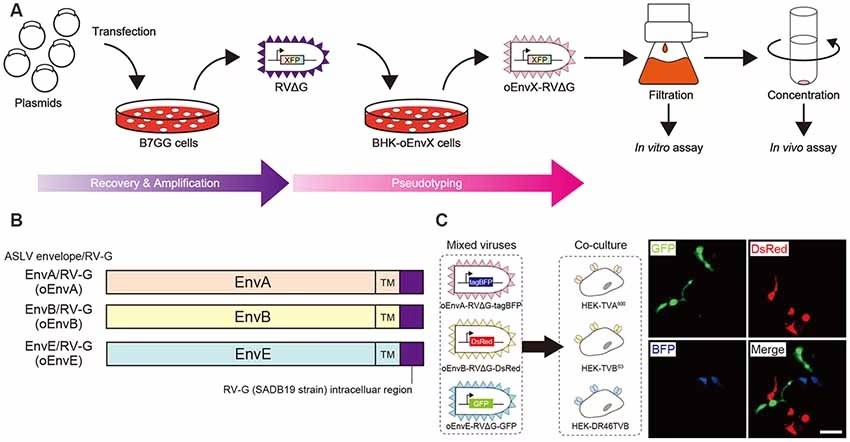
- Målrettet infektion: Først inficeres en specifik, genetisk defineret gruppe af neuroner (starter-celler) med den G-slettede virus. Dette gøres ofte ved hjælp af en 'pseudotyping'-teknik, hvor virussen midlertidigt udstyres med et andet overfladeprotein (f.eks. EnvA), som kun kan binde sig til en receptor (f.eks. TVA), som forskerne kunstigt har placeret på netop deres ønskede starter-celler.
- Tilførsel af G-protein 'in trans': Samtidig sørger forskerne for, at kun disse starter-celler også udtrykker G-proteinet. Dette gøres ved at levere G-genet separat, så det ikke er en del af rabiesvirusgenomet.
- Kontrolleret et-trins spredning: Inde i starter-cellen replikerer den G-slettede virus sig. De nye viruspartikler 'låner' nu det G-protein, som cellen producerer, og bygger det ind i deres egen overflade. Nu er disse nye viruspartikler i stand til at foretage ét enkelt spring – de bevæger sig retrogradt og inficerer alle de neuroner, der sender signaler direkte til starter-cellerne.
- Stop for spredning: Når virussen ankommer til disse 'første-ordens' neuroner, kan den igen replikere sig. Men fordi disse neuroner ikke har fået tilført G-genet, kan de nye viruspartikler ikke producere G-proteinet. De er 'nøgne' og kan derfor ikke sprede sig yderligere. Spredningen stopper efter ét enkelt synaptisk spring.
For at visualisere de inficerede neuroner, bærer virussen typisk også et gen for et fluorescerende protein, såsom mRFP (monomerisk rødt fluorescerende protein). Dette får alle de inficerede neuroner til at lyse op i en klar farve under et mikroskop, hvilket skaber et smukt og præcist kort over kredsløbet.
Uventede, men Markante Fordele
Da forskere udviklede den G-slettede vektor, opdagede de to yderligere, markante fordele, som har forbedret dens anvendelighed betydeligt.

1. Markant Lavere Cytotoksicitet
Studier har vist, at rabies G-proteinet i sig selv er en væsentlig årsag til den celleskade og celledød (apoptose), som ses i inficerede neuroner. Ved at fjerne G-genet er den nye virusvektor blevet meget mindre giftig for cellerne. Forskning har vist, at neuroner inficeret med en G-slettet vektor kan overleve og bevare deres normale elektrofysiologiske egenskaber i ugevis (over 16 dage i nogle studier), sammenlignet med få dage for den G-kompetente virus. Denne lave cytotoksicitet er afgørende for at kunne studere funktionelle aspekter af de kortlagte kredsløb over tid.
2. Højere Transgen-Ekspression
Overraskende nok førte fjernelsen af G-genet også til et meget højere udtryk af det medfølgende transgen (f.eks. det fluorescerende protein). Neuroner inficeret med den G-slettede vektor lyser meget kraftigere og hurtigere op. Inden for blot 3 dage kan fine detaljer som dendritiske spines og axoner visualiseres tydeligt uden behov for yderligere farvning. Dette skyldes sandsynligvis en kombination af den lavere celletoksicitet, som tillader cellens maskineri at fungere bedre, og mulige ændringer i, hvordan virussens eget polymerase-gen (L) udtrykkes.
Sammenligning af Rabiesvirus Vektorer
Nedenstående tabel opsummerer de vigtigste forskelle mellem en traditionel, formeringsdygtig rabiesvirusvektor og den moderne G-slettede vektor.
| Egenskab | Formeringdygtig RV Vektor (med G) | G-slettet RV Vektor (ΔG) |
|---|---|---|
| Spredning | Ukontrolleret, poly-synaptisk | Ingen spredning (kan gøres monosynaptisk) |
| Kontrol | Meget lav | Meget høj, tillader præcis sporing |
| Cytotoksicitet | Høj, forårsager hurtig celledød | Lav, neuroner overlever i ugevis |
| Transgen-ekspression | Moderat | Meget høj, giver et stærkt og klart signal |
Ofte Stillede Spørgsmål (FAQ)
Er denne modificerede virus farlig?
Den G-slettede rabiesvirus er baseret på svækkede (attenuerede) laboratoriestammer. Fordi den mangler G-proteinet, kan den ikke sprede sig fra celle til celle eller fra dyr til menneske. Alle eksperimenter udføres under strenge biosikkerhedsprotokoller (typisk Biosafety Level 2) for at sikre fuld sikkerhed for forskerne.
Hvorfor bruge rabiesvirus og ikke en anden virus som AAV?
Mens andre vira som AAV (Adeno-associeret virus) er fremragende til at levere gener til neuroner, har de generelt ikke den naturlige evne til at krydse synapser på en effektiv og retningsbestemt måde. Rabiesvirussens unikke evne til effektiv retrograd trans-synaptisk transport gør den uovertruffen til netop kredsløbssporing.
Hvad kan man bruge denne teknik til?
Teknikken bruges til at besvare fundamentale spørgsmål om hjernen. For eksempel har forskere brugt den til at identificere alle de input, som specifikke celletyper, som dopamin-neuroner, modtager fra hele hjernen. Man har også brugt den til at studere, hvordan nyfødte neuroner i den voksne hjerne gradvist integreres i de eksisterende kredsløb over tid. Det er et værktøj, der lægger fundamentet for at forstå alt fra sanseopfattelse til beslutningstagning.
Hvis du vil læse andre artikler, der ligner G-slettet Rabiesvirus: Et Værktøj til Hjernen, kan du besøge kategorien Sundhed.