30/08/2020
Granulocyt-kolonistimulerende faktor, bedre kendt som G-CSF, er et molekyle med to vidt forskellige ansigter inden for kræftbehandling. For mange patienter, der gennemgår kemoterapi, er det en afgørende livline, der beskytter mod farlige infektioner ved at styrke immunforsvaret. Samtidig afslører en voksende mængde forskning en mere ildevarslende side af G-CSF: Dets potentiale til at nære og fremme selve den kræft, man forsøger at bekæmpe. Denne dualitet placerer G-CSF i centrum for en intens videnskabelig debat og skubber forskere til at afdække, hvordan man kan udnytte dets fordele uden at falde i dets fælder.
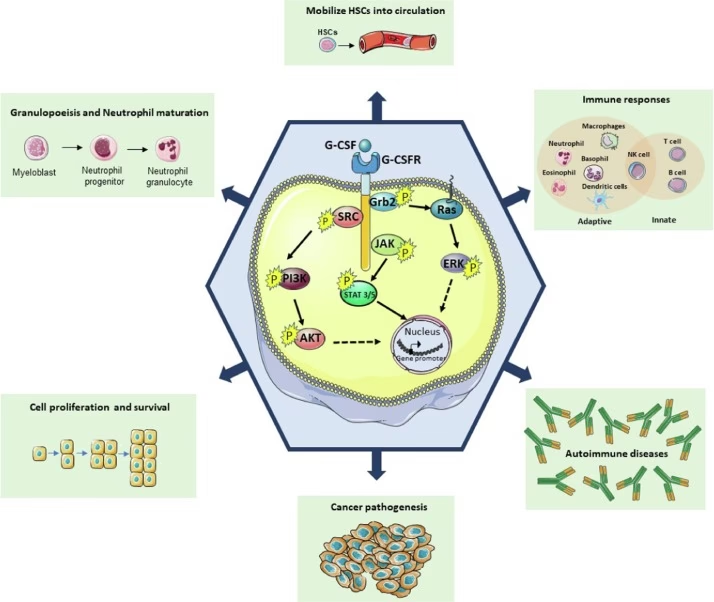
Hvad er G-CSF (Granulocyt-kolonistimulerende faktor)?
G-CSF er et cytokin, en type protein, der fungerer som en signalstof i kroppen. Dets primære og mest kendte funktion er at stimulere knoglemarven til at producere og frigive flere neutrofile granulocytter, en afgørende type hvide blodlegemer, der er kroppens frontlinjesoldater mod bakterielle infektioner. Når kroppen udsættes for en infektion, øges produktionen af G-CSF naturligt for at mobilisere immunforsvaret.
Denne evne til at booste antallet af neutrofiler har gjort syntetiske versioner af G-CSF (såsom filgrastim og pegfilgrastim) til et standardværktøj i onkologien. Mange former for kemoterapi er myelosuppressive, hvilket betyder, at de undertrykker knoglemarvens funktion og fører til en farlig mangel på hvide blodlegemer – en tilstand kaldet neutropeni. Ved at administrere G-CSF kan læger forebygge eller behandle alvorlig neutropeni, hvilket reducerer risikoen for livstruende infektioner og sikrer, at patienterne kan fortsætte deres planlagte kemoterapiforløb.
Den Tveæggede Sværd: G-CSF's Rolle i Kræft
Mens den terapeutiske brug af G-CSF er uomtvistelig, bliver billedet mere kompliceret, når man ser på, hvordan G-CSF interagerer med selve kræftsvulsten. Problemet opstår, fordi nogle kræftceller har lært at udnytte dette kraftfulde signalstof til deres egen fordel.
Den Mørke Side: Når Kræftceller Producerer og Reagerer på G-CSF
Forskning har vist, at en række forskellige kræftformer selv kan producere høje niveauer af G-CSF. Dette gælder blandt andet for tumorer i tyktarmen, brystet, bugspytkirtlen, blæren, lungerne og leveren. Når en tumor udskiller G-CSF, er det ofte et tegn på en mere aggressiv sygdom. Kliniske rapporter tyder på, at patienter med G-CSF-producerende tumorer har en dårligere prognose, øget risiko for spredning (metastase) og højere dødelighed.
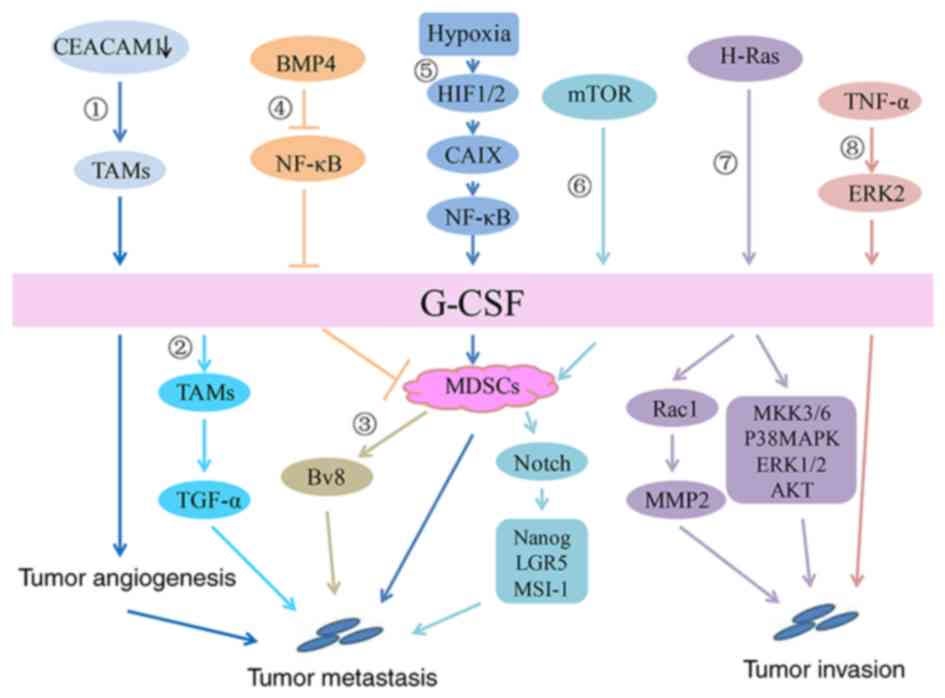
Problemet er ikke kun, at tumoren producerer G-CSF, men også at kræftcellerne i nogle tilfælde selv har receptorer for det (G-CSFR). Dette skaber en ond cirkel, kendt som en autokrin eller parakrin løkke, hvor tumoren producerer sit eget vækstsignal, der får den til at vokse hurtigere og blive mere invasiv.
Hvordan Fremmer G-CSF Kræft?
Mekanismerne, hvormed G-CSF kan fremme kræft, er komplekse og involverer både en direkte påvirkning af kræftcellerne og en indirekte manipulation af det omkringliggende væv, kendt som tumormikromiljøet.
Direkte Påvirkning af Kræftceller
- Øget Proliferation: Når G-CSF binder sig til receptorer på kræftceller, kan det aktivere intracellulære signalveje (såsom JAK/STAT, PI3K/AKT og MAPK/ERK), der direkte instruerer cellen i at dele sig hurtigere.
- Fremmet Migration og Invasion: G-CSF kan øge kræftcellers evne til at bevæge sig og invadere omkringliggende væv. Studier har vist en klar sammenhæng mellem høje niveauer af G-CSF i mave- og tarmkræft og spredning til lymfeknuder.
- Overlevelse af Kræftstamceller: Måske mest bekymrende er, at G-CSF ser ud til at kunne understøtte overlevelsen og væksten af en lille population af kræftstamceller. Disse celler menes at være ansvarlige for tilbagefald og resistens over for behandling, da de er svære at udrydde med konventionel kemoterapi.
Manipulation af Tumormikromiljøet
G-CSF's mest potente pro-tumor effekt er måske dets evne til at omforme tumormikromiljøet til at være mere gæstfrit for kræftvækst. Det gør det primært ved at påvirke immunceller:
- Rekruttering af Pro-tumor Immunceller: G-CSF tiltrækker og fremmer udviklingen af immunceller, der i stedet for at bekæmpe kræften, hjælper den. Dette inkluderer M2-makrofager, der fremmer vævsheling og angiogenese (dannelse af nye blodkar, som tumoren har brug for), og myeloid-afledte suppressorceller (MDSC'er), som er notorisk kendte for at undertrykke de T-celler, der ellers ville angribe tumoren.
- Undertrykkelse af Anti-tumor Immunitet: Ved at fremme MDSC'er og regulatoriske T-celler (Tregs) skaber G-CSF et stærkt immunundertrykkende miljø omkring tumoren. Dette fungerer som et usynligt skjold, der beskytter kræftcellerne mod kroppens eget immunforsvar.
G-CSF i Specifikke Kræftformer: En Nærmere Gennemgang
Sammenhængen mellem G-CSF og aggressiv sygdom er blevet observeret i flere kræfttyper, men er særligt veldokumenteret i mave-tarmkræft og brystkræft.
| Kræfttype | Nøglefund | Prognostisk Betydning |
|---|---|---|
| Mave-tarmkræft (især colon og ventrikel) | Både kræftceller og stromaceller (bindevævsceller) producerer G-CSF. Høje niveauer af G-CSF og dets receptor (G-CSFR) er forbundet med øget proliferation, migration og metastase til lymfeknuder. | Markør for aggressiv sygdom og dårligere overlevelse. |
| Brystkræft (især triple-negativ) | Høj G-CSF-ekspression er forbundet med infiltration af pro-tumor M2-makrofager og øget invasivitet. Fremmer MDSC'er, der kan bidrage til kemoresistens. | Forbundet med dårligere samlet overlevelse, især i triple-negative subtyper. |
| Lungekræft (især ikke-småcellet) | Tumor-relateret leukocytose (forhøjet antal hvide blodlegemer) drevet af G-CSF er et tegn på en meget aggressiv tumor med hurtig spredning. | Indikator for kortere overlevelse, selv efter vellykket operation. |
Implikationer for Kræftbehandling og Fremtiden
Denne viden om G-CSF's dobbelte rolle rejser vigtige spørgsmål for den kliniske praksis og fremtidig forskning.

Udfordringer og Overvejelser
Et centralt spørgsmål er, om det er sikkert at give G-CSF til patienter, hvis tumorer potentielt kan reagere på det. Selvom den kortvarige, høje dosis af terapeutisk G-CSF er anderledes end den kroniske, lave dosis produceret af en tumor, er der en teoretisk bekymring for, at man utilsigtet kan fremme tumorvækst eller kemoresistens. Dette understreger behovet for yderligere forskning for at identificere, hvilke patienter der er i risikozonen.
G-CSF og Immunterapi
Fremkomsten af immunterapi, såsom PD-1/PD-L1-hæmmere, har revolutioneret kræftbehandlingen. Disse behandlinger virker ved at fjerne de bremser, som kræftceller sætter på immunsystemet. Men G-CSF's evne til at skabe et immunundertrykkende mikromiljø kan gøre tumorer resistente over for immunterapi. En tumor, der er badet i G-CSF og fyldt med MDSC'er, reagerer muligvis ikke på behandlinger, der er afhængige af en effektiv T-celle-respons.
Fremtidige Strategier: Blokering af G-CSF Signalvejen
Den nye forståelse af G-CSF har åbnet døren for nye behandlingsstrategier. I stedet for kun at tilføre G-CSF, undersøger forskere nu muligheden for at blokere det. Ved at bruge antistoffer mod G-CSF eller dets receptor kunne man potentielt:
- Gøre kemoterapi mere effektiv ved at forhindre G-CSF-drevet resistens.
- Forbedre effekten af immunterapi ved at nedbryde det immunundertrykkende skjold omkring tumoren.
- Direkte hæmme væksten og spredningen af G-CSF-afhængige tumorer.
Kombinationsbehandlinger, hvor man blokerer G-CSF-signalvejen samtidig med at man giver kemo- eller immunterapi, kan vise sig at være en yderst effektiv tilgang for udvalgte patientgrupper i fremtiden.
Ofte Stillede Spørgsmål (FAQ)
Er det farligt at modtage G-CSF under kemoterapi?
For langt de fleste patienter er fordelene ved G-CSF-behandling – at forhindre livstruende infektioner – langt større end de potentielle teoretiske risici. Den terapeutiske brug er kortvarig og designet til at overvinde en akut mangel på hvide blodlegemer. Den kroniske produktion fra en tumor er en helt anden biologisk situation. Læger vurderer altid den enkelte patients situation, men G-CSF forbliver en sikker og essentiel del af den understøttende behandling i kræftplejen.
Kan G-CSF bruges som en markør for kræft?
Meget høje niveauer af G-CSF i blodet, især hvis det ledsages af et unormalt højt antal hvide blodlegemer uden tegn på infektion, kan være en stærk indikator for en G-CSF-producerende tumor. Det bruges ikke som et standard diagnostisk værktøj alene, men det kan give vigtig prognostisk information og pege i retning af en mere aggressiv sygdom.
Hvad er forskellen på, når kroppen laver G-CSF, og når en tumor gør det?
Kroppens produktion af G-CSF er en stramt reguleret og midlertidig proces, der aktiveres som respons på specifikke signaler som f.eks. en infektion. Når infektionen er bekæmpet, falder niveauet igen. En tumor kan derimod producere G-CSF kronisk og ukontrolleret, hvilket skaber et vedvarende pro-tumor og immunundertrykkende miljø, som kroppen ikke er designet til at håndtere.
Afslutningsvis står det klart, at G-CSF er et molekyle med en dyb dualitet. Det er et uundværligt værktøj, der redder liv i den daglige kræftbehandling, men også en potentiel medskyldig i kræftens progression. At forstå og navigere i denne kompleksitet er nøglen til at udvikle smartere og mere personlige behandlingsstrategier, der kan forbedre overlevelsen for kræftpatienter i fremtiden.
Hvis du vil læse andre artikler, der ligner G-CSF: Ven eller Fjende i Kræftbehandling?, kan du besøge kategorien Kræft.
