16/03/2002
Nanopartikel-baserede lægemiddelleveringssystemer er dukket op som en transformerende tilgang inden for moderne terapeutik, der tilbyder forbedret præcision og effektivitet i lægemiddeladministration. Disse bittesmå partikler, typisk mellem 1 og 100 nanometer i størrelse, besidder unikke egenskaber såsom et højt overfladeareal-til-volumen-forhold, forbedret opløselighed og evnen til at målrette specifikke væv eller celler. Disse egenskaber gør dem yderst effektive til at levere terapeutiske midler og åbner døren for en ny æra inden for personlig medicin. I de seneste år har anvendelsen af nanopartikler i lægemidler set betydelige fremskridt, hvilket har ført til udviklingen af nye systemer, der forbedrer biotilgængeligheden, stabiliteten og den kontrollerede frigivelse af lægemidler.
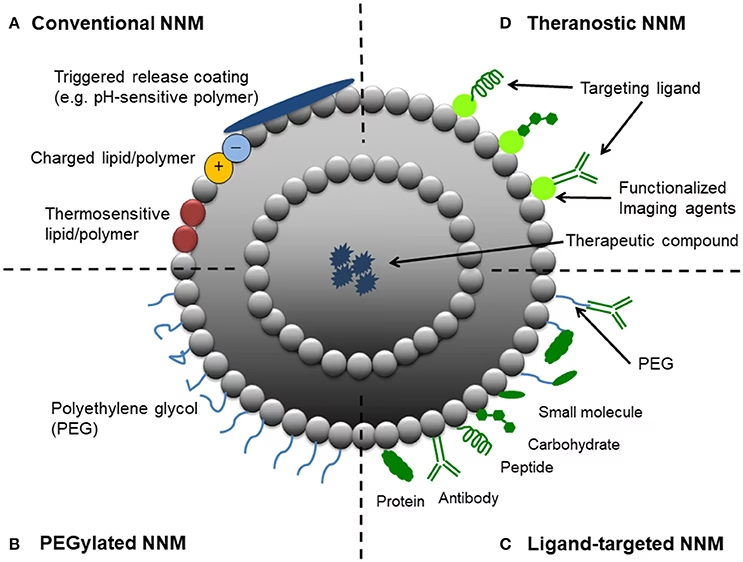
Alsidigheden af nanopartikler strækker sig også til målrettet lægemiddellevering, hvor de kan funktionaliseres med ligander eller antistoffer for specifikt at binde sig til receptorer på syge celler, såsom i kræftterapi. Denne målrettede tilgang minimerer bivirkninger og øger behandlingens effektivitet ved at koncentrere de terapeutiske midler direkte på virkningsstedet. Mens forskningen på dette felt fortsætter med at udvikle sig, forventes nanopartikler at spille en stadig mere afgørende rolle i udviklingen af personlig medicin og avancerede terapeutiske modaliteter. Denne artikel giver en omfattende oversigt over de nuværende tendenser, udfordringer og fremtidsperspektiver inden for nanopartikel-baserede farmaceutiske anvendelser.
Historien om Nanopartikler i Medicin
Konceptet med nanopartikler har udviklet sig markant gennem de sidste par årtier, drevet af fremskridt inden for nanoteknologi og materialevidenskab. Udviklingen af nanopartikler til medicinske anvendelser har været præget af flere vigtige milepæle:
Tidlige Koncepter og Kolloidale Systemer
Rødderne til nanopartikelforskning kan spores tilbage til det tidlige 20. århundrede med studiet af kolloidale systemer. Kolloider, som er suspensioner af partikler i en væske, lagde grundlaget for forståelsen af, hvordan små partikler interagerer med deres omgivelser.
Polymeriske Nanopartikler (1960'erne-1970'erne)
I 1960'erne og 1970'erne opstod polymeriske nanopartikler som lægemiddelbærere. Tidlige studier fokuserede på potentialet i syntetiske polymerer til at indkapsle lægemidler og kontrollere deres frigivelse. Et afgørende øjeblik var i 1976, da Couvreur og kolleger udviklede polyalkylcyanoakrylat (PACA) nanopartikler, hvilket var et af de første eksempler på anvendelsen i lægemiddellevering.
Liposomer som Lægemiddelbærere (1970'erne)
Liposomer, sfæriske vesikler sammensat af lipid-dobbeltlag, blev først beskrevet i 1960'erne og blev hurtigt anerkendt for deres potentiale. I 1970'erne tog forskningen fart, hvilket førte til deres anvendelse til indkapsling af både hydrofile og hydrofobe lægemidler. Udviklingen af Doxil, det første FDA-godkendte liposomale lægemiddel i 1995, understregede den kliniske betydning af nanopartikler.
Fremkomsten af Målrettede og Multifunktionelle Nanopartikler (2000'erne-2010'erne)
De tidlige 2000'ere så udviklingen af målrettede nanopartikler, designet til specifikt at levere lægemidler til syge væv. Dette markerede begyndelsen på "aktiv målretning". I 2010'erne blev multifunktionelle nanopartikler, kendt som "teranostika", introduceret. Disse partikler kan udføre samtidige diagnostiske og terapeutiske funktioner, hvilket muliggør realtidsovervågning af behandlingseffektiviteten.
Typer af Nanopartikler Anvendt i Lægemidler
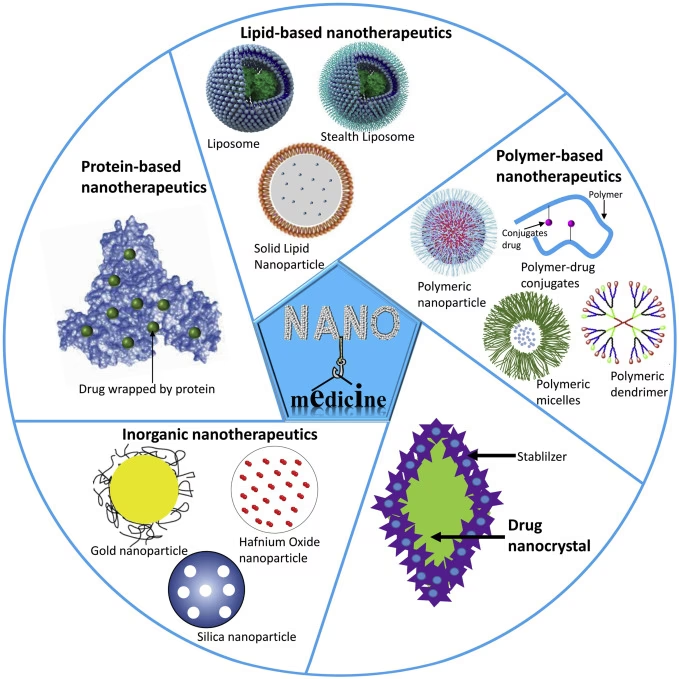
Der findes en række forskellige typer nanopartikler, hver med unikke egenskaber og anvendelsesområder inden for medicin.
- Polymeriske Nanopartikler: Sammensat af naturlige eller syntetiske polymerer. De er meget alsidige og anvendes til kontrolleret frigivelse af en bred vifte af lægemidler, herunder kemoterapeutika, proteiner og vacciner.
- Lipid-baserede Nanopartikler: Inkluderer liposomer, faste lipidnanopartikler (SLN'er) og nanostrukturerede lipidbærere (NLC'er). De er fremragende til at indkapsle både vand- og fedtopløselige lægemidler, beskytte dem mod nedbrydning og forbedre deres optagelse i kroppen.
- Metalliske Nanopartikler: Partikler af guld, sølv og jernoxid bruges til lægemiddellevering, billeddannelse og som terapeutiske midler i sig selv. Guldnanopartikler er kendt for deres høje biokompatibilitet.
- Dendrimerer: Meget forgrenede, træ-lignende polymerer med en veldefineret struktur. Dette giver præcis kontrol over lægemiddelfrigivelse og målretning og muliggør levering af flere lægemidler samtidigt.
- Quantum Dots: Halvledernanopartikler, der udsender lys (fluorescens) og primært bruges til avanceret billeddannelse og diagnostik.
- Magnetiske Nanopartikler: Typisk sammensat af jernoxid. Deres magnetiske egenskaber gør det muligt at styre dem til specifikke steder i kroppen ved hjælp af eksterne magnetfelter, hvilket forbedrer præcisionen i behandlinger som hypertermi ved kræftbehandling.
- Silica Nanopartikler: Kendt for deres stabilitet og porøse struktur, som giver en høj lægemiddelbelastningskapacitet. De bruges ofte som bærere for lægemidler og billeddannelsesmidler.
Mekanismer for Lægemiddellevering med Nanopartikler
Nanopartikler udnytter flere sofistikerede mekanismer til at levere lægemidler effektivt og præcist.
Passiv Målretning
Denne mekanisme er baseret på nanopartiklernes naturlige tendens til at akkumulere i visse væv, især tumorer. Dette skyldes den såkaldte "Enhanced Permeability and Retention" (EPR) effekt. Tumorer har utætte blodkar og dårlig lymfedrænage, hvilket får nanopartikler til at samle sig i tumorvævet. EPR-effekten er en hjørnesten i mange nanopartikel-baserede kræftbehandlinger.
Aktiv Målretning
Ved aktiv målretning modificeres overfladen af nanopartiklerne med specifikke molekyler (ligander, antistoffer), der genkender og binder sig til receptorer på overfladen af målcellerne. Dette sikrer, at lægemidlet leveres direkte til de syge celler, mens raske celler skånes.
Kontrolleret og Stimuli-Responsiv Frigivelse
Nanopartikler kan designes til at frigive deres lægemiddelindhold på en kontrolleret måde over tid. Nogle er "smarte" og reagerer på specifikke stimuli i kroppen, såsom ændringer i pH-værdi, temperatur eller tilstedeværelsen af bestemte enzymer. Dette sikrer, at lægemidlet frigives præcis, hvor og hvornår det er nødvendigt.
Fordele og Ulemper ved Nanopartikel-baseret Lægemiddellevering
Selvom teknologien er yderst lovende, er det vigtigt at overveje både fordele og ulemper.
| Fordele | Ulemper |
|---|---|
| Forbedret biotilgængelighed af lægemidler. | Potentiel toksicitet og inflammatoriske reaktioner. |
| Målrettet levering reducerer bivirkninger. | Kompleks og omkostningstung fremstilling. |
| Kontrolleret og vedvarende frigivelse af medicin. | Udfordringer med regulatorisk godkendelse og sikkerhed. |
| Evne til at krydse biologiske barrierer som blod-hjerne-barrieren. | Risiko for bioakkumulering i organer og miljøet. |
| Mulighed for multifunktionalitet (terapi og diagnostik). | Høje udviklingsomkostninger kan begrænse tilgængelighed. |
Fremtidens Udsigter og Udfordringer
Fremtiden for nanopartikel-teknologi er tæt forbundet med integrationen af kunstig intelligens (AI) til at optimere design og forudsige partiklernes adfærd i kroppen. Dette kan fremskynde udviklingen af mere effektive og sikrere behandlinger. Der er også et stigende fokus på at udvikle bionedbrydelige og miljøvenlige nanopartikler for at imødekomme bekymringer om bioakkumulering og miljøpåvirkning.
På trods af det enorme potentiale er der stadig betydelige udfordringer. Langsigtet toksicitet, komplekse produktionsprocesser og strenge regulatoriske krav er fortsat store forhindringer for en bred klinisk implementering. Kontinuerlig forskning og tværfagligt samarbejde er afgørende for at overvinde disse udfordringer og fuldt ud realisere potentialet i nanopartikel-baserede terapier, hvilket kan revolutionere behandlingen af alt fra kræft til genetiske lidelser.
Ofte Stillede Spørgsmål (FAQ)
Hvad er en nanopartikel?
En nanopartikel er en mikroskopisk partikel med en størrelse på mellem 1 og 100 nanometer. Til sammenligning er et menneskehår omkring 80.000-100.000 nanometer tykt. Deres lille størrelse giver dem unikke fysiske og kemiske egenskaber, som udnyttes i medicin.
Er nanopartikler sikre at bruge i medicin?
Sikkerheden afhænger af typen af nanopartikel, dens størrelse, materiale og overfladekemi. Mange nanopartikler, såsom dem baseret på lipider eller bionedbrydelige polymerer, er designet til at være biokompatible og sikre. Der udføres omfattende toksikologiske studier for at sikre, at de ikke forårsager skade, før de godkendes til klinisk brug.
Hvordan hjælper nanopartikler med at behandle kræft?
Nanopartikler kan indkapsle kemoterapi og levere det direkte til kræftceller. Dette opnås enten passivt via EPR-effekten, hvor partiklerne ophobes i tumorer, eller aktivt ved at udstyre partiklerne med molekyler, der genkender kræftceller. Dette øger effektiviteten og reducerer skaden på raske celler.
Hvad er forskellen på passiv og aktiv målretning?
Passiv målretning udnytter kroppens naturlige processer og tumorens fysiologi (EPR-effekten) til at akkumulere nanopartikler i det syge område. Aktiv målretning er mere specifik og indebærer, at man designer nanopartiklerne til aktivt at søge og binde sig til målceller ved hjælp af overflademonterede "nøgler" (ligander), der passer til "låse" (receptorer) på cellerne.
Hvis du vil læse andre artikler, der ligner Nanopartikler: Fremtidens Målrettede Medicin, kan du besøge kategorien Sundhed.