29/05/2016
Medicinsk udstyr spiller en afgørende rolle i moderne sundhedspleje, hvor det hjælper med at diagnosticere, behandle og overvåge en lang række medicinske tilstande. Fra simple instrumenter som skalpeller til komplekse MR-scannere er innovation inden for dette felt konstant. Men før en ny idé til medicinsk udstyr kan blive til et færdigt produkt på markedet, er det essentielt at evaluere dets levedygtighed og effektivitet. Det er her, et feasibility-studie, eller en gennemførlighedsundersøgelse, kommer ind i billedet. Denne type studie er en grundig analyse, der afgør, om et foreslået produkt er teknisk muligt, kommercielt rentabelt og i overensstemmelse med de strenge lovgivningsmæssige standarder, der gælder for sundhedssektoren. Uden denne indledende analyse risikerer udviklere at spilde enorme summer og utallige arbejdstimer på et projekt, der var dømt til at mislykkes fra starten.
Hvad er formålet med et feasibility-studie for medicinsk udstyr?
Et feasibility-studie tjener flere afgørende formål i udviklingen og kommercialiseringen af medicinsk udstyr. Det er en holistisk vurdering, der belyser projektet fra flere vinkler for at sikre, at alle aspekter er gennemtænkt. De tre primære mål er at bestemme teknisk gennemførlighed, vurdere markedspotentialet og evaluere den regulatoriske overholdelse.
Bestemmelse af Teknisk Gennemførlighed
Den tekniske del af studiet er kernen i at afgøre, om enheden overhovedet kan bygges. Formålet er at få en dybdegående forståelse for enhedens teknologiske krav og vurdere effektiviteten af at implementere den nødvendige teknologi. Dette indebærer en evaluering af:
- Design- og udviklingsudfordringer: Identificering af potentielle tekniske forhindringer og kompleksiteter i designfasen. Kan de nødvendige komponenter skaffes eller udvikles?
- Materialer og processer: Vurdering af, om de valgte materialer er biokompatible, holdbare og egnede til formålet.
- Produktionsmuligheder: Analyse af, om enheden kan fremstilles i stor skala med ensartet kvalitet og inden for et rimeligt budget.
Vurdering af Markedspotentiale
En teknisk genial enhed er værdiløs, hvis der ikke er et marked for den. Derfor er markedsanalyse en vital del af feasibility-studiet. Her indsamles information om efterspørgsel, markedstendenser, kundepræferencer og det konkurrencemæssige landskab. Studiet evaluerer enhedens kommercielle levedygtighed og potentielle rentabilitet, samtidig med at det identificerer eventuelle barrierer eller udfordringer, der kan påvirke dens succes. Spørgsmål, der skal besvares, inkluderer:
- Hvem er den primære målgruppe (patienter, hospitaler, klinikker)?
- Hvilket problem løser enheden, og hvor stort er dette problem?
- Hvem er konkurrenterne, og hvad er deres styrker og svagheder?
- Hvad er enhedens unikke salgsargumenter (Unique Selling Points)?
Evaluering af Regulatorisk Overholdelse
Medicinsk udstyr er underlagt nogle af de strengeste regulativer af alle brancher. Et tidligt feasibility-studie evaluerer enhedens overensstemmelse med gældende regulatorisk lovgivning, standarder, certificeringer og godkendelser (f.eks. CE-mærkning i Europa eller FDA-godkendelse i USA). Dette sikrer, at enheden opfylder de krævede sikkerheds- og kvalitetsstandarder, samtidig med at potentielle regulatoriske risici eller udfordringer identificeres tidligt i udviklings- og kommercialiseringsprocessen. At overse dette trin kan føre til kostbare forsinkelser eller endda en fuldstændig afvisning af produktet.
Processen: Sådan udføres et feasibility-studie
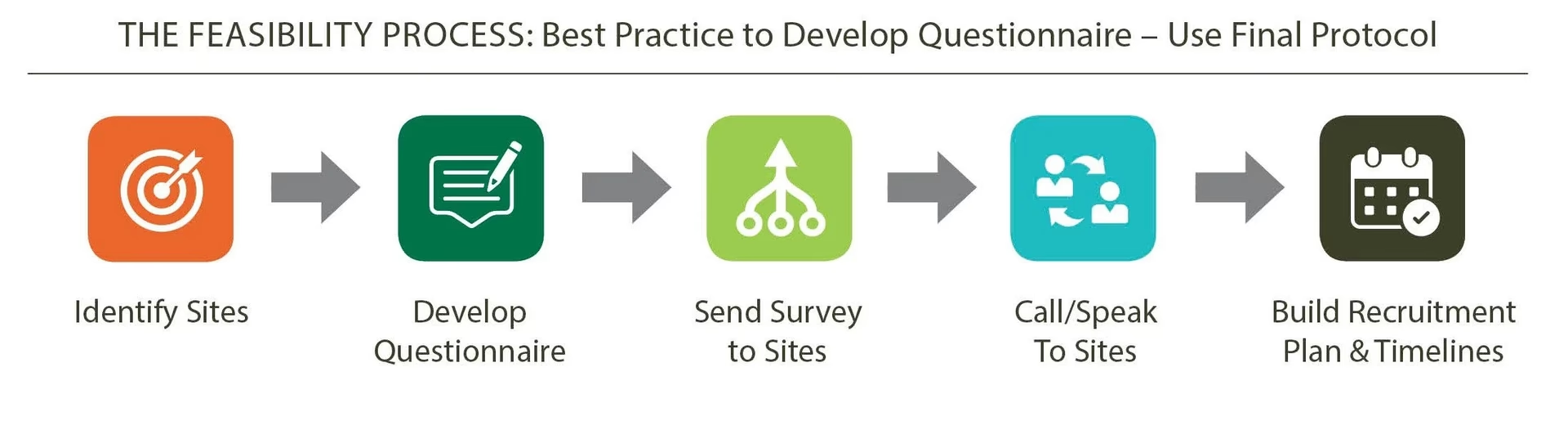
Gennemførelsen af et feasibility-studie følger en struktureret proces for at sikre, at alle relevante områder dækkes grundigt. Processen kan variere afhængigt af enhedens kompleksitet, men følger typisk disse trin:
- Definér Målene: Det første skridt er klart at identificere formålet med studiet, bestemme de specifikke mål, der skal nås, og skitsere de ønskede resultater.
- Identificér Målgruppen: En dyb forståelse af målgruppens karakteristika, behov og præferencer er afgørende for at evaluere markedspotentialet. Dette indebærer at definere den specifikke demografiske eller kundegruppe, enheden sigter mod at betjene.
- Indsaml Markedsdata: Det næste skridt involverer indsamling af information om efterspørgslen efter lignende enheder, markedstendenser, markedsstørrelse, vækstpotentiale og kundepræferencer.
- Analysér Konkurrencelandskabet: For at analysere markedskonkurrencen er det afgørende at undersøge og evaluere eksisterende medicinske enheder eller løsninger. Dette hjælper med at identificere potentielle konkurrenter, forstå deres styrker og svagheder og bestemme de unikke salgsargumenter for den foreslåede enhed.
- Vurdér Tekniske Krav: Studiet evaluerer de tekniske krav til det medicinske udstyr, herunder den nødvendige teknologi, design, udvikling og fremstillingsprocesser. Derudover sigter det mod at identificere eventuelle potentielle tekniske forhindringer eller begrænsninger, der skal løses.
- Gennemgå Regulatoriske Forpligtelser: I dette trin evaluerer udviklerne det regulatoriske landskab og identificerer de nødvendige certificeringer, godkendelser og standarder, som det foreslåede produkt skal opfylde.
- Estimer Finansiel Levedygtighed: Finansielle fremskrivninger, såsom omsætningsprognoser, omkostningsanalyser (udvikling, produktion, markedsføring) og afkastningsanalyser (Return on Investment), udføres for at bestemme enhedens økonomiske potentiale.
Hvornår er et feasibility-studie særligt vigtigt?
Selvom et feasibility-studie er værdifuldt for næsten ethvert medicinsk udstyrsprojekt, er der visse kategorier af enheder, hvor en grundig forundersøgelse er absolut kritisk:
- Nye og nyskabende medicinske anordninger: Enheder, der introducerer unikke løsninger på medicinske udfordringer og ofte involverer banebrydende teknologier eller metoder. Her er usikkerheden størst, og et studie sikrer, at alle aspekter er grundigt gennemgået.
- Innovative Teknologier: Medicinsk udstyr, der inkorporerer innovative teknologier som kunstig intelligens (AI), robotteknologi eller avancerede billeddannelsesteknikker. Disse teknologier kan præsentere hidtil usete tekniske udfordringer og kræver derfor en streng vurdering for at bestemme deres gennemførlighed, ydeevne og sikkerhed.
- Komplekse eller højrisiko-anordninger: Implantérbart medicinsk udstyr (f.eks. pacemakere) eller avancerede diagnostiske værktøjer har ofte indviklede designs eller involverer direkte interaktion med menneskekroppen, hvilket udgør betydelige tekniske og sikkerhedsmæssige udfordringer. Gennem omfattende analyser kan producenter mindske risici, optimere designs og sikre sikkerheden og effektiviteten af disse enheder.
Fra idé til klinik: Feasibility i kliniske forsøg
Når et medicinsk udstyr er blevet anset for at være teknisk, kommercielt og regulatorisk levedygtigt, er næste skridt ofte at bevise dets sikkerhed og effektivitet i praksis gennem kliniske forsøg. Ligesom selve enheden kræver planlægningen af et klinisk forsøg også sin egen, dybdegående feasibility-analyse for at undgå at spilde ressourcer på et upraktisk eller uetisk studie.
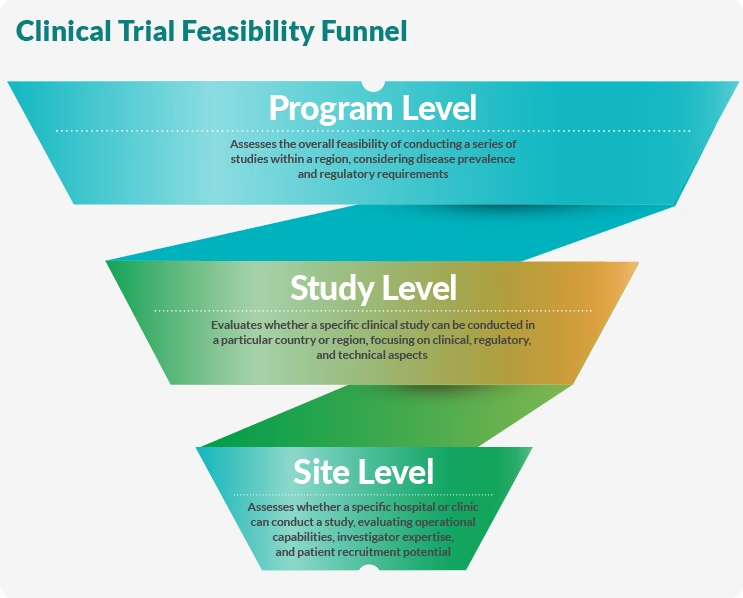
Denne proces kan opdeles i tre niveauer:
- Feasibility på programniveau: Dette er det bredeste niveau, der ser på et helt forskningsprogram eller et terapeutisk område. Man undersøger forekomsten af en sygdom i en bestemt region, eksisterende behandlingsmønstre og de overordnede regulatoriske rammer.
- Feasibility på studieniveau: Her indsnævres fokus til et specifikt klinisk forsøg. Forskere ser på epidemiologiske data for den specifikke patientpopulation, evaluerer om inklusions- og eksklusionskriterierne er realistiske, og undersøger de tekniske krav til selve forsøget.
- Feasibility på lokationsniveau (Site-level): Dette er det mest detaljerede niveau, hvor man vurderer, om et specifikt hospital, en klinik eller en forsker har de nødvendige ressourcer, erfaring og patientpopulation til at gennemføre studiet succesfuldt.
Ved at udføre disse analyser sikrer sponsorer, at kliniske forsøg er veldesignede, patientcentrerede og har en høj sandsynlighed for at blive gennemført med succes.
Udfordringer og løsninger i feasibility-processen
Udførelsen af en feasibility-analyse er ikke uden udfordringer. Nøjagtigheden afhænger stærkt af kvaliteten af den indsamlede data og ekspertisen hos de involverede interessenter. Nogle almindelige udfordringer inkluderer:
- Upræcis dataindsamling: Forskere kan overvurdere antallet af egnede patienter eller et hospitals kapacitet.
- Tids- og ressourcebegrænsninger: Stramme tidsplaner og begrænsede budgetter kan føre til overfladiske undersøgelser.
- Manglende deling af information: Hvis de involverede parter ikke får alle protokol-detaljer, kan de træffe beslutninger baseret på forkerte antagelser.
- Kompleks lovgivning: At navigere i forskellige nationale og internationale regler kan være en stor hindring.
For at overvinde disse udfordringer er der flere best practices, man kan følge. Brug af teknologi, såsom analyse af Real-World Data (RWD) fra elektroniske patientjournaler, kan give mere præcise estimater. Tæt samarbejde mellem alle interessenter – fra ingeniører og klinikere til regulatoriske eksperter – er afgørende. Endelig er det vigtigt at tilpasse feasibility-processen til det specifikke projekt i stedet for at bruge en generisk skabelon.
Sammenligning: Med vs. Uden Feasibility-Studie
| Aspekt | Med Feasibility-Studie | Uden Feasibility-Studie |
|---|---|---|
| Risiko | Risici identificeres og minimeres tidligt i processen. | Høj risiko for tekniske, markedsmæssige og regulatoriske fejl. |
| Ressourceforbrug | Optimeret brug af tid og penge ved at fokusere på levedygtige projekter. | Stort spild af ressourcer på projekter, der er dømt til at mislykkes. |
| Markedssucces | Højere sandsynlighed for succes, da produktet er tilpasset markedets behov. | Lav sandsynlighed for succes; produktet opfylder muligvis ikke et reelt behov. |
| Regulatorisk Godkendelse | Processen for godkendelse er glattere, da kravene er indarbejdet fra starten. | Risiko for afvisning eller store forsinkelser på grund af manglende overholdelse. |
Ofte Stillede Spørgsmål (OSS)
Hvad er et feasibility-studie for medicinsk udstyr?
Et feasibility-studie, eller en gennemførlighedsundersøgelse, er en systematisk analyse, der evaluerer, om et foreslået medicinsk udstyr er teknisk muligt at udvikle, har potentiale til at blive en kommerciel succes, og om det kan opfylde de strenge regulatoriske krav fra sundhedsmyndighederne.
Hvorfor er det så vigtigt at lave et feasibility-studie?
Det er vigtigt, fordi det markant reducerer risikoen for fiasko. Ved at identificere potentielle udfordringer tidligt kan udviklere spare betydelige mængder tid og penge, sikre en mere effektiv ressourceallokering og øge chancerne for at bringe et sikkert og effektivt produkt på markedet.
Hvad er de vigtigste komponenter i et feasibility-studie?
De vigtigste komponenter er en teknisk vurdering (design, materialer, fremstilling), en markedsanalyse (efterspørgsel, konkurrence, rentabilitet) og en regulatorisk evaluering (overholdelse af standarder og love).
Hvem er typisk involveret i processen?
Processen involverer typisk et tværfagligt team bestående af ingeniører, produktdesignere, klinikere, markedsføringsspecialister, regulatoriske eksperter og økonomiske analytikere.
Hvad sker der efter et vellykket feasibility-studie?
Efter et vellykket studie, der konkluderer, at projektet er levedygtigt, fortsætter projektet typisk til de næste faser, som omfatter detaljeret design, prototypeudvikling, testning og ofte planlægning og udførelse af kliniske forsøg for at indsamle data om enhedens sikkerhed og ydeevne.
Hvis du vil læse andre artikler, der ligner Feasibility-studie for Medicinsk Udstyr, kan du besøge kategorien Sundhed.
