28/03/2009
Når du modtager medicin fra apoteket, forventer du med rette, at den er sikker, effektiv og ægte. Desværre udgør forfalskede lægemidler en alvorlig og voksende trussel mod folkesundheden globalt. Disse ulovlige produkter kan indeholde forkerte ingredienser, ingen aktive ingredienser eller endda skadelige stoffer, hvilket kan føre til alvorlig sygdom eller i værste fald død. For at bekæmpe denne trussel og styrke sikkerheden i den lovlige forsyningskæde, introducerede EU Direktivet om Falske Lægemidler (FMD), 2011/62/EU. Denne lovgivning er en hjørnesten i sikringen af patientsikkerhed i hele Europa og har fundamentalt ændret, hvordan medicin spores og verificeres fra producent til patient.

Hvad er Direktivet om Falske Lægemidler (FMD)?
Direktivet om Falske Lægemidler, eller Falsified Medicines Directive (FMD), trådte i fuld kraft den 9. februar 2019. Dets primære formål er at forhindre, at forfalskede lægemidler trænger ind i den legale forsyningskæde. Dette gøres ved at implementere et robust, paneuropæisk system til verifikation af lægemidler. Direktivet pålægger lægemiddelproducenter at anbringe to obligatoriske sikkerhedsforanstaltninger på emballagen til de fleste receptpligtige lægemidler.
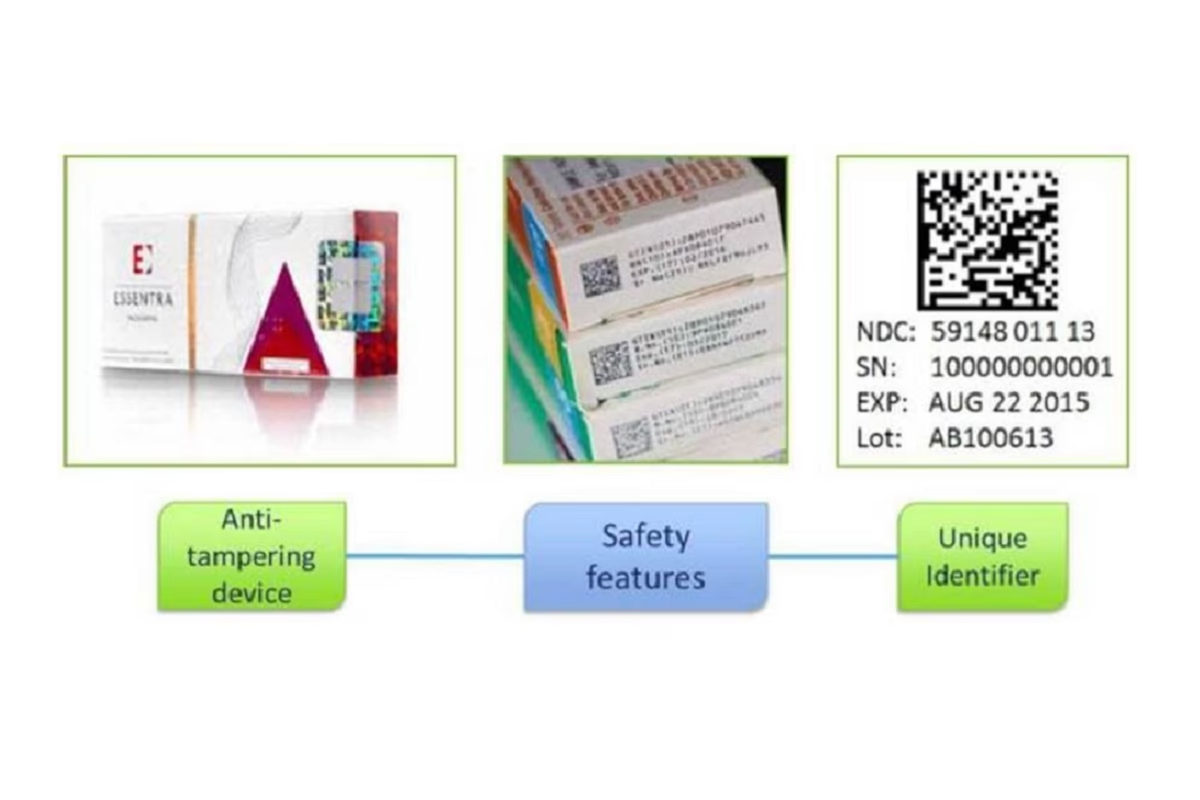
Disse to foranstaltninger er kernen i systemet:
- En unik identifikator (UI): En unik 2D-datamatrixkode, der er specifik for hver enkelt lægemiddelpakke.
- En anbrudssikring (ATD - Anti-Tampering Device): En forsegling, der tydeligt viser, om pakken har været åbnet eller manipuleret.
Sammen sikrer disse funktioner, at hver pakke medicin kan autentificeres og spores, hvilket gør det ekstremt vanskeligt for forfalskninger at komme i omløb via apoteker og hospitaler.
Hvordan Fungerer Verifikationssystemet i Praksis?
FMD's succes afhænger af et komplekst, men effektivt, digitalt økosystem, der forbinder alle aktører i forsyningskæden. Processen kan opdeles i flere trin:
- Produktion og Upload: Når en lægemiddelproducent producerer en pakke medicin, genererer de en unik identifikator (UI). Denne UI, som indeholder produktkode, serienummer, batchnummer og udløbsdato, printes på pakken i form af en 2D-datamatrixkode. Samtidig uploades oplysningerne fra denne UI til en central europæisk database, kendt som European Medicines Verification System (EMVS).
- Distribution til Nationale Systemer: Fra den europæiske hub (EMVS) distribueres dataene sikkert til de nationale verifikationssystemer (NMVS) i de lande, hvor medicinen skal sælges. I Danmark varetages denne opgave af DMVO (Danish Medicines Verification Organisation).
- Verifikation ved Dispensering: Det afgørende skridt sker i slutningen af kæden. Når en apoteker eller hospitalspersonale skal udlevere medicin til en patient, scanner de 2D-koden på pakken.
- Systemtjek og Deaktivering: Scanningssoftwaren kommunikerer øjeblikkeligt med det nationale system (f.eks. DMVO i Danmark) for at verificere, at den unikke identifikator er gyldig og aktiv i databasen. Hvis koden er gyldig, bliver den deaktiveret (eller 'dekommissioneret') i realtid. Dette forhindrer, at den samme kode kan bruges igen, og fungerer som en digital lås, der fuldfører pakkens rejse.
- Alarmering ved Uoverensstemmelser: Hvis systemet opdager et problem – f.eks. at koden er ukendt, allerede er blevet deaktiveret, eller er udløbet – udløses en alarm. Dette giver apotekeren besked om ikke at udlevere medicinen og iværksætte en undersøgelse.
Dette end-to-end verifikationssystem skaber en digital barriere, der er yderst vanskelig for forfalskede produkter at trænge igennem.
Trin til Overholdelse for Organisationer
Implementeringen af FMD var en stor opgave for hele lægemiddelindustrien, fra de største producenter til det mindste lokale apotek. For at sikre en vellykket overgang var en omhyggelig og velovervejet tilgang nødvendig. Nøglen til succes ligger i en kombination af procesoptimering, teknologivalg og medarbejderinddragelse.
Gennemgang af Eksisterende Processer
Før implementering af ny teknologi er det afgørende at analysere og forstå de nuværende arbejdsgange. Målet er at integrere FMD-kravene med mindst mulig forstyrrelse af den daglige drift. Ved at inddrage de operationelle teams, der arbejder med medicinen hver dag, sikres det, at de nye løsninger er praktiske og effektive. En velstyret implementering, understøttet af grundig træning og åben kommunikation, er essentiel for en hurtig og problemfri lancering.
Valg af den Rette Teknologi
Teknologi spiller en central rolle i at reducere fejl og sikre nøjagtighed. Valget afhænger i høj grad af driftsvolumen. Store distributionscentre kan have brug for semi-automatiserede eller fuldautomatiske scanningsløsninger for at håndtere store mængder medicin hurtigt og præcist. Mindre apoteker kan måske klare sig med simple håndholdte scannere, men skal til gengæld have robuste manuelle procedurer på plads for at undgå fejl. Det er vigtigt at undgå systemer, der er låst til specifik hardware eller software, da dette kan begrænse fremtidig fleksibilitet og skalerbarhed.
Skab Merværdi for Forretningen
Selvom overholdelse af lovgivning ofte ses som en omkostning, kan FMD-implementering faktisk skabe værdi. Ved at digitalisere og optimere forsyningskæden kan virksomheder opnå større effektivitet, færre fejl og bedre sporbarhed. De data, der genereres gennem systemet, kan give værdifuld indsigt, der kan bruges til at forbedre lagerstyring, forudsige efterspørgsel og håndtere tilbagekaldelser mere effektivt. Dermed kan en regulatorisk byrde omdannes til en forretningsmæssig fordel.

Sammenligning: Før og Efter FMD
For at illustrere den markante forbedring i lægemiddelsikkerheden, kan man sammenligne situationen før og efter direktivets implementering.
| Aspekt | Før FMD | Efter FMD |
|---|---|---|
| Pakkesikkerhed | Variabel, ofte uden fysisk forsegling. | Obligatorisk anbrudssikring (ATD) på de fleste pakker. |
| Identifikation | Primært batchnummer og udløbsdato. | En unik identifikator (2D-kode) på hver enkelt pakke. |
| Verifikation | Manuel og visuel inspektion af pakken. | Obligatorisk elektronisk scanning og verifikation mod en national database. |
| Sporbarhed | Begrænset til batch-niveau, hvilket gør tilbagekaldelser besværlige. | Fuld sporbarhed på individuelt pakkeniveau fra producent til patient. |
| Patientrisiko | Højere risiko for, at forfalskede lægemidler når patienten. | Markant reduceret risiko takket være multiple sikkerhedslag. |
Ofte Stillede Spørgsmål (OSS)
Hvad defineres som et forfalsket lægemiddel?
Et forfalsket lægemiddel er et lægemiddel, der bevidst og svigagtigt er mærket forkert med hensyn til dets identitet, kilde eller historik. Det kan indeholde ingredienser af lav kvalitet, forkerte doser, slet ingen aktiv ingrediens eller endda giftige stoffer.
Gælder FMD for al medicin?
Nej, direktivet gælder primært for receptpligtig medicin. De fleste håndkøbslægemidler er undtaget, medmindre de er vurderet til at have en høj risiko for forfalskning. Omvendt er visse receptpligtige lægemidler, hvor risikoen for forfalskning anses for at være meget lav, også undtaget.
Hvad sker der, hvis en scanning udløser en alarm på apoteket?
Hvis en pakke udløser en alarm, må den ikke udleveres til patienten. Apotekspersonalet skal sætte pakken i karantæne og følge nationale procedurer for at undersøge årsagen. Dette kan involvere kontakt til producenten og de nationale lægemiddelmyndigheder for at afgøre, om der er tale om en teknisk fejl eller en potentiel forfalskning.
Har Brexit påvirket FMD?
Ja. Efter Brexit er Storbritannien (med undtagelse af Nordirland) ikke længere en del af EU's FMD-system. De har arbejdet på at udvikle deres eget nationale system for at sikre lægemiddelforsyningen. For lægemidler, der handles mellem EU og Storbritannien, gælder der nu specifikke regler.
Konklusion
Direktivet om Falske Lægemidler (FMD) repræsenterer et af de mest betydningsfulde fremskridt inden for patientsikkerhed i nyere tid. Ved at skabe et sammenhængende og robust system for verifikation på tværs af Europa, har FMD opbygget en stærk forsvarslinje mod den alvorlige trussel fra forfalskede lægemidler. Selvom implementeringen har været en kompleks udfordring for industrien, er fordelene uomtvistelige: øget tillid, forbedret sporbarhed og, vigtigst af alt, en langt større sikkerhed for, at den medicin, patienter modtager, er ægte og sikker.
Hvis du vil læse andre artikler, der ligner FMD: Beskyttelse mod Falske Lægemidler i EU, kan du besøge kategorien Sundhed.