18/05/2022
I den moderne medicinske verden er begrebet evidensbaseret medicin (EBM) blevet en grundpille. Det handler i sin essens om at finde det bedste tilgængelige bevis og bruge det til at træffe velinformerede kliniske beslutninger for patientbehandling. En central del af EBM er et hierarkisk system til at klassificere styrken af den videnskabelige evidens. Dette system, kendt som evidensniveauer, fungerer som en vejledning for læger og forskere til at vurdere kvaliteten af forskning og dens pålidelighed. At forstå disse niveauer er ikke kun afgørende for sundhedsprofessionelle, men også for patienter, der ønsker at forstå grundlaget for deres behandlingsplaner. Denne artikel vil udforske oprindelsen, betydningen og anvendelsen af evidensniveauer i medicin.
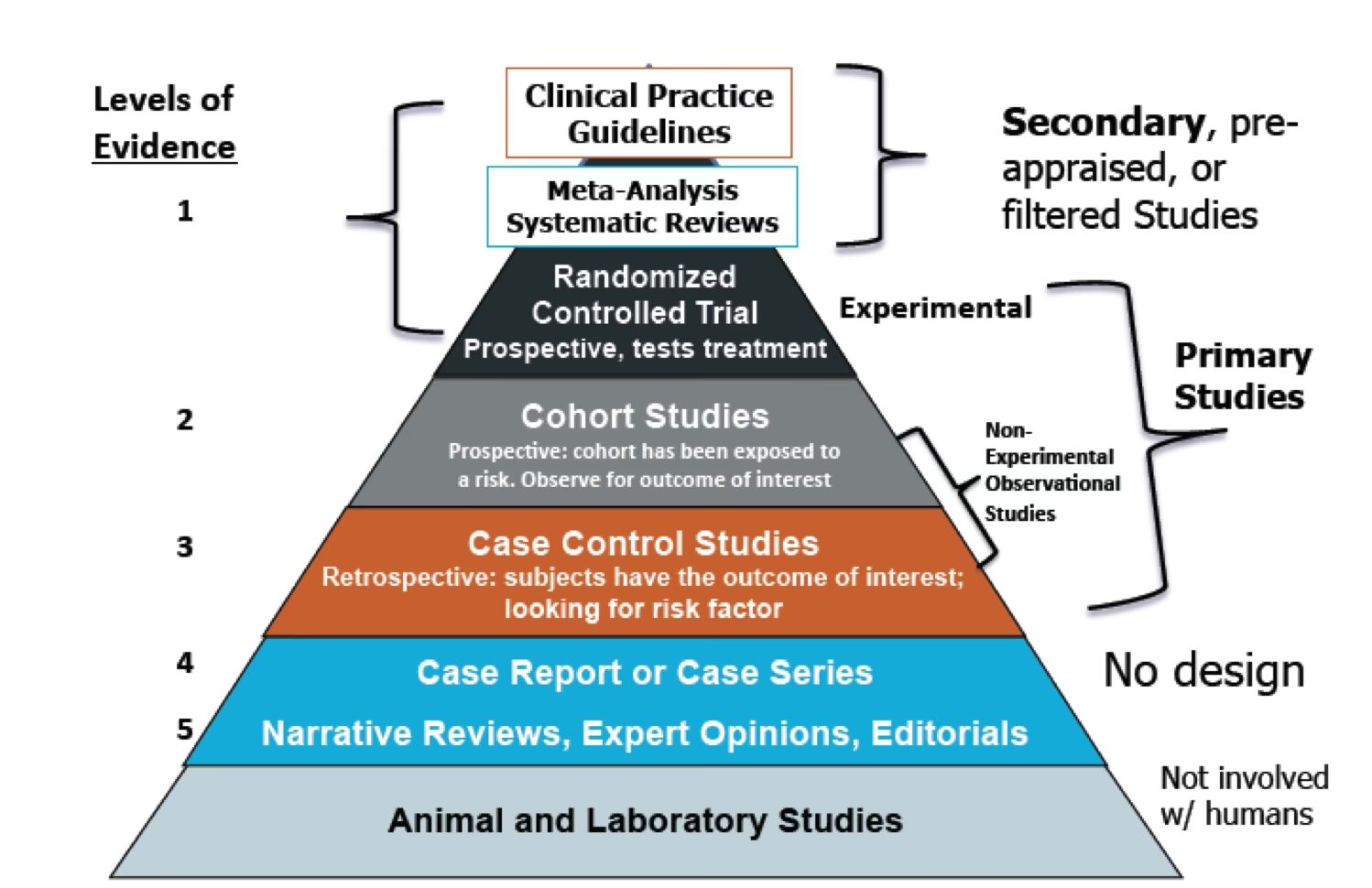
Historien bag Evidensniveauer
Konceptet med formelt at rangordne medicinsk evidens er ikke nyt, men det blev systematiseret og populariseret med fremkomsten af EBM-bevægelsen. Den første formelle beskrivelse af evidensniveauer kom i en rapport fra Canadian Task Force on the Periodic Health Examination i 1979. Formålet med rapporten var at udvikle anbefalinger til periodiske helbredsundersøgelser baseret på en systematisk gennemgang af den medicinske litteratur. Forfatterne skabte et system til at vurdere evidensens styrke, som direkte påvirkede styrken af deres anbefalinger. For eksempel krævede en 'Grad A' anbefaling, at der var god evidens for at inkludere en bestemt undersøgelse.
Dette system blev yderligere udviklet og udvidet af David Sackett, en af pionererne inden for evidensbaseret medicin, i en artikel fra 1989. Begge systemer placerede randomiserede kontrollerede forsøg (RCT'er) øverst i hierarkiet og caseserier eller ekspertudtalelser nederst. Denne rangordning er baseret på sandsynligheden for systematisk fejl, også kendt som bias.
Sammenligning af Tidlige Klassifikationssystemer
For at illustrere udviklingen er her en oversigt over de to tidlige og indflydelsesrige systemer.
Tabel 1: Canadian Task Force's Evidensniveauer (1979)
| Niveau | Type af Evidens |
|---|---|
| I | Mindst ét randomiseret kontrolleret forsøg (RCT) med korrekt randomisering. |
| II.1 | Veldesignede kohorte- eller case-kontrolstudier. |
| II.2 | Tidsserie-sammenligninger eller dramatiske resultater fra ukontrollerede studier. |
| III | Ekspertudtalelser, baseret på klinisk erfaring uden eksplicit kritisk vurdering. |
Tabel 2: Sacketts Evidensniveauer (1989)
| Niveau | Type af Evidens |
|---|---|
| I | Store RCT'er med entydige og klare resultater. |
| II | Små RCT'er med uklare resultater. |
| III | Kohorte- og case-kontrolstudier. |
| IV | Historiske kohorte- eller case-kontrolstudier. |
| V | Caseserier og studier uden kontrolgrupper. |
Hvorfor er et Hierarki af Evidens Vigtigt?
Hovedårsagen til at rangordne studier er at minimere risikoen for bias. Bias er systematiske fejl i et studies design, udførelse eller analyse, som kan føre til misvisende resultater. RCT'er anses for at være 'guldstandarden' for klinisk forskning, fordi de er designet til at være så objektive som muligt. Ved tilfældigt at tildele deltagere til enten en behandlingsgruppe eller en kontrolgruppe, minimerer forskerne indflydelsen fra forstyrrende faktorer (confounders), som ellers kunne påvirke resultatet. Dette sikrer, at en eventuel observeret forskel mellem grupperne med stor sandsynlighed skyldes den undersøgte intervention.
I modsætning hertil er studier på lavere niveauer, såsom caseserier eller ekspertudtalelser, meget mere modtagelige for bias. En ekspertudtalelse kan være farvet af personlig erfaring, og en caseserie mangler en sammenligningsgruppe, hvilket gør det umuligt at afgøre, om de observerede resultater ville være sket alligevel. Selvom disse typer evidens kan være værdifulde til at generere nye hypoteser, er de ikke pålidelige nok til at basere vigtige kliniske beslutninger på alene.
Moderne Klassificeringssystemer og Tilpasninger
Siden de første systemer blev introduceret, har mange organisationer og tidsskrifter udviklet deres egne variationer. Det blev hurtigt anerkendt, at forskellige kliniske spørgsmål kræver forskellige typer af evidens. Et spørgsmål om en behandlings effektivitet besvares bedst med et RCT, mens et spørgsmål om prognose (sygdomsforløb) bedst besvares med et kohortestudie.

Et af de mest anerkendte moderne systemer er GRADE (Grading of Recommendations Assessment, Development and Evaluation). GRADE-tilgangen vurderer ikke kun studiets design, men også andre faktorer, der kan påvirke tilliden til resultaterne, såsom studiets kvalitet, konsistens mellem studier og præcisionen af resultaterne.
GRADE-tilgangen til Evidenskvalitet
GRADE klassificerer evidensens kvalitet i fire niveauer:
- Høj: Vi er meget sikre på, at den sande effekt ligger tæt på den estimerede effekt.
- Moderat: Vi er moderat sikre på den estimerede effekt. Den sande effekt er sandsynligvis tæt på estimatet, men der er en mulighed for, at den er væsentligt anderledes.
- Lav: Vores tillid til den estimerede effekt er begrænset. Den sande effekt kan være væsentligt anderledes.
- Meget lav: Vi har meget lidt tillid til den estimerede effekt. Den sande effekt er sandsynligvis væsentligt anderledes.
GRADE starter typisk med at klassificere evidens fra RCT'er som høj kvalitet og observationsstudier som lav kvalitet, men justerer derefter op eller ned baseret på en række faktorer. For eksempel kan et veludført observationsstudie med en stor effekt opgraderes, mens et RCT med alvorlige metodologiske fejl kan nedgraderes.
Fra Evidens til Kliniske Anbefalinger
At have et evidenshierarki er kun det første skridt. Det næste er at omsætte denne evidens til konkrete kliniske anbefalinger. Systemer som det udviklet af American Society of Plastic Surgeons (ASPS) forbinder evidensniveauet direkte med styrken af en anbefaling.
Tabel 3: Eksempel på Anbefalingsgrader
| Grad | Beskrivelse | Kvalificerende Evidens | Implikationer for Praksis |
|---|---|---|---|
| A | Stærk anbefaling | Niveau I evidens eller konsistente fund fra flere studier på niveau II, III eller IV. | Klinikere bør følge anbefalingen, medmindre der er en klar og overbevisende grund til at gøre anderledes. |
| B | Anbefaling | Niveau II, III eller IV evidens og generelt konsistente fund. | Klinikere bør generelt følge anbefalingen, men være opmærksomme på ny information og patientpræferencer. |
| C | Mulighed | Niveau II, III eller IV evidens, men inkonsistente fund. | Klinikere bør være fleksible. Patientpræferencer bør have en væsentlig indflydelse. |
| D | Mulighed | Niveau V evidens: lidt eller ingen systematisk empirisk evidens. | Klinikere bør overveje alle muligheder. Patientpræferencer bør have en væsentlig indflydelse. |
Fortolkning af Evidensniveauer: Mere end Bare et Tal
Det er afgørende at forstå, at et højt evidensniveau ikke automatisk garanterer høj kvalitet. Et dårligt udført RCT kan give mere misvisende resultater end et veludført kohortestudie. Læsere af medicinsk litteratur skal derfor altid vurdere kvaliteten af det enkelte studie kritisk. Værktøjer som Jadad-skalaen er udviklet til at bedømme kvaliteten af RCT'er, men selv uden formelle skalaer kan man kigge efter nøgleelementer:
- Randomisering: Var tildelingen til grupperne virkelig tilfældig?
- Blinding: Vidste patienter, behandlere eller resultatvurderere, hvem der fik hvilken behandling? Dobbelt-blinding (hvor hverken patient eller behandler ved det) er idealet.
- Frafald: Blev der redegjort for alle deltagere, der startede i studiet? Et stort og ujævnt frafald kan introducere bias.
- Power-analyse: Var studiet stort nok til at opdage en klinisk relevant forskel, hvis en sådan eksisterede? Underpowered studier kan fejlagtigt konkludere, at der ingen effekt er.
Kliniske Eksempler: Evidensniveauer i Praksis
For at illustrere, hvordan evidenshierarkiet fungerer i den virkelige verden, er her to eksempler fra medicinsk historie.
Eksempel 1: Silikoneimplantater og Lymfom
Baseret på en række caserapporter (laveste evidensniveau, IV eller V) opstod en hypotese om en mulig sammenhæng mellem silikonebrystimplantater og lymfom (lymfekræft). Disse caserapporter var nok til at skabe bekymring og anspore til yderligere forskning. Efterfølgende blev der udført flere store, retrospektive kohortestudier (højere evidensniveau, II) i USA, Canada og Skandinavien. Ingen af disse studier fandt en statistisk signifikant øget risiko. Til sidst blev resultaterne fra disse kohortestudier samlet i et systematisk review og en meta-analyse (højeste evidensniveau, I). Denne analyse bekræftede, at der ikke var nogen øget risiko. Dette eksempel viser, hvordan lavniveauevidens kan generere en hypotese, som derefter kan testes og modbevises af studier med et stærkere design.
Eksempel 2: Adrenalin i Fingrene
I årtier blev læger undervist i, at injektion af lokalbedøvelse med adrenalin i fingrene var farligt og kunne føre til koldbrand (iskæmi). Denne læresætning var baseret på caserapporter fra før 1950 (niveau IV/V evidens). Denne "sandhed" blev videreført i lærebøger i generationer. En grundig litteraturgennemgang afslørede dog senere, at de oprindelige tilfælde sandsynligvis skyldtes en forurenet formulering af lokalbedøvelsen, ikke adrenalinen i sig selv. Efterfølgende kohortestudier (niveau II evidens) har vist, at brugen af adrenalin i fingrene er sikker. Dette eksempel illustrerer faren ved at basere klinisk praksis på lavniveauevidens og vigtigheden af konstant at genoverveje etablerede dogmer i lyset af ny og bedre evidens.

Konklusion
Evidensniveauer er en uundværlig del af evidensbaseret medicin. De giver en ramme til at vurdere og prioritere den enorme mængde af medicinsk information, der publiceres hver dag. Ved at forstå hierarkiet – fra de robuste, systematiske reviews øverst til de hypotesegenererende caserapporter nederst – kan både læger og patienter træffe bedre og mere sikre beslutninger om sundhed og behandling. Det er dog vigtigt at huske, at systemet er en vejledning, ikke en lov. Kritisk vurdering af hvert enkelt studie er altid nødvendigt for at sikre, at den bedste tilgængelige evidens anvendes korrekt.
Ofte Stillede Spørgsmål (FAQ)
Hvad er evidensbaseret medicin (EBM)?
Evidensbaseret medicin er en tilgang til lægepraksis, hvor kliniske beslutninger træffes ved samvittighedsfuldt, eksplicit og velovervejet at bruge den bedste tilgængelige videnskabelige evidens, kombineret med klinikerens ekspertise og patientens værdier og præferencer.
Hvorfor er et randomiseret kontrolleret forsøg (RCT) anset for at være så stærk evidens?
Et RCT anses for at være 'guldstandarden', fordi randomiseringen minimerer risikoen for selektionsbias og forstyrrende faktorer. Dette betyder, at forskelle i resultater mellem behandlings- og kontrolgruppen med stor sandsynlighed kan tilskrives selve behandlingen, hvilket giver en stærk indikation af årsag og virkning.
Betyder et lavt evidensniveau, at en undersøgelse er ubrugelig?
Nej, slet ikke. Studier med lavere evidensniveauer, som f.eks. caserapporter og caseserier, spiller en vigtig rolle. De er ofte de første til at beskrive nye sygdomme, sjældne bivirkninger eller innovative behandlinger. De er afgørende for at generere hypoteser, som derefter kan testes i studier med et stærkere design, som f.eks. RCT'er.
Hvordan bruges evidensniveauer i praksis af læger?
Læger bruger evidensniveauer til hurtigt at vurdere troværdigheden af nye forskningsresultater. Når de står over for en klinisk beslutning, vil de søge efter den højest mulige evidens. Kliniske retningslinjer, som er udarbejdet af ekspertgrupper, bygger ofte deres anbefalinger på en systematisk gennemgang af litteraturen, hvor evidensens niveau og kvalitet er centralt for anbefalingens styrke.
Hvad er en meta-analyse?
En meta-analyse er en statistisk teknik, der bruges i et systematisk review til at kombinere resultaterne fra flere uafhængige, men lignende, studier. Ved at samle data fra mange studier kan en meta-analyse give et mere præcist og pålideligt estimat af en behandlings effekt, end et enkelt studie alene kan. Den placeres ofte øverst i evidenshierarkiet.
Hvis du vil læse andre artikler, der ligner Evidensniveauer i Medicin: En Komplet Guide, kan du besøge kategorien Medicin.
